A indústria química utiliza a fluorita (CaF2)para a obtenção do flúor elementar, de diversos produtos químicos designados genericamente de fluoroquímicos e do ácido fluorídrico (HF). O fluoreto de cálcio apresenta baixa solubilidade em água e sua constante do produto de solubilidade a 25C, é 3,9 x 10–11. A solubilidade do fluoreto de cálcio em uma solução 0,10 mol.L–1 de fluoreto de sódio nessa temperatura é, em mol.L–1:
As cirurgias no globo ocular geram dor e, em alguns casos, inflamação após procedimento. Um anestésico de ação local, a base de proparacaina,
tem sido utilizado nestas intervençõess e tem diminuido as complicagoes no pos-operatorio. Um método de síntese da proparacaina envolve inicialmente
a reação:
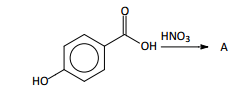
H A estrutura do composto representado por A é: 0
Uma ampla variedade de compostos químicos utilizados como
herbicida apresenta alto potencial de contaminação de águas
subterrâneas.
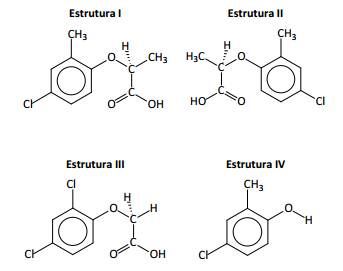
Os compostos, cujas estruturas estão representadas acima, fazem
parte de uma formulação comercializada para aplicação em
cultivos de trigo e cevada.
Analise as estruturas e assinale a afirmativa correta.
A célula eletroquímica hipotética, representada por
X (s) │ X2+ (1,00 mol.L–1) ││ Cu2+ (0,01 mol.L–1) │ Cu (s)
apresentou potencial igual 0,686 volts.
Esta célula hipotética foi construída por duas semi‐células, uma
formada por um eletrodo desconhecido imerso em uma solução
de concentração 1,00 mol.L–1 contendo seus cátions X´2+ e outra
formada por um eletrodo de cobre imerso em uma solução
diluída com íons Cu2+ na concentração 0,01 mol.L–1.
Nas condições do enunciado, os eletrodos apresentam os
potenciais padrão:
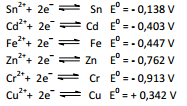
Nestas condições, X é o
Segundo a Lei Complementar n. 125/07, a Superintendência do Desenvolvimento do Nordeste (SUDENE) tem natureza
O servidor estável só perdera o cargo em virtude de sentença judicial transitada em julgado ou de processo administrativo disciplinar no qual
lhe seja assegurada ampla defesa. Com relação ao Processo Administrativo Disciplinar, assinale a afirmativa correta.
Uma amostra de 0,100 g de propano foi queimada com excesso de oxigênio em um calorímetro calibrado de pressão constante, cuja capacidade calorífera é de 520 J.C–1. Nessa experiência a temperatura do calorímetro aumentou 9,62ºC. Utilizando os dados apresentados, a entalpia de combustão do propano em kJ.mol–1 é aproximadamente: Dados: Massa molar (g.mol–1): H = 1 C = 12
A decomposição do NOCl pode ser descrita pela reação
elementar: 2NOCl(g) → 2NO(g)+Cl2(g).
Sendo a velocidade dessa reação dada em mol.L–1 . s–1, a sua
constante de velocidade será expressa em
O S-metolacloro é representado pela formula:
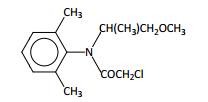
Este é o ingrediente ativo de um herbicida de use geral, aplicado no controle de ervas daninhas. Existem evidencias da contaminação de águas
subterrâneas e superficiais por esse herbicida e também de bioacumulag5o em peixes. Na estrutura do S-metolacloro estão presentes as funções orgânicas
As propriedades químicas de uma substância podem se relacionar
com o seu pKa determinado por métodos simples como titulação,
condutimetria e ultravioleta. Os valores dos pKa de três ácidos
carboxílicos foram determinados: ácido benzóico ( I), ácido‐p‐
metil‐benzóico (II ) e ácido‐p‐cloro‐benzóico ( III).
A ordem crescente dos pKa desses ácidos é
O uso indiscriminado de compostos orgânicos sintéticos
persistentes e acumulativos e as descargas de agentes
contaminantes têm provocado a degradação de alguns
ecossistemas aquáticos. Alguns desses compostos são
potencialmente cancerígenos e podem provocar efeitos
negativos na reprodução ou no desenvolvimento dos seres
humanos.
O Conselho Nacional do Meio Ambiente estabelece parâmetros
para enquadrar corpos d'água em classes. Cientistas avaliaram as
concentrações de endossulfan e dieldrin em três amostras
distintas de água e compararam com os parâmetros
apresentados na legislação.
Os dados deste estudo estão apresentados na tabela a seguir:
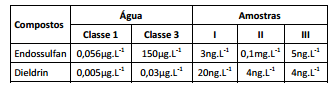
concentrações de endossulfan e dieldrin, são classificadas como
Uma reação de oxidação do ácido acético com permanganato de potássio em meio ácido fornece como produtos sulfato de potássio, sulfato de manganês (II), dióxido de carbono e água. Na equação que representa essa reação balanceada com os menores coeficientes estequiométricos inteiros, o coeficiente estequiométrico da água é
Os filmes finos são usados em microeletrônica como condutores,
resistores, capacitores e em revestimentos óticos em lentes.
Esses filmes podem ser produzidos pela deposição de vapor
químico, utilizando tetrabrometo de titânio que é evaporado e
misturado com hidrogênio gasoso. A mistura é passada sobre
uma superfície aquecida a aproximadamente 1300ºC. O haleto
metálico sofre reação com hidrogênio para formar um
revestimento de titânio metálico.
A massa máxima de titânio metálico que poderá ser produzida
quando 8 mol de gás hidrogênio reagem com o tetrabrometo de
titânio, considerando um rendimento de 100% no processo, é:
Dados: Massa molar (g.mol–1): H = 1Ti = 48 Br=80
A expressão “efeito estufa” indica o fenômeno natural responsável pelo aumento da temperatura da atmosfera terrestre. Desde o final do século XIX temos assistido a um aumento gradual da temperatura global, algo que pode também ser causado pela flutuação natural de temperatura. Esses fenômenos naturais bastante complexos e imprevisíveis podem ser a explicação para as alterações climáticas que a Terra tem sofrido, mas também é possível e mais provável que estejam sendo provocados pelo aumento do efeito estufa, basicamente relacionado à atividade humana. O dióxido de carbono vem sendo acusado de ser o principal responsável pelo aumento do efeito estufa devido à absorção de radiação na região do Infravermelho por essa substância. Essa radiação interage com moléculas por meio de suas ligações interatômicas. Com relação às características da molécula do dióxido de carbono, analise as afirmativas a seguir. I.A molécula de CO2 possui geometria linear e no estado fundamental o momento dipolar é igual a zero. II.A molécula de CO2 possui modo de vibração conhecido como deformação axial simétrica. III. A molécula de CO2 possui modo de vibração conhecidos como deformação angular simétrica. Assinale:
Os compostos de enxofre, sobretudo o dióxido de enxofre, SO2, esteio entre os gases poluentes mais comuns. Vários métodos tem sido
desenvolvidos para a remoção de SO2 dos gases formados quando o carvão o petróleo seio queimados. o calcário em pó pode ser injetado no forno de uma usina de energia, onde se decompõe em Ca0 e CO2, sendo o processo de remoção de SO2 ilustrado no esquema a seguir:
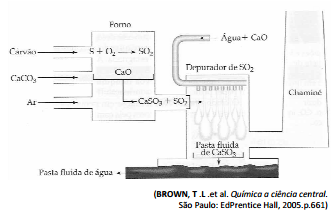
Considerando que com esse processo é possível retirar todo o SO2 produzido na queima
do carvão, o numero de moléculas desse gás que deixariam de atingir a atmosfera, reagindo totalmente 28kg de CaO, é
Dados: Massa molar (g.mor1): 0 = 16Ca = 40

