Acerca da termoquímica, julgue os itens subsequentes.
O valor calorífico de um combustível é medido a partir do calor de absorção que ele apresenta.
No contexto a que se refere o fragmento de texto anterior, a energia vibracional é
Considere o diagrama de energia para a reação X + Y → Z.
Os intervalos I, II e III representam, correta e respectivamente,
A combustão tem sua origem quando uma energia de ignição é fornecida para um sistema formado por um composto que atua como combustível e um composto que atua como comburente, normalmente o gás oxigênio.
Sobre as reações de combustão, assinale a alternativa correta.
O gás hidrogênio é considerado um ótimo combustível — o único produto da combustão desse gás é o vapor de água, como mostrado na equação química.
![]()
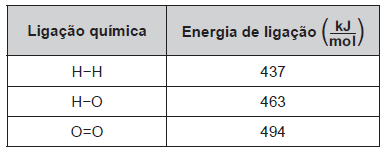
Um cilindro contém 1 kg de hidrogênio e todo esse gás foi queimado. Nessa reação, são rompidas e formadas ligações químicas que envolvem as energias listadas no quadro.
Massas molares ![]()
Qual é a variação da entalpia, em quilojoule, da reação de combustão do hidrogênio contido no cilindro?
Em uma aula experimental de calorimetria, uma professora queimou 2,5 g de castanha-de-caju crua para aquecer 350 g de água, em um recipiente apropriado para diminuir as perdas de calor. Com base na leitura da tabela nutricional a seguir e da medida da temperatura da água, após a queima total do combustível, ela concluiu que 50% da energia disponível foi aproveitada. O calor específico da água é 1 cal g−1 °C−1, e sua temperatura inicial era de 20 °C.
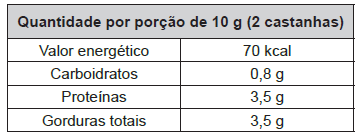
Qual foi a temperatura da água, em grau Celsius, medida ao final do experimento?
Glicólise é um processo que ocorre nas células, convertendo glicose em piruvato. Durante a prática de exercícios físicos que demandam grande quantidade de esforço, a glicose é completamente oxidada na presença de O2. Entretanto, em alguns casos, as células musculares podem sofrer um déficit de O2 e a glicose ser convertida em
duas moléculas de ácido lático. As equações termoquímicas para a combustão da glicose e do ácido lático são, respectivamente, mostradas a seguir:
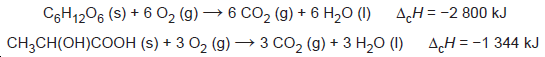
O processo anaeróbico é menos vantajoso energeticamente porque
O etanol é um combustível renovável obtido da cana-de-açúcar e é menos poluente do que os combustíveis fósseis, como a gasolina e o diesel. O etanol tem densidade ![]() massa molar
massa molar ![]() e calor de combustão aproximado de
e calor de combustão aproximado de ![]() Com o grande aumento da frota de veículos, tem sido incentivada a produção de carros bicombustíveis econômicos, que são capazes de render até
Com o grande aumento da frota de veículos, tem sido incentivada a produção de carros bicombustíveis econômicos, que são capazes de render até ![]() em rodovias, para diminuir a emissão de poluentes atmosféricos.
em rodovias, para diminuir a emissão de poluentes atmosféricos.
O valor correspondente à energia consumida para que o motorista de um carro econômico, movido a álcool, percorra 400 km na condição de máximo rendimento é mais próximo de
A respeito dos conceitos de equilíbrio químico, entalpia, entropia e energia livre, assinale a alternativa correta.
A gasolina, combustível largamente utilizado pela população mundial, é constituída majoritariamente de octano, um composto classificado como hidrocarboneto. Considerando que 1 mol de octano libera aproximadamente 5400 kJ, determine a massa de CO2 que será formada numa reação de combustão do octano que libera 323 kcal.
Dados das massas molares em g.mol-1 : C = 12 e O = 16.
O gás de cozinha é fundamentalmente composto pelos gases propano (C3H8) e butano (C4H10), a queima deste gás está sendo usada para aquecer 3,60 Kg de água. Qual a quantidade de calor (q) absorvida pela água sabendo-se que um mol do gás elevou a temperatura da água de 25ºC para 78,7ºC
Dados: calor específico da água (c) = 4,18 J/goC.
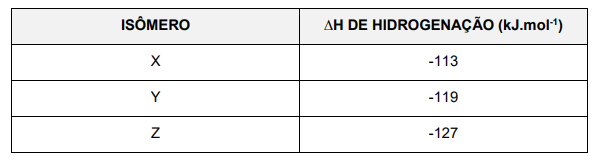
O metilbutano pode ser obtido a partir da hidrogenação catalítica, em fase gasosa, de alguns alcenos que são isômeros planos entre si. A tabela a seguir apresenta os isômeros de posição, denominados X, Y e Z, e seus respectivos valores hipotéticos de entalpia da reação de hidrogenação:
Sobre esses isômeros, é correto afirmar que
No que se refere à termoquímica, a reações exotérmicas e endotérmicas e à variação de entalpia, julgue o item a seguir.
A quantidade de calor que é absorvida ou liberada por um sistema durante uma variação independe de como a variação ocorre.
No que se refere à termoquímica, a reações exotérmicas e endotérmicas e à variação de entalpia, julgue o item a seguir.
Grande parte dos processos químicos é conduzida à pressão constante ou quase constante. Com isso, o calor absorvido em uma reação é igual à soma do aumento na energia do sistema com qualquer trabalho realizado sobre o sistema.
O monóxido de carbono (CO) é um gás extremamente tóxico. Ele interfere no processo respiratório dos vertebrados, pois se o CO estiver presente no ar, haverá no sangue uma “competição" entre o CO e o O2.
Infelizmente, grande parte da população convive diariamente com a presença desse gás, uma vez que ele é produzido em grandes quantidades