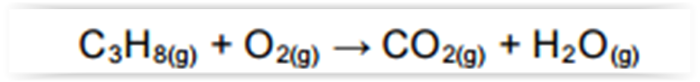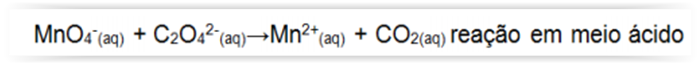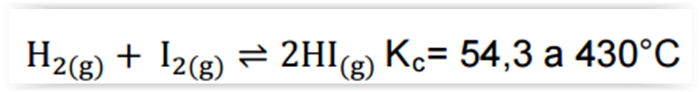Dois líquidos, X e Y, possuem massas específicas a 20°C de 500kg/m³ e 800kg/m³ , respectivamente. Em um tanque mantido à temperatura constante de 20°C, serão misturados 80m3 do líquido X com 40 toneladas do líquido Y, formando uma mistura líquida ideal Z. A massa específica da mistura Z, em kg/m³ , é aproximadamente:
Considerando-se a reação abaixo, assinalar a
alternativa CORRETA:
Assinalar a alternativa CORRETA:
Uma solução de ácido sulfúrico é preparada a partir de 9,8g de ácido sulfúrico, com pureza de 100%, acrescentando-se o ácido sobre a água destilada. Qual o volume de água, em litros, que deve ser adicionado à solução para que o pH final seja 2? (Dados: H = 1; S = 32; O = 16)
O hidróxido de magnésio (massa molar 58,33g/mol), conhecido como “leite de magnésia”, é frequentemente usado como antiácido para alívio de azia, má digestão e excesso de acidez no estômago. Considerando-se que uma colher (15mL) de leite de magnésia contenha 1.214mg de hidróxido de magnésio, qual a quantidade de matéria (mol) ingerida por um homem que administrou 5 doses (colheres) do medicamento ao longo do dia?
Considerando-se a reação de oxirredução a seguir, assinalar a alternativa CORRETA
Considerando-se a reação de formação a seguir, assinalar a alternativa CORRETA:
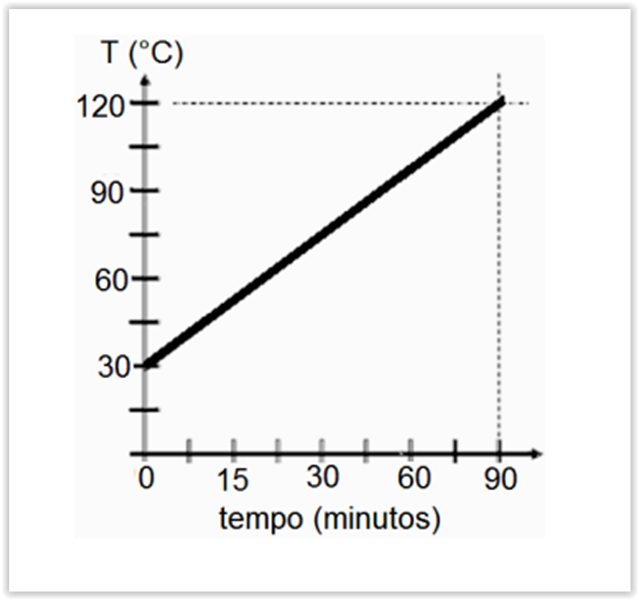
Três quartos de quilograma de uma substância desconhecida são aquecidos à taxa de 75 calorias por minuto, e a
variação de temperatura foi acompanhada conforme apresentado no gráfico abaixo. Com base nessas informações, o
calor específico da referida substância, em cal g-1 K-1
, é igual a:
O principal mineral nos ossos e nos dentes é a hidroxiapatita, Ca 5(PO4)3OH, que contém o íon Ca2+. No estado fundamental, o elemento cálcio, de símbolo Ca, tem número atômico 20. Dessa forma, considerando a posição na tabela periódica dos elementos, o cálcio encontra-se no
Com relação aos significados de mistura, molécula e substância, julgue os itens a seguir.
Mistura é um tipo de matéria que consiste em mais de uma substância. Seus componentes podem ser separados, fazendo-se uso das diferentes propriedades físicas das substâncias presentes.
Considerando os conceitos de átomo, estados da matéria e reações químicas, julgue os itens seguintes.
As reações químicas podem ser reversíveis ou irreversíveis; como exemplo de uma transformação reversível, tem-se a solubilização de comprimidos efervescentes em água com formação de bolhas.
Os humanos convivem com polímeros desde sempre,
pois as proteínas, o DNA e os polissacarídeos que existem em
nosso organismo são polímeros naturais. Foi no século XX que
um químico formulou a hipótese macromolecular, afirmando
que existem moléculas muito grandes, as macromoléculas. A
importância dos materiais poliméricos pode ser observada
olhando ao nosso redor e vendo a quantidade de objetos
feitos de plástico que nós utilizamos, sustentando uma
intensa atividade industrial e muitos empregos.
E. Wan, E. Galembeck e F. Galembeck. Polímeros sintéticos.
Cadernos Temáticos de Química Nova na Escola.
Edição especial, maio/2001 (com adaptações).
Considerando o texto, a química e sua importância social,
julgue os itens subsequentes.
A partir das contribuições da ciência, em especial da química, os polímeros sintéticos estão hoje presentes na vida diária porque permitem resolver um grande número de problemas na indústria, na agricultura e nos serviços.
Julgue os itens seguintes a respeito das funções orgânicas
mais comuns e suas propriedades químicas mais importantes.
Aldeído é um composto orgânico que contém um grupo - CHO. Como exemplo, tem-se o benzaldeído, de fórmula C6H5CHO.
Em relação às propriedades gerais dos sólidos no estudo de
soluções, julgue os itens subsequentes.
Sólido é uma forma rígida de matéria que mantém a mesma forma qualquer que seja a forma de seu recipiente. Um sólido molecular consiste em um conjunto de moléculas unidas por forças intermoleculares.
Acerca da termoquímica, da espontaneidade de reações e da
ação de catalisadores, julgue os itens a seguir.
Um processo é espontâneo se é acompanhado por uma diminuição na entropia total do sistema e das vizinhanças. Dessa forma, os processos espontâneos à temperatura e pressão constantes são acompanhados por um aumento da energia livre, ou seja, a direção da mudança espontânea é a direção do aumento da energia livre.