Avalie as afrmações que seguem com base no tema “metalurgia” atribuindo respectivamente V (verdadeiro) ou F (falso) e assinale a alternativa que apresenta a sequência correta de cima para baixo. ( ) Nitretação consiste no enriquecimento superfcial de nitrogênio de peças de baixo carbono. ( ) Nitretação consiste no enriquecimento superfcial de carbono de peças de baixo carbono. ( ) Revenido é um tratamento aplicado nos aços temperados, imediatamente após a têmpera.
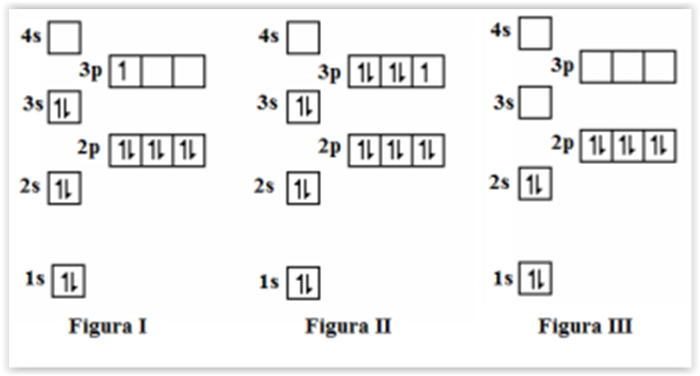
As figuras I, II e III, abaixo, representam as
configurações eletrônicas no estado fundamental de três
espécies químicas denominadas X, Y e Z,
respectivamente:
Com base na distribuição eletrônica apresentada,
assinalar a alternativa CORRETA:
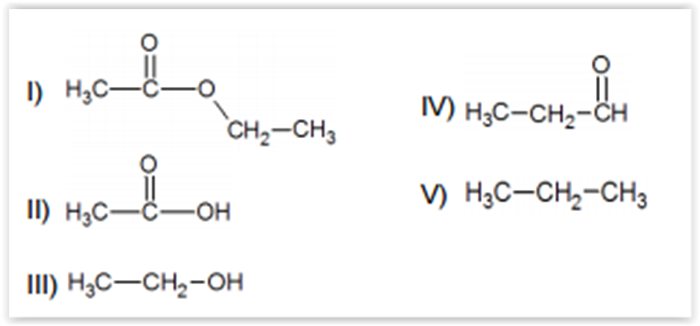
Considerando-se as estruturas abaixo, assinalar a
alternativa CORRETA:
A figura a seguir representa diluições de uma solução aquosa básica de Ca(OH)2 a partir da solução inicial A.
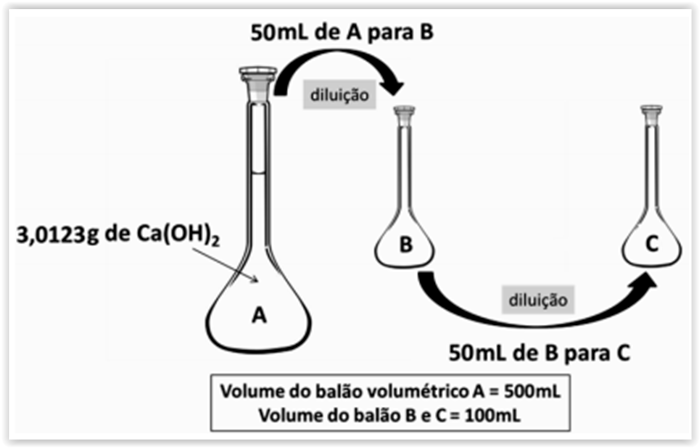
Entende-se que, após o preparo da solução A, coletou-se 50mL do frasco A para o frasco B, completando-o com água
destilada até que o menisco inferior do nível do líquido tangenciasse a linha de aferição do gargalo do balão. Após
homogeneização, coletou-se 50mL de B e passou-se para C, completando C com água destilada até a linha de aferição.
Diante do exposto, assinalar a alternativa CORRETA:
Dados: Ca = 40,078g/mol; O = 15,999g/mol; H = 1,008g/mol.
Com relação à segurança no laboratório, assinalar a alternativa CORRETA:
Com relação aos significados de mistura, molécula e substância, julgue os itens a seguir.
Molécula é a menor porção de um composto, com um
grupo variável de átomos ligados em um arranjo mutável
e eletricamente neutro.
Na época de chuvas vemos desastres que ocorrem em regiões do nosso país que muitas vezes impossibilitam a população de ter acesso à água potável. Qual das medidas apresentadas a seguir que a população dessas regiões precisa tomar para garantir o consumo de água potável e, assim, evitar maior contaminação?
Artefatos de aço inoxidável são resistentes à corrosão devido a um fenômeno conhecido como passivação, que é a
formação de uma fina camada de óxido de cromo na superfície, por ação do ar ou de oxidantes químicos. Sabendo-se que
o ácido nítrico (HNO3) na concentração de 1,6 mol/L pode ser usado como agente passivante, qual volume de HNO3
concentrado (em litros) deve ser utilizado para a obtenção de 100 L de solução passivante?
(Dados: MM(HNO3) = 63,0 g/mol; HNO3 concentrado: d = 1,40 g/mL; teor máximo = 65%(m/m))
Na determinação de cálcio em águas naturais, a AOAC (Ass°CIation of OfficIal Analytical Chemists/USA) recomenda um
método gravimétrico que consiste em adicionar excesso de ácido oxálico (C2H2O4) a um volume conhecido de amostra e,
em seguida, adicionar a quantidade necessárIa de NH4OH. O precipitado obtido é filtrado, seco, calcinado e pesado, e a
massa de CaO obtida é utilizada para calcular a quantidade de Ca na amostra que, segundo a norma da AOAC, deve ser
expressa como teor de carbonato de cálcio. O método citado é ilustrado pelas equações a seguir. Na análise de uma
amostra de 100,00 mL de água, a massa de CaO obtida foi de 0,2800 g.
Ca+2(aq.) + C2O4-2(aq.) → CaC2O4(s)CaC2O4(s) → CaO(s) + CO + CO2
Dados: Massas molares aproximadas: MM(C2H2O4.2H2O) = 126 g/mol; MM(CaO) = 56 g/mol; MM(CO2) = 44 g/mol, MM(CaCO3) = 100 g/mol;
densidade (H2O) = 1,0 kg/L.
De acordo com os dados apresentados, qual é a concentração de cálcio na amostra de água analisada, expressa em ppm
de CaCO3?
O ácido fosfórico (H3PO4) de alta pureza é obtido por vIa seca ou térmica, pela combustão do fósforo elementar e posterior
hidratação do P2O5, de acordo com as reações abaixo:
Nesse pr°Cesso, de acordo com as equações acima, assinale a alternativa que apresenta a quantidade de calor liberado
na formação do H3PO4 (em kcal/mol).
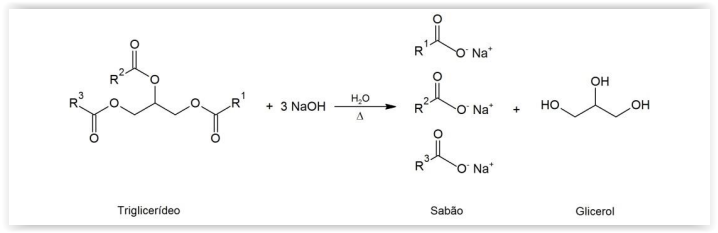
Sabões são sais de sódio ou potássio de ácidos graxos, obtidos pela reação de gorduras e óleos (triglicerídeos) com
NaOH, KOH ou Na2CO3. A reação de saponificação é representada a seguir:
em que R1, R2 e R3 são cadeIas lineares saturadas ou insaturadas, geralmente com doze ou mais átomos de carbono.
Com base nessas informações, considere as seguintes afirmativas:
1- Uma solução aquosa de sabão puro apresenta pH < 7
2- Adição de ácido forte a uma solução de sabão acarreta precipitação de ácidos graxos.
3- Ca(OH)2 não pode ser usado na obtenção de sabão, pois sais de cálcio de ácidos graxos são insolúveis em água.
4- A obtenção de sabão com Na2CO3 segue a mesma estequiometrIa que no uso do NaOH.
Assinale a alternativa correta.
Vários medicamentos atuam como inibidores enzimáticos.
A lovastatina é um deles. Ela se liga de forma não
covalente no sítio ativo da enzima 3-hidroxi 3-
metilglutaril-coenzimaA (HMG-CoA) redutase, que é a
responsável pela etapa inicial da síntese de colesterol. Por
isso, é considerado um agente redutor do colesterol no
organismo. Essas características evidenciam que a
lovastatina é um inibidor enzimático do tipo
São exemplos de substância inflamável e explosiva, respectivamente:
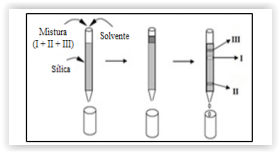
O esquema a seguir mostra a separação cromatográfica das
substâncias I, II e III, utilizando sílica (Si02) como fase
estacionária. Cada faixa representa uma substância.
A mistura analisada é composta de substâncias, com pesos
moleculares equivalentes, das classes: álcool, amina e
hidrocarboneto. Com base nestas informações, as
substâncias I, II e III representam, respectivamente,
compostos das classes:
A análise elementar de um composto orgânico resultou em 48,63% de carbono, 43,19% de oxigênio e 8,18% de H. Sabendo-se que o peso molecular desse composto é 222,3 g mol-1, sua fórmula molecular é: