O metano é um dos subprodutos dos aterros sanitários, produzido pela decomposição anaeróbica de resíduos orgânicos. Os produtos de sua combustão são C02 e H2O. Quantos mols de vapor de água podem ser produzidos por 4,0 g de metano?
Em um experimento, para determinar a massa atômica de um elemento, foi constatado que a massa determinada era 140 vezes mais pesada do que um átomo de hidrogênio. Sabendo que o número de prótons é igual a 59, determine o número de átomos em um 1 kg de amostra desse elemento:Considere que a massa do próton é igual à massa do nêutron e vale 1,7 x 10-27 kg.
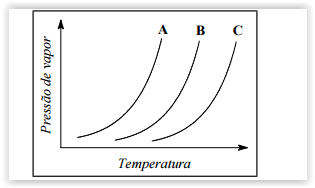
Em uma aula experimental de química, três soluções foram
submetidas à destilação. O gráfico a seguir representa o
comportamento dessas soluções.
Este gráfico evidencia o ponto de ebulição
O processo de oxidação de minérios é comumente empregado
para reduzir seu teor de carbono. Desse modo, qual é a massa
de oxigênio, em kg, necessária para reduzir o teor de carbono
de 5% para 2% em 50 toneladas de minério?
Considere que apenas o dióxido
de carbono é produzido
Um cátion trivalente é apresentado na alternativa:
Uma reação de simples troca é apresentada na alternativa:
Uma solução de AgNO 3 com concentração de 16,98 g.L-1 (m/v) corresponde em Molaridade (Mol.L-1 ) à concentração de:
Dados: Massa molecular da AgNO 3 =169,8 g.Mol-1
O isótopo 6C14, conhecido como "carbono 14", é radioativo e empregado em datações arqueológicas e estratigráficas. O carbono 14 apresenta decaimento do tipo β. O isótopo 6C14 ao emitir uma partícula (-1β0) dá origem ao isótopo:
Átomos ou íons que apresentam o mesmo número de elétrons são denominados espécies isoeletrônicas. Nas espécies isoeletrônicas F-, Na+ , Mg2+ e Al3+, o íon
Considere quatro elementos químicos genéricos, representados por A, B, C e Z. Os elementos A e Z pertencem ao mesmo grupo da tabela periódica; os elementos A, B e C apresentam números atômicos consecutivos; e B é um gás nobre. Dessa forma,
A dureza da água está relacionada à presença de íons metálicos (M 2+) dissolvidos em determinado volume de amostra. Nesse contexto, para determinar a dureza da água, um volume de 50 mL foi titulado com uma solução 0,01 mol L-1 de EDTA, gastando-se um volume médio de 7 mL dessa solução. A equação química geral representativa do processo está descrita a seguir.
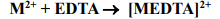
A dureza da água, expressa em mg de CaCO3 por litro de amostra, é igual a
Um haleto de alquila terciário deve ser submetido às condições reacionais que favoreçam reações de substituição nucleofílica SN1.
Esse tipo de reação é favorecida por
O grafeno é um alótropo do carbono e apresenta propriedades elétricas atrativas para o desenvolvimento de sensores. Nesse material, a hibridização dos átomos de carbono é:
concentração de ácido lático (HX) presente em uma amostra foi determinada por análise volumétrica. No experimento, 1,0 mL da amostra foi transferido para um balão de 100 mL. Em seguida, 10 mL dessa solução foram transferidos para um erlenmeyer e titulados com NaOH 0,050 mol L-1. Considerando a proporção estequiométrica igual a 1:1 e que o volume gasto da solução de NaOH foi igual a 5,0 mL, a concentração de HX, em mol L-1, na amostra foi igual a
Com relação aos métodos de separação de misturas, julgue o
próximo item.
Os métodos de separação de misturas podem ser processos mecânicos ou físicos. Dissolução fracionada, destilação e evaporação são exemplos de processos mecânicos, enquanto catação, filtração e sedimentação são exemplos de processos físicos.