A estrutura geral de duas moléculas de polipropileno está representada na figura a seguir.
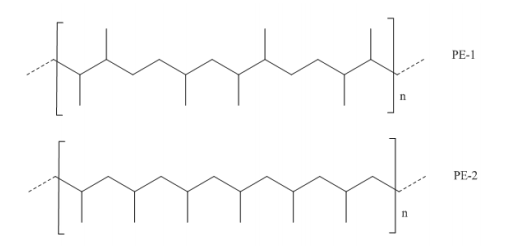
Sobre estas estruturas, assinale a afirmativa correta.
O carvão mineral é responsável por cerca de 8% de todo o consumo mundial de energia e de 39% de toda a energia elétrica gerada e, apesar dos graves impactos sobre o meio ambiente, o carvão continuará sendo, por muitas décadas, o principal insumo para a geração de energia elétrica, especialmente nos países em desenvolvimento.
A geração de energia a partir do carvão pode ser obtida através de um processo chamado de gaseificação de carão, onde o carvão reage com oxigênio molecular e água, sendo transformado em gás de síntese (CO+H2), que é queimado em seguida.
As equações químicas relativas ao processo de gaseificação do carvão estão representadas a seguir (considera−se o carvão mineral como carbono puro).

Com base nas informações fornecidas, a variação de entalpia, em kJ/mol do processo global é:
A combustão é uma reação entre uma substância (combustível)
e o oxigênio (O2) (comburente), com liberação de energia
levando à formação de gás carbônico e água. A falta de
oxigênio durante a combustão pode levar à formação de um
produto indesejável como a fuligem (C), que não tem oxigênio
na sua constituição.
A quantidade de calor liberada é menor nos casos de
combustão incompleta. Portanto, além de gerar compostos
nocivos à saúde humana, a combustão incompleta apresenta
uma grande desvantagem econômica, pois com a mesma
quantidade de combustível haverá menor quantidade de
energia gerada.
O calor liberado na combustão completa de metano é de
802 kJ.mol–1 e, nas mesmas condições de temperatura, o calor
liberado na queima incompleta desse composto, produzindo
fuligem é de 408,5 kJ.mol–1.
(Combustão e Energia disponível em
http://www.usp.br/qambiental/combustao_energia.html; Acesso 01/10/2013)
A massa de metano, queimada de maneira incompleta
produzindo fuligem, necessária para produzir a mesma
quantidade de calor que a queima completa de 8 kg de metano é
Dados: Massa molar do H=1 g.mol–1 C = 12g.mol–1
Umteoremmassa de 1,0 ppm equivale a:
Qual é a massa (expressa em gramas) de uma amostra de um solvente líquido e puro, com volume de 3 mL e cuja densidade absoluta é de aproximadamente 0,78 g/mL?
A figura a seguir representa uma curva de energia potencial (Ep) versus distância internuclear de dois átomos. O conhecimento dessa curva permite avaliar a energia de ligação de uma molécula diatômica.
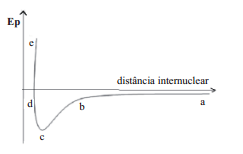
O ponto da curva relacionado com o comprimento da ligação química está representado pela letra:
A asparagina é um aminoácido que participa da biossíntese de glicoproteínas e que pode atuar no sistema nervoso central.
Essa substância pode ser representada como:
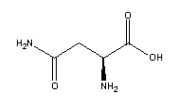
Uma propriedade física que pode ser utilizada para diferenciar os isômeros espaciais dessa substância é:
Uma empresa de bebidas anunciou o recall de 96 embalagens de um suco de maçã que foram envasadas com solução de hidróxido de sódio a 2,5% em massa (densidade aproximadade 1,0 g/cm3 ). A empresa informou que o conteúdo pode representar risco de queimadura ou sensação de forte ardência na boca, caso venha a ser ingerido. De acordo com essas informações, o pH da solução que foi envasada no lugar do suco equivale, aproximadamente, a:

O Departamento de Energia dos EUA produziu seu primeiro lote de plutônio usado para alimentar sondas espaciais, sem fins armamentistas, desde que desligou seu reator nuclear, há 25 anos, segundo informaram funcionários da NASA.
(Disponível em: http://oglobo.globo.com/ciencia/eua-voltam-produzir-plutonio-paraalimentar-sondas-espaciais-7881294. Acesso em março de 2013.)
Este radionuclídeo pode ser sintetizado pelo bombardeio de núcleos de urânio-238 com deutério, produzindo netúnio-238. O netúnio-238 sofre um decaimento produzindo o plutônio-238, esse decaimento ocorre com a emissão de partícula:
Certamente ocorrerá com diminuição de energia livre de Gibbs, ΔG, e portanto será espontânea em determinada temperatura T, uma transformação química que apresente]
O gás natural é utilizado mundialmente e, neste sentido, o Brasil segue essa tendência de aproveitamento de combustíveis mais limpos. Sua utilização é vantajosa, principalmente em razão de
O uso crescente de fibras ópticas para a construção de redes de
telecomunicações em banda larga levou a avanços consideráveis
na tecnologia da fabricação de vidros (...). Os vidros têm estrutura
em rede baseada em um óxido de ametal, normalmente a sílica
(SiO2), fundida juntamente com óxidos de metais que agem como
“modificadores de rede" e alteram o arranjo das ligações do
sólido (...). O vidro resiste ao ataque da maior parte dos
reagentes. Entretanto, a sílica do vidro reage com ácido
fluorídrico para formar íons fluoro‐silicatos:

Na reação apresentada
Os óxidos de nitrogênio são os componentes principais das
névoas, um fenômeno ao qual os habitantes das grandes cidades
estão habituados. O óxido nítrico forma‐se em pequenas
quantidades nos cilindros de combustão interna dos motores
pela combinação direta de nitrogênio e oxigênio:
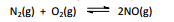
A constante de equilíbrio para essa reação aumenta de
aproximadamente 10–15 a 300K para cerca de 0,05 a 2400 K
(temperatura aproximada no cilindro de um motor em
funcionamento).
Com relação à reação entre o gás nitrogênio e o gás oxigênio,
assinale a afirmativa correta.
A água contendo uma concentração relativamente alta de íons Ca2+, Mg2+ e outros cátions divalentes é chamada de água dura. Em alguns lugares é necessário que se realize o abrandamento da água para evitar depósitos indesejáveis de sais insolúveis em sistemas de água quente. O abrandamento da água pode ser realizado por troca iônica. Este método consiste em fazer a água dura passar por um leito de resina de troca iônica que pode ser constituída por pérolas de plástico com grupos aniônicos do tipo fosfato. Essa resina captura os íons Ca2+ e Mg2+, substituindo‐os por íons que formarão compostos solúveis. O fosfato utilizado nesse tipo de resina tem como cátion
Alumínio metálico pode ser produzido eletroliticamente pelo processo Hall-Heroult em que o A603 é dissolvido em criolita fundida, Na3AiF6.
Nesse processo o Ion alumínio é reduzido a alumínio metálico e o ion 02 é oxidado a 02, que reage com os anodos de carbono gerando CO2.
A massa de aluminio obtida nessa eletrolise por uma corrente de 8,0A durante 3 horas e 20 minutos e rendimento de 100%, é de:
Dados: Massa molar (g.mor-1): Ai= 27 1F = 96500C

