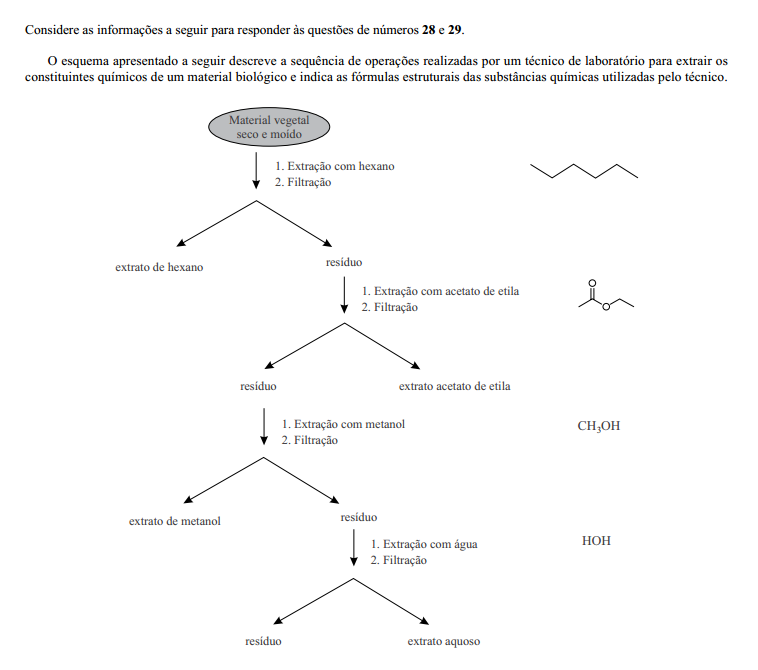
Observe a estrutura a seguir, que representa o composto antibiótico conhecido como isopenicilina N, cuja estrutura química possui diversas funções orgânicas.
Assinale a alternativa que NÃO contém uma função orgânica representada na estrutura isopenicilina N.
Sobre as ligações químicas, analise as afirmativas.
I. A característica principal das ligações iônicas é a grande diferença de eletronegatividade entre os átomos. Um átomo deve ter baixa energia de ionização e o outro uma elevada afinidade eletrônica.
II. A atração eletrostática entre os íons na ligação iônica é a força mais significativa da estabilização da ligação.
III. A baixa energia de ionização necessária para uma ligação iônica é característica dos metais. A alta energia de afinidade eletrônica, que também é necessária para uma ligação iônica, é uma característica dos elementos químicos não metálicos, que necessitam de um, dois ou três elétrons para completar suas camadas de valência.
Está(ão) correta(s) a(s) afirmativa(s)
Um método clássico da química analítica de medir o teor de água oxigenada é a reação da água oxigenada com íon permanganato, que é reduzido a Mn+2, em meio ácido, de acordo com a equação a seguir (não balanceada).
KMnO4(aq) + H2O2(aq) + H+ (aq) → Mn2+ (aq) + H2O(l) + O2(g)
Um analista recebeu em um Erlenmeyer um volume de 10 mL de uma amostra de água oxigenada e acrescentou 100 mL de água destilada. A análise foi feita utilizando 15,3 mL de uma solução padrão de permanganato de potássio padrão 0,1103 mol/L. (Considere as seguintes massas moleculares (g/mol): Mn = 55; H = 1; O = 16; K = 39.)
O teor de H2O2 na amostra anterior, expresso em g% (m/V), e o de mol/L são, respectivamente,
A reatividade química dos metais está relacionada às propriedades periódicas e à configuração eletrônica dos elementos. Com relação à reatividade dos metais, é INCORRETO afirmar que
Numere a COLUNA II de acordo com a COLUNA I, fazendo a relação entre a geometria
molecular e a espécie.

Assinale a alternativa que apresenta a sequência CORRETA.
A Cromatografia Líquida de Alta Eficiência (CLAE) é o tipo mais versátil e mais amplamente empregado de cromatografia por eluição. Essa técnica é utilizada pelos químicos para separar e determinar espécies em uma grande variedade de materiais orgânicos, inorgânicos e biológicos. Analise as seguintes afirmações a respeito da técnica analítica de CLAE. I. O tipo de CLAE é definido pelo mecanismo de separação ou pelo tipo de fase estacionária. II. Os detectores em CLAE devem apresentar um volume pequeno, de forma que minimize o alargamento de banda extracoluna. III. O tipo de CLAE mais utilizado é a cromatografia por troca iônica, na qual a fase estacionária é um segundo líquido que é imiscível com o líquido da fase móvel. A partir dessa análise, pode–se concluir que estão CORRETAS.
A classificação primária dos reatores químicos pode ser feita com base na forma de energia usada na realização da reação.
Sendo assim, correlacione os tipos de reatores com o tipo de energia usada na reação.

No Brasil, o biodiesel é vendido, regularmente, misturado ao diesel de petróleo em postos de abastecimento espalhados pelo país. A mistura classificada como B2, autorizada para uso automotivo, apresenta:
Em relação à logística dos biocombustíveis no Brasil, é correto afirmar que:
De um modo geral, no laboratório, os reagentes não são misturados na exata proporção exigida pelas reações químicas. Ao
contrário, é comum o excesso de um dos reagentes, geralmente o mais barato. Considerando que o iodeto de alumínio é
formado pelo aquecimento de alumínio em presença de iodo, representamos esta reação através da equação:
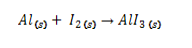
Com base nessas informações, partindo-se de 1,40 moles de Al e 3,00 moles de I2, o reagente limitante e o rendimento
teórico do produto serão respectivamente:
Uma solução tampão de qualquer pH desejado pode ser preparada pela combinação de quantidades calculadas de um par
ácido-base conjugado adequado. Na prática, porém, os valores de pH de tampões preparados em laboratório utilizando
quantidades teóricas diferem dos valores previstos, por conta de incertezas nos valores numéricos de muitas constantes de
dissociação e das simplificações utilizadas nos cálculos. Em virtude disso, é comum se prepararam tampões gerando uma
solução cujo pH seja aproximadamente aquele desejado, e então o ajustam pela adição de um ácido forte ou base forte até
que o pH requerido seja indicado por um pH-metro. Assim, para preparar 500 mL de uma solução tampão com pH= 5,00 a
partir do ácido acético (HOA
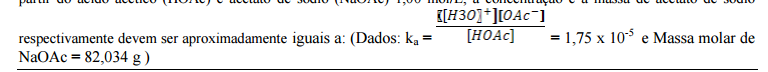
O efeito estufa é um fenômeno natural e possibilita a vida humana na Terra. Quando existe um balanço entre a energia solar incidente e a energia refletida na forma de calor pela superfície terrestre, o clima se mantém praticamente inalterado. Entretanto, o balanço de energia pode ser alterado devido às mudanças na concentração de gases de efeito estufa na atmosfera, decorrente da poluição. Dentre os principais gases de efeito estufa regulados pelo Protocolo de Quioto, aquele que é utilizado como referência para classificar o poder de aquecimento global dos demais gases de efeito estufa é o:
Dois métodos básicos são empregados para estabelecer a concentração de soluções padrão: o método direto (utiliza padrão primário) e o método da padronização (utiliza solução padrão secundário). A concentração de uma solução padrão secundário está sujeita a incertezas maiores que a da solução padrão primário. Então, se houver escolha, as soluções serão mais bem preparadas por meio do método direto. Supondo que se queira preparar 2,00 L de AgNO3 com concentração de 0,05 mol/L a partir de um sólido com grau padrão primário, a quantidade de AgNO3 a ser dissolvida será (Dados: Massa molar de AgNO3 = 169,87 g/mol)
Considerando a massa molar do NaCl igual a 58,5 g/mol e sabendo que um organismo adulto contém em média 250 g de NaCl e que nele circulam 42 litros de água, a concentração de NaCl, em mol/L, no corpo de um adulto corresponde aproximadamente a
Sabendo que o material vegetal contém óleos, açúcares, polissacarídeos, vitamina C e sais minerais, afirma-se que o extrato em hexano e o resíduo após extração com água devem conter, respectivamente,