Rafaela foi designada, de acordo com os preceitos legais, como fiscal de determinado contrato de execução de obras e serviços de engenharia em unidade operacional da PETROBRAS.
Com referência a essa situação hipotética, julgue os próximos itens de acordo com o RLCP.
Rafaela deverá, sempre, manter o registro de reclamações, irregularidades, falhas e outras ocorrências que sejam consideradas relevantes pela fiscalização, na execução das atividades contratadas.
Assinale a opção correta em relação aos sistemas de informações gerenciais e à utilização estratégica de recursos de tecnologia da informação que pode levar à obtenção de vantagem competitiva.
Acerca dos critérios necessários para a nomeação de diretor-geral em empresa estatal, julgue os itens a seguir, com base na Lei n.º 13.303/2016, que dispõe sobre o estatuto jurídico da empresa pública e da sociedade de economia mista.
I A pessoa indicada para ocupar o cargo de diretor-geral de empresa estatal deve ter formação acadêmica compatível com o cargo.
II A avaliação de competências dos nomeados ao referido cargo deve ser feita pelo Senado Federal.
III Os indicados ao referido cargo deverão ter ocupado, previamente, pelo menos, um cargo de direção ou chefia
superior, em empresa de porte ou objeto social semelhante ao da empresa estatal, por, no mínimo, um ano.
Assinale a opção correta.
A respeito do projeto e da montagem de bombas centrífugas, julgue os itens que se seguem.
Na montagem de bombas centrífugas, o acoplamento bomba-motor requer cuidado especial com o alinhamento correto entre o motor e a bomba, para evitar vibrações excessivas e danos aos componentes.
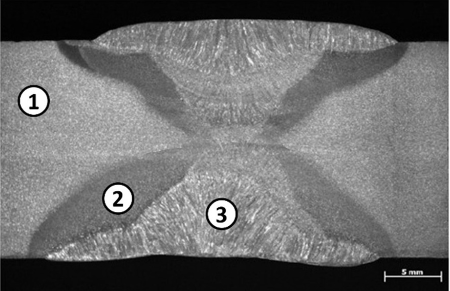
Internet: <abmproceedings.com.br> (com adaptações)
A respeito da soldagem com eletrodo revestido, considerando a figura precedente, que mostra três seções de uma junta soldada
por esse tipo de soldagem, julgue os itens a seguir.
Na soldagem por arco elétrico com eletrodo revestido, o revestimento do eletrodo tem a função de proteger o metal fundido da atmosfera e fornecer elementos de ligas adicionais para melhorar as propriedades da junta soldada.
2 H2O ⇌ 2 H2 + O2
Considerando a reação de eletrólise da água mostrada acima, e sabendo que ZH = 1, ZO = 8, ZP = 15, MH = 1,0 g/mol, MO = 16,0 g/mol e que R = 0,082 atm ∙ L ∙ K−1 ∙ mol−1 é a constante universal dos gases perfeitos, julgue os itens que se seguem.
A reação de eletrólise da água é incompatível com o modelo atômico de Dalton, segundo o qual, em uma reação química, os átomos são alterados, pois as propriedades das substâncias são alteradas.
O petróleo é constituído por uma mistura de compostos químicos orgânicos (hidrocarbonetos), cujo estado físico, em condições normais de temperatura e pressão (CNTP), é predominantemente líquido, podendo assumir o estado gasoso quando a mistura contiver uma maior porcentagem de componentes com baixa massa molecular. O petróleo geralmente se apresenta associado à água, que, por sua vez, contém sais minerais em solução. Essa associação é devida, sobretudo, à tendência natural de acúmulo de água salgada gerada pelas formações geológicas nas partes inferiores de reservatórios de petróleo. Apesar de o tratamento que o óleo sofre nos campos de produção reduzir consideravelmente os teores de água, sais e sedimentos, os requisitos de altas vazões de óleo produzido impedem a remoção total da água salgada do petróleo. As águas de formação são compostas de vários tipos de sais; porém, costuma-se relacionar a salinidade global dessas águas em base de cloreto de sódio. Os sais contidos no petróleo constituem uma fonte de corrosão por gerarem ácido clorídrico (HCl) nas condições correntes nos equipamentos de destilação.
Internet: (com adaptações).
A partir das informações do texto precedente, julgue os próximos itens.
Sais muito solúveis são aqueles que apresentam valores elevados da constante do produto de solubilidade (Kps) em uma dada temperatura.
Na gasolina brasileira, um componente presente que merece destaque especial é o etanol. O Decreto n.º 10.940/2022 estabelece que a gasolina do tipo C deve conter 27% de etanol. O principal papel desse componente é atuar como antidetonante. Um ensaio simples para verificar o teor de etanol na gasolina comercial consiste em transferir 50 mL da amostra a ser avaliada para uma proveta de 100 mL, completando-se o volume com água destilada. Após agitação e repouso, a mistura contendo gasolina, etanol e água sofrerá separação.
Tendo como referência o ensaio acima descrito e considerando os usos da gasolina, julgue os itens que se seguem.
Uma das formas mais promissoras para a produção de combustíveis líquidos é a pirólise, também conhecida como craqueamento; ela pode acontecer na presença ou na ausência de catalisadores, que são responsáveis por alterar a cinética e o equilíbrio das reações químicas.
O gás natural veicular (GNV) contido em um tanque de armazenamento ocupa um volume gasoso de 15 m3 e está submetido à pressão de 20 MPa às 6 h, quando a temperatura ambiente, em equilíbrio térmico com o gás, é de 10 °C.
Com relação a essa situação hipotética, julgue os itens seguintes, considerando que todos os gases se comportem idealmente,
que não haja processo de liquefação ou vaporização e que 0 K = −273 °C.
Se o referido GNV for totalmente transferido para outro botijão à mesma temperatura e, nesse novo botijão, a pressão final dos gases for de 30 MPa, então o volume gasoso desse novo botijão será de 10 m3.
Com referência a funções orgânicas, julgue os itens que se seguem.
O grupo dos hidrocarbonetos inclui o subgrupo dos ciclanos, cuja fórmula geral é CnH2n+2.
Uma das causas do aquecimento global é o aumento da concentração de gás carbônico (CO2) na atmosfera, pois esse gás
é um dos que provoca o chamado efeito estufa. As emissões de CO2 são oriundas principalmente da queima de combustíveis
fósseis e de processos industriais. Uma das formas de se reduzir essa emissão consiste em passar a fumaça gerada por plantas
industriais através de uma suspensão aquosa de CaSiO3, onde ocorre a seguinte reação química.
2 CO2 (g) + H2O (l) + CaSiO3 (s) → SiO2 (s) + Ca(HCO3)2 (s)
Com base nessa reação química, julgue os próximos itens.
Participam da reação três óxidos e dois sais.
Na gasolina brasileira, um componente presente que merece destaque especial é o etanol. O Decreto n.º 10.940/2022 estabelece que a gasolina do tipo C deve conter 27% de etanol. O principal papel desse componente é atuar como antidetonante. Um ensaio simples para verificar o teor de etanol na gasolina comercial consiste em transferir 50 mL da amostra a ser avaliada para uma proveta de 100 mL, completando-se o volume com água destilada. Após agitação e repouso, a mistura contendo gasolina, etanol e água sofrerá separação.
Tendo como referência o ensaio acima descrito e considerando os usos da gasolina, julgue os itens que se seguem.
No ensaio em questão, o álcool contido na gasolina comercial será transferido para a fase aquosa em decorrênci da semelhança entre suas forças intermoleculares e as da água, tornando-se o soluto da nova solução aquosa.
Julgue os itens subsequentes, relativos a reações orgânicas e a aspectos pertinentes a isomeria.
As reações de polimerização em cadeia apresentam as seguintes etapas: iniciação, propagação e término.
A equação y = mx + b, com m = 2,09 e b = 0,257, foi obtida na calibração de um método para a determinação cromatográfica de isoctano em misturas de hidrocarbonetos. Nessa equação, o eixo x apresenta valores de concentração de isoctano, em porcentagem molar, e o eixo y, a área sob o pico cromatográfico, em uma unidade arbitrária.
Tendo como referência as informações precedentes, julgue os itens subsecutivos, a respeito de fundamentos de estatística.
No método dos mínimos quadrados, os valores calculados de xi, yi, xi2, yi2, xiyi e seus respectivos somatórios devem ser
arredondados para três algarismos significativos antes de se calcular os demais parâmetros da regressão linear.
Julgue os próximos itens, a respeito da equação de Nernst e de potencial de eletrodo, eletrodos indicadores e medidas de pH.
A equação de Nernst tem por finalidade prever o potencial de uma pilha durante o seu funcionamento, correlacionando a variação do potencial da pilha em certo instante da reação com a variação das concentrações de produtos e reagentes.

