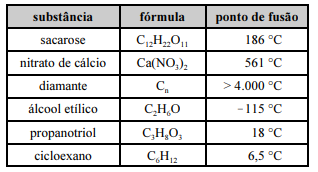
Considerando os dados da tabela precedente, assim como as características e as propriedades das substâncias nela apresentadas, julgue o item a seguir.
Dado que viscosidade é a resistência que um líquido apresenta para fluir, o propanotriol é mais viscoso que o álcool etílico.
A equação a seguir sintetiza a reação de combustão entre o salitre, o enxofre e o carvão, substâncias presentes na pólvora.
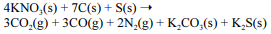
Acerca desse assunto, julgue o próximo item.
A massa molar do composto formado pelo ânion do carbonato de potássio e o cátion do nitrato de alumínio é maior que 250,0 g/mol.

Considere as reações I, II e III a seguir.
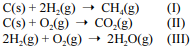
Com relação a essas informações, julgue o item que se segue.
A substituição de 1, 2 ou 3 átomos de hidrogênio por átomos de cloro na molécula de metano tornaria polares todos os compostos formados, contudo, caso os 4 átomos de hidrogênio na molécula de metano fossem substituídos por átomos de cloro, a molécula formada seria mantida apolar, como o próprio metano.
As interações intramoleculares e intermoleculares são as responsáveis pelas várias fases (estados) da matéria e pelas propriedades físico-químicas dos materiais, além de necessárias para a determinação de estruturas de moléculas biologicamente importantes. Acerca das ligações químicas nos materiais, julgue o próximo item.
A energia de ligação entre os átomos de flúor em uma molécula de F2 é maior que a energia de ligação entre os átomos de nitrogênio em uma molécula de N2.
As interações intramoleculares e intermoleculares são as responsáveis pelas várias fases (estados) da matéria e pelas propriedades físico-químicas dos materiais, além de necessárias para a determinação de estruturas de moléculas biologicamente importantes. Acerca das ligações químicas nos materiais, julgue o próximo item.
O ponto de ebulição do etanal (CH3CHO) é maior que o ponto de ebulição do éter dimetílico (CH3OCH3).
A precipitação de cátions metálicos pela adição de um ânion com o qual eles formem composto insolúvel é uma ferramenta bastante utilizada para a remoção, identificação e(ou) quantificação de um metal em solução. Por exemplo, a adição de uma solução de H 2S é empregada para promover a precipitação de sulfetos metálicos pouco solúveis.
Considerando que as constantes de ionização ácida do H
2S (Ka1 e Ka2) sejam iguais a 1,0 × 10-7 e 1,0 × 10-13, que o produto de solubilidade (Kps) do CdS seja igual a 1,0 × 10-27 e que todas as soluções envolvidas apresentem comportamento ideal, julgue o item a seguir.
Em uma solução aquosa de H 2S, a ordem decrescente de concentração das espécies presentes é [H2O] > [H3O+] > [H2S] > [S2-] > [HS-].
A solubilidade dos sulfetos depende fortemente do pH do meio. Por esse motivo, muitas vezes a precipitação desses compostos é realizada em meio tamponado. Considerando que pOH = -log [OH -] e pKb = -log Kb, julgue o seguinte item.
A solubilidade de um sulfeto metálico é tanto menor quanto maior for a acidez do meio.
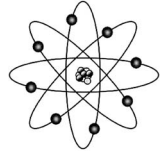
A tabela periódica e o modelo atômico evoluíram gradualmente ao longo do tempo, até as versões atuais. A figura precedente mostra uma ilustração bastante utilizada na representação de um átomo e que se baseia no modelo atômico de Bohr. Com relação à tabela periódica, aos modelos atômicos e aspectos a eles relacionados, julgue o próximo item.
A proposta de existência de órbitas com trajetórias bem definidas para os elétrons de um átomo, conforme ilustrado na figura, mostrou-se, mais tarde, ser um equívoco, visto que os elétrons apresentam propriedades de ondas e, portanto, não podem ser descritos como partículas com trajetórias bem definidas.
Os alquenos são matéria-prima de grande importância na indústria porque podem ser facilmente transformados em uma vasta gama de compostos químicos. Exemplos típicos são as reações de hidratação e de polimerização catalisadas por ácido. Com relação às reações de alquenos, julgue o item subsequente.
Se a reação de desidratação de um alqueno ocorre de acordo com uma cinética de pseudoprimeira ordem, então o gráfico da concentração do alqueno em função do tempo terá aspecto conforme indicado no gráfico a seguir.

Considerando o texto precedente e os múltiplos aspectos a ele relacionados, julgue o item seguinte, a respeito de competências e habilidades propostas pelos Parâmetros Curriculares Nacionais de Ensino Médio (PCNEM) para a disciplina de química.
Em decorrência da aridez e da especificidade dos conteúdos da química, a contextualização e a interdisciplinaridade constituem eixos secundários na organização das dinâmicas interativas no ensino de química.

Considerando o texto precedente e os múltiplos aspectos a ele relacionados, julgue o item seguinte, a respeito de competências e habilidades propostas pelos Parâmetros Curriculares Nacionais de Ensino Médio (PCNEM) para a disciplina de química.
As atividades práticas não devem ser meras repetições dos procedimentos experimentais, mas sim possuir caráter investigativo, para que o aluno possa compreender a relação teórico-conceitual da situação real.
Com relação aos materiais utilizados nos laboratórios de ensino de química e às normas de segurança laboratoriais, julgue o item subsequente.
O símbolo a seguir, muito comum em frascos de vidro nos laboratórios, indica que o conteúdo do frasco é constituído de substância que apresenta risco biológico.

Considerando o texto precedente, julgue o item subsecutivo, acerca do uso de recursos e habilidades didáticos no ensino de química.
Os jogos de química são atividades lúdicas que podem auxiliar na construção de determinado conteúdo de química.

Considerando os dados da tabela precedente, assim como as características e as propriedades das substâncias nela apresentadas, julgue o item a seguir.
O nitrato de cálcio é um exemplo de sólido iônico, formado por íons, mas que apresenta ligações covalentes na sua estrutura.

Considerando essas informações e os diversos aspectos a elas relacionados, julgue o item que se segue.
Algumas vidrarias, técnicas experimentais e diversas substâncias até hoje utilizadas são originárias da alquimia.



