A extração líquido-líquido é um método de separação dos componentes de uma mistura líquida, bastante empregado em laboratório de química. A respeito desse método, assinale a alternativa correta.
Na produção de aço é comum reduzir-se o óxido de ferro (III) (Fe2O3) pela adição do elemento carbono (C), na presença de oxigênio e sob condições apropriadas, em uma reação que leva à produção do elemento ferro (Fe) e dióxido de carbono (CO2). Supondo que 0,5 mols de Fe2O3 e 0,3 mols de C são misturados na presença do oxigênio e reagem, assinale a alternativa que apresenta a substância que está em excesso na reação e a massa em excesso desta substância.
(Dados: massas atômicas Fe=55,8; C=12; O=16,0)
Para preparar 75 mL de uma solução tampão fosfato de potássio 0,05 mol.L-1 (pH 2,3), serão necessários 450 mg de ácido fosfórico. Qual volume deve ser utilizado de ácido fosfórico a partir de uma apresentação comercial desse ácido com 85% de pureza para o preparo da solução tampão?
(Dados: densidade=1,88 g.cm-3)

Considerando essas informações e os diversos aspectos a elas relacionados, julgue o item que se segue.
Apesar da grande contribuição da alquimia para a ciência, as primeiras transformações químicas conduzidas pelo ser humano aconteceram apenas com o surgimento da química moderna.
A equação a seguir sintetiza a reação de combustão entre o salitre, o enxofre e o carvão, substâncias presentes na pólvora.
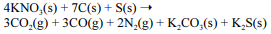
Acerca desse assunto, julgue o próximo item.
Sendo a pólvora formada somente por salitre, enxofre e carvão, na mesma proporção molar da reação apresentada, a queima de 10,0 g de pólvora produzirá mais de 3,0 g de sulfeto de potássio (K2S).

Considere as reações I, II e III a seguir.
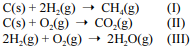
Com relação a essas informações, julgue o item que se segue.
De acordo com a teoria da ligação de valência, nas moléculas de metano e de água ocorre a hibridização para se formar um orbital híbrido do tipo sp3 , o que leva as duas moléculas a terem arranjos eletrônicos tetraédricos.
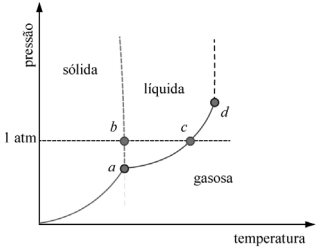
A figura precedente mostra um diagrama de fase para uma substância pura que exibe três fases: sólida, líquida e gasosa. Com base nessas informações, julgue o item subsecutivo.
A uma dada temperatura, a sublimação da substância em questão é favorecida aumentando-se a pressão.
As interações intramoleculares e intermoleculares são as responsáveis pelas várias fases (estados) da matéria e pelas propriedades físico-químicas dos materiais, além de necessárias para a determinação de estruturas de moléculas biologicamente importantes. Acerca das ligações químicas nos materiais, julgue o próximo item.
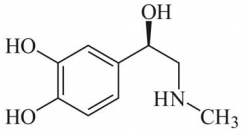
A estrutura química da epinefrina, mostrada a seguir, dispõe de sítios capazes de interagir com seus receptores no organismo, por meio de interações químicas de Van der Waals e de ligação de hidrogênio, além de ligação iônica.
Considere que, para determinar a concentração de uma solução de H
2S, um químico tenha misturado uma alíquota de 20,0 mL dessa solução com 20,0 mL de uma solução-padrão de NaOH (aq) 0,430 mol/L. Após a reação de neutralização, ele determinou o excesso de NaOH na solução resultante por meio da titulação dessa solução com 20,0 mL de uma solução-padrão de HC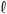
Considerando essas informações e que a viragem do indicador fenolftaleína ocorra na faixa de pH entre 8,2 e 9,8, julgue o item que se segue.
No ponto de viragem da fenolftaleína, durante a titulação que envolve as soluções de NaOH e HC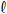
A tabela periódica e o modelo atômico evoluíram gradualmente ao longo do tempo, até as versões atuais. A figura precedente mostra uma ilustração bastante utilizada na representação de um átomo e que se baseia no modelo atômico de Bohr. Com relação à tabela periódica, aos modelos atômicos e aspectos a eles relacionados, julgue o próximo item.
As primeiras propostas de tabela periódica baseavam-se na massa atômica dos elementos como critério de alocação dos elementos ao longo da tabela, o que causava algumas incoerências que, mais tarde, foram sanadas com a adoção do número atômico como critério.

A tabela periódica e o modelo atômico evoluíram gradualmente ao longo do tempo, até as versões atuais. A figura precedente mostra uma ilustração bastante utilizada na representação de um átomo e que se baseia no modelo atômico de Bohr. Com relação à tabela periódica, aos modelos atômicos e aspectos a eles relacionados, julgue o próximo item.
Com exceção do hélio, os gases nobres possuem oito elétrons de valência e, por esse motivo, não são capazes de compartilhar elétrons para formar ligações covalentes.
Os alquenos são matéria-prima de grande importância na indústria porque podem ser facilmente transformados em uma vasta gama de compostos químicos. Exemplos típicos são as reações de hidratação e de polimerização catalisadas por ácido. Com relação às reações de alquenos, julgue o item subsequente.
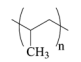
A estrutura do polímero formado pela reação de polimerização por adição do propeno está corretamente representada na figura a seguir.
Os alquenos são matéria-prima de grande importância na indústria porque podem ser facilmente transformados em uma vasta gama de compostos químicos. Exemplos típicos são as reações de hidratação e de polimerização catalisadas por ácido. Com relação às reações de alquenos, julgue o item subsequente.
O efeito da adição do catalisador ácido é o de reduzir a energia de ativação da reação e, com isso, aumentar a fração de colisões efetivas.
Analise o texto a seguir, a respeito do funcionamento básico de um equipamento rotineiramente usado em laboratório de química. A qual equipamento o texto se refere?

A reciclagem de resíduos gerados nos laboratórios de química é importante para a manutenção adequada do meio ambiente. Nesse contexto, assinale a alternativa que apresenta a técnica mais adequada para a separação/purificação de misturas de dois ou mais solventes orgânicos miscíveis, de pontos de ebulição próximos.