Na indústria, o densímetro é frequentemente usado na caracterização de diferentes materiais. A respeito dos densímetros e seus usos, assinale V para as afirmações verdadeiras, ou F para as falsas.
( ) O densímetro é frequentemente usado na exata identificação e caracterização de diferentes materiais, pois a densidade é uma propriedade específica de cada substância.
( ) Como a densidade varia diretamente com a temperatura e pressão, seu valor é dado em função dessas outras grandezas.
( ) A densidade não varia com o volume ocupado por determinada massa. Assim, amostras muitos concentradas apresentam a mesma densidade que aquelas diluídas, nas mesmas condições de temperatura e pressão.
( ) O alcoômetro é um tipo específico de densímetro usado para medir o teor do álcool etílico em misturas hidroalcoólicas, sob temperatura pré-definida.
A sequência correta, de cima para baixo, é:
Analise a equação e as afirmações a seguir, a respeito dos fatores que afetam o equilíbrio de solubilidade e a cinética química das reações. Assinale V para as afirmações verdadeiras, ou F para as falsas.
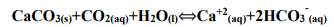
( ) Se a água subterrânea contendo dióxido de carbono (CO2) dissolvido entrar em contato com calcário (CaCO3), à baixa pressão (ex. no interior de uma caverna), mais CaCO3 é dissolvido.
( ) Se a água subterrânea contendo dióxido de carbono (CO2) dissolvido gotejar sobre o calcário (CaCO3), à alta pressão (ex. em regiões de águas profundas), CaCO3 permanece no estado sólido (ex. na forma de estalactites e estalagmites).
( ) Se a água do mar contendo dióxido de carbono (CO2) dissolvido entrar em contato com o calcário (CaCO3), a altas temperaturas (ex. regiões de mar quente), CaCO3 permanece no estado sólido (ex. na forma de corais).
( ) Se a água do mar contendo dióxido de carbono (CO2) dissolvido entrar em contato com o calcário (CaCO3), a baixas temperaturas (ex. regiões de mar frio), mais CaCO3 é dissolvido.
A sequência correta, de cima para baixo, é:
A oxigenoterapia consiste na administração suplementar de oxigênio (O2) gasoso a um paciente, com o objetivo de elevar ou manter a saturação de oxigênio aos níveis aceitáveis, corrigindo uma possível deficiência no aporte de oxigênio aos tecidos nesse indivíduo. A quantidade de oxigênio a ser administrada é medida em função do teor de oxigênio no paciente, e as informações sobre a quantidade de mols de O2 são necessárias para a correta aplicação da técnica. A esse respeito, assinale a alternativa que apresenta aproximadamente o número de mols de oxigênio em uma amostra contendo 1,20x1021 moléculas de O2.
(Dados: número de Avogadro=6,02x1023)
Questão anterior:

Ainda a respeito da produção de amônia, conforme reação apresentada anteriormente (questão 52), assinale a alternativa que apresenta, respectivamente, quantas moléculas de H2(g) serão consumidas na reação, considerando que foram consumidas 3,60x1020 moléculas de N2(g), e quantos mols de NH3(g) serão produzidos, se forem empregados 1,2mols de N2.
O ácido clorídrico com a denominação PA (Padrão Analítico) é comercializado em solução a 37%. Por ser um ácido forte, que origina soluções diluídas estáveis, é frequentemente empregado em análises titrimétricas. Para conhecer a real concentração do HCl nas soluções empregadas, torna-se necessário o procedimento de padronização das mesmas. Assinale a alternativa que apresenta uma substância que pode ser empregada como padrão primário para a padronização do HCl, e a justificativa para sua escolha.
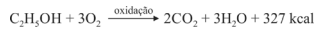
Sabendo que a reação apresentada mostra o processo de oxidação do etanol — em que são liberadas 327 kcal por mol de energia — e que as massas atômicas do carbono, do oxigênio e do hidrogênio são, respectivamente, iguais a 12, 16 e 1, julgue o item a seguir.
Para cada mol de etanol, são liberados 88 g de CO2.
A separação de misturas é um tema importante no ensino de química, pois muitos processos industriais ou cotidianos exigem a utilização de substâncias puras ou com o maior grau de pureza possível. Sendo assim, assinale a alternativa que apresenta processos de separação de misturas.
O estado gasoso é o mais simples e o mais estudado da matéria. Além disso, os gases têm muitas aplicações e muitas reações acontecem nessa fase. A respeito da lei dos gases ideais, é correto afirmar que
Uma reação química entre um ácido e uma base é denominada de reação de neutralização. O composto iônico produzido nesse tipo de reação é chamado de sal. O estudo dos diversos tipos de sal mostra‐se, portanto, de essencial importância no estudo da química. Sendo assim, assinale a alternativa que apresenta exemplos de sais que, quando dissolvidos em água, promovem a diminuição do valor do pH.
Termoquímica é o ramo da química que estuda os calores de reações e a energia envolvida em transformações químicas. A partir dessa informação, considerem‐se as duas equações químicas a seguir, que representam a reação de combustão do metano, com dois diferentes conjuntos de produtos, em que são indicadas as respectivas variações de entalpia (ΔH).
Assinale a alternativa que apresenta a relação entre essas variações de entalpia.
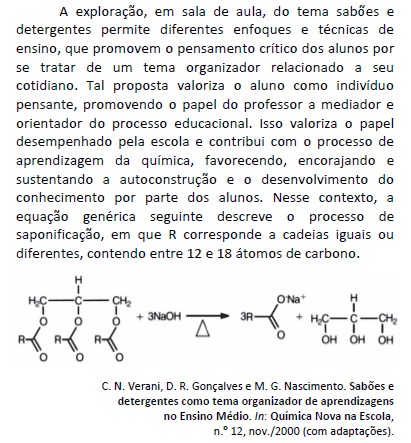
Assinale a alternativa que apresenta as principais características químicas dos sabões.
Com relação aos métodos de preparação, polímeros de condensação são produzidos quando ocorre reação
No laboratório de controle de qualidade de uma indústria petroquímica, equivocadamente uma amostra de benzeno puro foi misturada à outra de hexano, também puro. Com o objetivo de determinar a composição molar da mistura, uma pequena amostra foi transferida para recipiente fechado e mantida a 25 ºC até que o equilíbrio líquido-vapor fosse estabelecido. Então, o vapor da mistura foi analisado por cromatografia gasosa, que indicou haver 25 %, em mol, de hexano. Considerando o sistema ideal e que a pressão de vapor do hexano puro é 135 mmHg e do benzeno é 95,1 mmHg, a 25 ºC, assinale a alternativa que contem a porcentagem molar de hexano no líquido em equilíbrio com o vapor a 25 ºC.
Uma amostra de 2,00 mL de uma solução de Fe2+ de concentração desconhecida foram adicionados a 1,00 mL de água destilada, 2,00 mL de solução diluída de H2O2 e 1,00 mL de alcalina de luminol. A medida da quimiluminescência desta amostra indicou um sinal integrado de 16,1. Quando, a uma outra alíquota de 2,00 mL desta amostra, foi adicionado 1,00 mL de solução de Fe2+ a 4,75.10-5 mol/L, e os mesmos volumes das soluções de H2O2 e luminol, o sinal integrado de quimiluminescência foi 29,6. Considerando que a intensidade da quimiluminescência aumenta linearmente com a concentração de Fe2+, determine a concentração deste íon na amostra inicial e indique a alternativa que apresenta o valor correto.
Analise as seguintes reações orgânicas e indique a alternativa que apresenta uma reação cujo produto apresentado é o esperado para a reação.