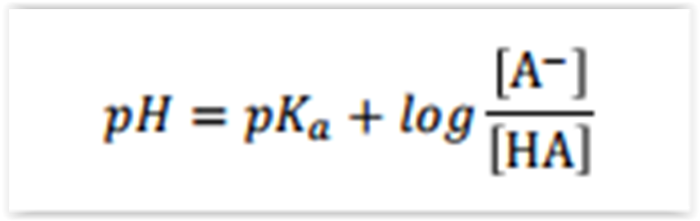Um técnico de laboratório da CASAN realizará um teste para determinar o teor de nitrato de prata em uma amostra de acordo com a seguinte reação: NaCl + AgNOM3 → AgCl + NaNO3 . Foram consumidos 36g de NaCl nesta reação. Assim, podemos afirmar que a quantidade de nitrato de prata na amostra é (Massa molar NaCl=58,6; AgNO3 = 169,9)
Em uma aula de Ciências, o professor escreveu no quadro a
seguinte frase:
Preguiças que se alimentam de folhas de embaúbas apresentam
pulgas que, por sua vez são parasitadas por protozoários.
Abaixo da frase, desenhou as três pirâmides ecológicas a seguir,
simbolicamente relacionadas à cadeia alimentar incluída na frase,
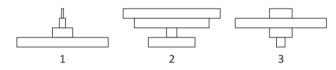
Seus alunos, após compararem as pirâmides com a cadeia
alimentar contida na frase, chegaram às seguintes conclusões:
I. a pirâmide 1 corresponde à pirâmide de biomassa;
II. a pirâmide 2 corresponde à pirâmide de números; e
III. a pirâmide 3 não tem correspondência com os seres da
cadeia.
Está correto o que se afirma em
No laboratório de Ciências o professor colocou 3 mL de água oxigenada (H2O2) em um tubo de ensaio, acrescentou uma pitada de um catalisador (MnO2 ) e, imediatamente, ocorreu uma efervescência, característica da liberação de um gás. Para testar o gás liberado, o professor introduziu um barbante em brasa dentro do tubo e a brasa inflamou. A repetição do experimento com água pura, em vez de água oxigenada, não teve o mesmo resultado, isto é, a brasa ficou mais fraca e não se inflamou. O experimento permitiu que os alunos concluíssem que o gás liberado era
O conceito de solubilidade pode ser trabalhado em sala de aula
por meio de análise da curva de solubilidade apresentada sob a
forma de gráficos e/ou da realização de experimentos simples
que mostrem os fatores que alteram a solubilidade.
Após uma discussão sobre esse assunto em sala de aula foram
levantados pelos alunos alguns fatores que alteram a solubilidade
tais como: o solvente, o ponto de fusão do soluto, a temperatura
da solução, a pressão, as interações intermoleculares envolvidas.
O fator apresentado pelos alunos que deve ser rediscutido por
não influenciar na solubilidade das substâncias é
O professor propôs, como introdução ao estudo das reações de
oxirredução, um experimento bem simples para que o aluno
tenha condições de observar um fenômeno que envolve
mudanças visuais muito nítidas desse tipo de reação.
No experimento, o aluno deve acrescentar um comprimido de
vitamina C não efervescente a uma solução de iodo
(farmacêutica) e adicionar água. Nessa reação a vitamina C que é
oxidada promove um descoramento da solução de iodo que é
reduzido.
A transformação que ocorre no iodo pode ser codificada em uma
linguagem química como
Relacione os conceitos que têm sido utilizados por pesquisadores
para refletir sobre o ensino de Química/Ciências aos respectivos
idealizadores/fundamentos.
1- Construtivismo
2- Aprendizagem significativa
3- Processo de internalização
4- Teoria da enunciação
( ) Constructo fundamental na obra de Vygotsky que aponta
para questões relacionadas com a constituição do sujeito.
( ) Foi proposta por Bakhtin que, juntamente com outras noções
como as de dialogia e das vozes, considera as interações
verbais orais e escritas na produção do conhecimento.
( ) Noção marcada por uma variedade de visões e abordagens,
as vezes contraditórias, que busca a valorização das
contribuições dos estudantes no processo ensinoaprendizagem.
( ) Admite que a aprendizagem ocorre por meio da “ancoragem”
de um novo conhecimento a um conceito já existente na
estrutura cognitiva do sujeito.
Assinale a opção que indica a relação correta, de cima para baixo.
No ensino de Química, os conteúdos abordados e as atividades
desenvolvidas devem ser propostas de forma a promover o
desenvolvimento de competências dentro de três domínios, com
suas características e especificidades próprias.
Segundo os Parâmetros Curriculares Nacionais para o Ensino
Médio, esses três domínios são:
Compostos orgânicos de baixa polaridade, como o p-diclorodifenil-tricloro-etano
(DDT), são pouco solúveis em água e muito
solúveis no tecido adiposo.
Quando um pesticida com polaridade semelhante ao DDT passa
da solução aquosa para a gordura dos animais pode ocorrer o
processo apresentado no esquema a seguir.
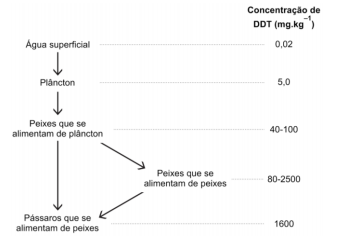
O processo é denominado
Foi detectada a presença de 32µg de dióxido de enxofre em 100L
de ar de um recinto fechado que se encontra a 25°C (a 1 atm).
A composição em ppm (v/v) desse poluente no recinto,
considerando o comportamento ideal dos gases, é
aproximadamente igual a
Dados: Constante dos gases = 0,082 atm.L.mol–1.K–1. Massa molares
(g.mol–1): S = 32 e O = 16
Usinas alimentadas por combustíveis fósseis (gás natural, diesel e
carvão) emitem grandes quantidades de CO2
.
Considerando as emissões de CO2 por kWh (quilowatt hora)
produzido, o combustível menos poluente e o mais poluente são,
respectivamente:
Todas as afirmações sobre as propriedades dos elementos químicos e a tabela periódica estão corretas, EXCETO.
Ao realizar uma inspeção em um depósito de materiais reciclados, um fiscal encontrou uma estátua fabricada em cobre puro, cuja massa é de 612g. Sabendo-se que a massa molar do cobre é de 63,55 g.mol-1, quantos mols de cobre contém a estátua?
Ao realizar-se a vistoria em um aterro sanitário, o fiscal
verificou que o aterro utilizava o gás metano produzido
para queima, gerando calor em um forno. Para assar um
bolo, foram consumidos 3.500g de metano. Determine qual
a quantidade de calor (em módulo) produzida no forno
para assar o bolo.
Dados:
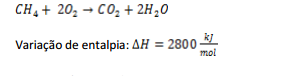
Massas atômicas relativas:
C = 12
H = 1
Para que os resíduos de laboratório possam ser eliminados de forma adequada, é necessário ter à disposição recipientes de tipo e tamanho adequados. Os recipientes coletores devem ser caracterizados claramente de acordo com o seu conteúdo, o que também implica em se colocar símbolos de periculosidade. No caso de embalagem para resíduos químicos perigosos, pode-se afirmar que: I.Resíduos líquidos contendo solventes devem ser armazenados em garrafas de vidro ou bombonas de material compatível. II.Resíduos líquidos isentos de solventes devem ser armazenados em frascos metálicos ou de aço inoxidável. III.Resíduos sólidos e lodos devem ser armazenados em recipientes (embalagens) individuais resistentes à ruptura. Assinale a alternativa correta:
Uma solução tampão é definida como uma solução
de um par de ácido-base conjugado ou uma base-
ácido conjugado. Essa solução tem a capacidade
de resistir a variações de pH quando são
adicionadas pequenas quantidades quer de ácido,
quer de base. As soluções tampões são muito
importantes nos sistemas químicos e biológicos. O
pH de uma solução tampão pode ser estimado pela
equação de Henderson-Hasselbalch:
imagem
em que, o HA é o ácido e A– é a base conjugada.
Com base no exposto, identifique as afirmativas
verdadeiras.
I.O pH da solução será igual ao pKa se a [A–] forigual a [HA]
II.O pH tende a aumentar se a concentração a [A–]for maior que [HA]
III.O pH tende a diminuir se a concentração a [A–]for maior que [HA]
IV.O pH tende a aumentar se a concentração a [A–]for menor que [HA]
V.O pH tende a diminuir se a concentração a [A–]for menor que [HA]
Assinale a alternativa correta: