Assinale a alternativa CORRETA sobre os parâmetros básicos que regem a resolução de uma separação:
Assinale a alternativa INCORRETA:
Atenção: As questões de números 31 a 34 referem-se ao conteúdo de Noções de Gás Natural.
Em comparação ao Gás Liquefeito de Petróleo − GLP, o gás natural tem uma maior capacidade de se dissipar na atmosfera. Isso se deve, basicamente
Dentre os hidrocarbonetos que compõem o gás natural, destacam-se nos campos (bacias) de exploração no Brasil
A companhia distribuidora adiciona um produto ao gás denominado odorante. A função do odorante é
Uma das aplicações do gás natural é no segmento residencial que NÃO o utiliza em
O gás natural de uma determinada tubulação tem o Limite Inferior de Explosividade de aproximadamente 5% em volume e o Limite Superior de Explosividade de aproximadamente 15% em volume. Isso significa que, se essa tubulação se romper e provocar uma mistura entre gás natural e ar, em que o gás natural esteja a uma concentração de 20% em volume
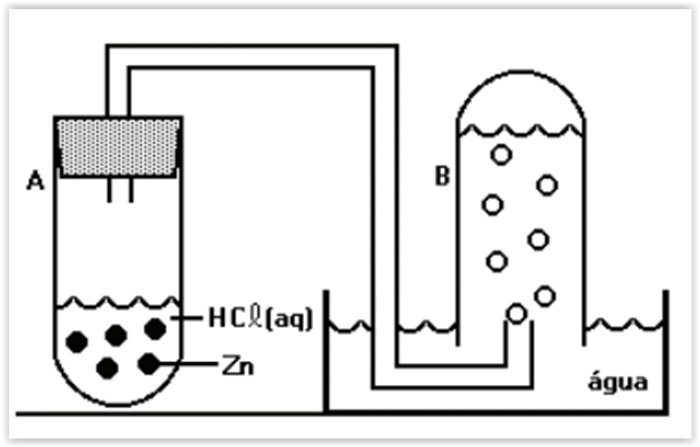
Um tubo inicialmente cheio de água (B ) foi conectado a
outro tubo (A ), ao qual foi adicionada solução de ácido
clorídrico e raspas de zinco com alto grau de pureza. O
sistema foi fechado e após algum tempo, apresentavase
como indicado na figura.
Analise as propostas a seguir:
I.Parte significativa do gás hidrogênio ficará retida na
água formando uma solução de caráter ácido.
II.A pressão de vapor da água, na temperatura da
realização do experimento, é importante para o cálculo
sobre o volume de hidrogênio, caso não se leve em
consideração a pressão de vapor da água o valor de
gás hidrogênio obtido será maior que o verdadeiro.
III.Quando o nível da água no interior do tubo B se igualar
com o nível da água do restante da cuba, pode-se
afirmar que a soma da pressão do hidrogênio com a
pressão de vapor da água, na temperatura de realização
do experimento, será praticamente igual à pressão
atmosférica local.
Assinale a alternativa que contém as propostas
verdadeiras:
O ácido perclórico P.A. apresenta concentração de 70%, sabendo que a densidade do ácido perclórico é 1,68g/cm-3 , assinale a alternativa que apresente o volume aproximado de solução do ácido que deve ser adicionado a um balão volumétrico de 200mL, afim de preparar uma solução 0,1 mol/L. Dados M=100,46g.mol-1
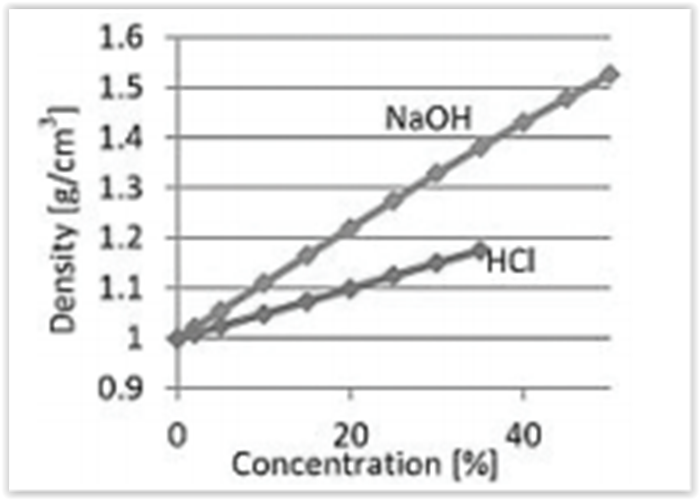
O diagrama a seguir apresenta a relação entre a
densidade e a concentração em porcentagem em
massa para o hidróxido de sódio (M = 40 g/mol) e o
ácido clorídrico (M = 36,5 g/mol).
Em uma situação hipotética, onde as duas soluções
apresentem densidade ao redor de 1,1g/cm³
é correto
afirmar que as concentrações, em mol/L, para o NaOH e
para o HCl serão respectivamente:
A um laboratorista, foi solicitado preparar 0,5 L de uma solução de sulfato de cobre (II) com concentração de 0,0190 mol.L-1 a partir de sulfato de cobre (II) penta-hidratado. A massa de CuSO4.5H2O necessária para esta preparação será:
A realização de aulas experimentais de química é uma importante estratégia para o ensino de cinética química. No tocante ao estudo da relação existente entre a superfície de contato dos reagentes e a velocidade da reação química, o procedimento experimental que melhor expressa essa relação é:
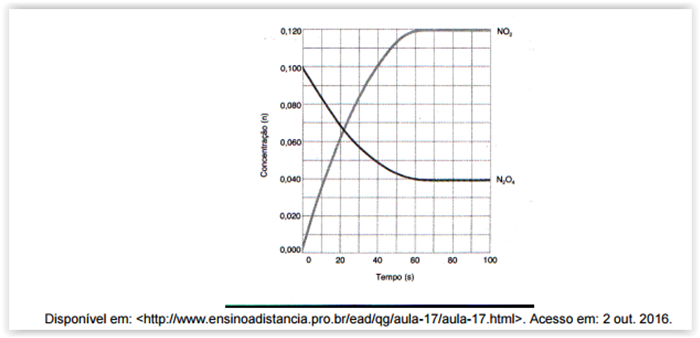
Considere o gráfico a seguir
Por meio da análise do gráfico de equilíbrio químico da reação de decomposição do N2O4, foi
construída uma tabela de evolução temporal do processo reativo. A alternativa que expressa essa
tabela corretamente é:
A titulação potenciométrica consiste em um método eletroanalítico com algumas vantagens quando comparada à titulação simples. Entre essas vantagens, está a de que
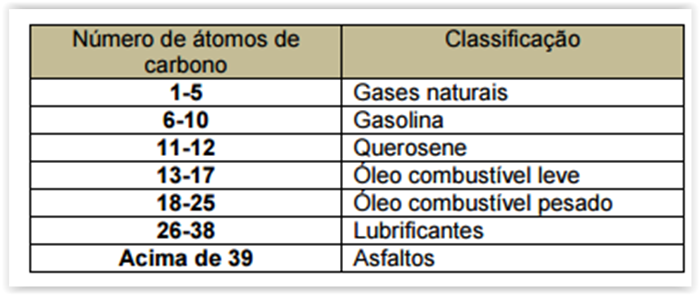
A tabela a seguir apresenta uma série de compostos extraídos do fracionamento do petróleo.
O ponto de ebulição dos compostos da tabela é diretamente proporcional ao