A amônia é um gás incolor à temperatura ambiente e possui um odor
extremamente forte. Seu caráter polar é a principal razão para a sua solubilidade em
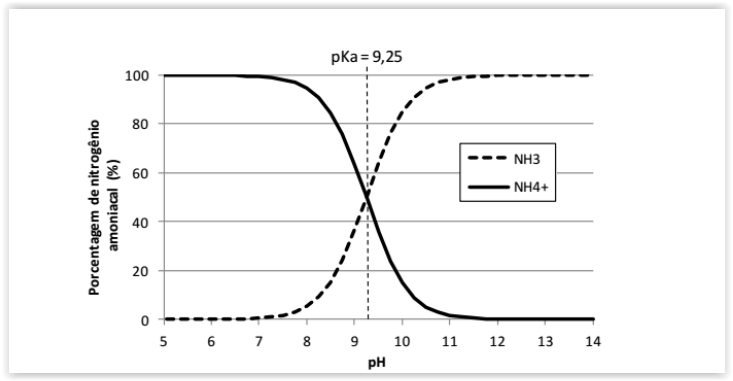
água, sendo que em ambientes aquáticos, o nitrogênio amoniacal compreende as
formas do íon amônio (NH4+) e da amônia (NH3) dissolvidos, de maneira que a
proporção entre elas depende da temperatura, salinidade e, principalmente, do pH
do meio.
De acordo com o gráfico acima e os conhecimentos sobre equilíbrio químico.
Assinale a alternativa CORRETA:
As técnicas eletroanalíticas se baseiam em processos de ________onde as espécies eletroativas do meio oferecem resposta à aplicação de um _______para o monitoramento da corrente elétrica ou valor do potencial em comparação ao potencial de um eletrodo de referência. A ________e a _______são bastante utilizadas em análises de espécies eletroativas orgânicas e inorgânicas e na determinação seletiva de íons orgânicos e inorgânicos em solução, respectivamente. Assinale a alternativa que corresponde as palavras CORRETAS para cada respectivo espaço vazio.
Para a segurança biológica do laboratório é crucial um conhecimento básico de
desinfecção e esterilização e dos seus princípios gerais. De acordo com estes
princípios, enumere a segunda coluna de acordo com a primeira e assinale a
alternativa CORRETA.
(1) Antimicrobiano
(2) Desinfecção
(3) Anti-séptico
(4) Esterilização
(5) Microbiocida
(6) Esporocida
( ) Processo que mata e/ou remove todas as classes de microrganismos e esporos.
( ) Substância que inibe o crescimento e desenvolvimento de microrganismos sem necessariamente os matar.
( ) Agente que mata microrganismos ou impede o seu desenvolvimento e multiplicação.
( ) Substância química ou mistura de substâncias químicas que matam microrganismos.
( ) Meio físico ou químico de matar microrganismos, mas não necessariamente esporos.
( ) Substância química ou mistura de substâncias químicas utilizadas para matar microrganismos e esporos.
Os fluoretos são os principais responsáveis pela redução da cárie dentária em países desenvolvidos e também no Brasil. Além da redução da prevalência da cárie, o flúor age reduzindo a velocidade de progressão de novas lesões. Em São Gonçalo, na ETA de Laranjal, o flúor é colocado na água através da adição de H2SiF6 (http://www.cruiser.com.br /sg/sg29.html), aplicado por meio de uma bomba dosadora de fluxo contínuo. H2SiF6 é uma substância:
A palavra alquimia, AL-Khemy, vem do árabe e quer dizer “a química”. Esta ciência começou a se desenvolver por volta do século III a. C. e obteve grande êxito na metalurgia, na produção de papiros e na aparelhagem de laboratório. A partir das obscuras etimologias e através de uma leitura intrincada, enigmática e carregada de símbolos dos escritos alquimistas, pode-se ter claramente que uma das finalidades da alquimia era transformar os metais chamados inferiores (principalmente o mercúrio e o chumbo) em ouro e prata, metais tidos como superiores. (http://www.cdcc.sc.usp.br/ciencia/artigos/art_25/alquimia. html, adaptado.) Para obter átomos de ouro a partir de átomos de metais inferiores, seria necessário que os alquimistas fossem capazes de:
Considerando a decomposição do nitrato
de amônio: NH4 NO3 → X N2 O + Y H2O, os
valores correspondentes a X e Y devem ser,
respectivamente,
Um técnico da CASAN irá coletar amostras de água em residências e encaminhá-las para análise microbiológica. Para isso, ele deve utilizar
Uma solução que possui 1 µg/mL de soluto possui quantos gramas por litro do soluto?
Sobre a titulação de um ácido forte por uma base forte, assinale a alternativa correta.
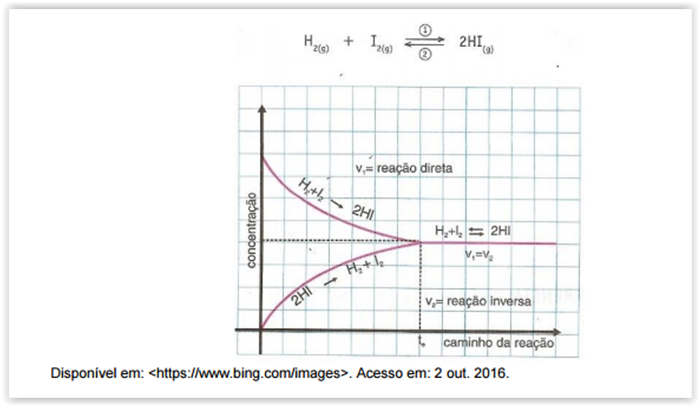
Considere o gráfico a seguir
Por meio da análise do gráfico, é possível destacar que o equilíbrio
A estocagem de substâncias deve levar em consideração a incompatibilidade dos reagentes para que não se iniciem reações espontâneas que provoquem riscos químicos nos laboratórios. Assim, é incompatível para estocagem
O Tolueno é uma substância presente em certas colas, que, se “cheiradas”, podem produzir uma excitação semelhante àquela causada pelo consumo de álcool, como visão dupla, fala inarticulada e falta de coordenação, podendo, ainda, resultar em estupor, coma e morte. A fórmula estrutural dessa substância éimagem
A glicose, na presença de enzimas, passa por um processo de fermentação, no qual açúcares são quimicamente convertidos em
Soluções de soda cáustica são constantemente utilizadas para ajuste de pH e para neutralizar soluções ácidas. Uma solução de hidróxido de sódio (NaOH) foi preparada dissolvendo-se 200 g de NaOH em 1000 g de água. Determine qual é a concentração em mol/L desta solução. (Dados: densidade da água = 1,0 g/cm3; massas molares: H= 1,0 g/mol, Na= 23 g/mol, O= 16 g/mol; 1 cm3 = 0,001 dm3). Assinale a alternativa CORRETA.
O Sulfato de amônio é um composto inorgânico utilizado na agricultura como
fertilizante. Este sal é obtido pela reação entre a amônia e o ácido sulfúrico, de
acordo com a reação abaixo.
NH3 + H2SO4 → (NH4)2SO4
Se a obtenção deste sal for obtida através da lavagem do gás amônia com uma
solução de ácido sulfúrico, dado que a concentração de amônia é de 34.000 mg/L,
qual seria a concentração de ácido sulfúrico em mol/L necessária para se obter
100% de rendimento? (Dados: massas molares: H= 1,0 g/mol, N= 14 g/mol, O= 16
g/mol, S= 32 g/mol)