O conceito de solubilidade pode ser trabalhado em sala de aula
por meio de análise da curva de solubilidade apresentada sob a
forma de gráficos e/ou da realização de experimentos simples
que mostrem os fatores que alteram a solubilidade.
Após uma discussão sobre esse assunto em sala de aula foram
levantados pelos alunos alguns fatores que alteram a solubilidade
tais como: o solvente, o ponto de fusão do soluto, a temperatura
da solução, a pressão, as interações intermoleculares envolvidas.
O fator apresentado pelos alunos que deve ser rediscutido por
não influenciar na solubilidade das substâncias é
O professor propôs, como introdução ao estudo das reações de
oxirredução, um experimento bem simples para que o aluno
tenha condições de observar um fenômeno que envolve
mudanças visuais muito nítidas desse tipo de reação.
No experimento, o aluno deve acrescentar um comprimido de
vitamina C não efervescente a uma solução de iodo
(farmacêutica) e adicionar água. Nessa reação a vitamina C que é
oxidada promove um descoramento da solução de iodo que é
reduzido.
A transformação que ocorre no iodo pode ser codificada em uma
linguagem química como
Relacione os conceitos que têm sido utilizados por pesquisadores
para refletir sobre o ensino de Química/Ciências aos respectivos
idealizadores/fundamentos.
1- Construtivismo
2- Aprendizagem significativa
3- Processo de internalização
4- Teoria da enunciação
( ) Constructo fundamental na obra de Vygotsky que aponta
para questões relacionadas com a constituição do sujeito.
( ) Foi proposta por Bakhtin que, juntamente com outras noções
como as de dialogia e das vozes, considera as interações
verbais orais e escritas na produção do conhecimento.
( ) Noção marcada por uma variedade de visões e abordagens,
as vezes contraditórias, que busca a valorização das
contribuições dos estudantes no processo ensinoaprendizagem.
( ) Admite que a aprendizagem ocorre por meio da “ancoragem”
de um novo conhecimento a um conceito já existente na
estrutura cognitiva do sujeito.
Assinale a opção que indica a relação correta, de cima para baixo.
No ensino de Química, os conteúdos abordados e as atividades
desenvolvidas devem ser propostas de forma a promover o
desenvolvimento de competências dentro de três domínios, com
suas características e especificidades próprias.
Segundo os Parâmetros Curriculares Nacionais para o Ensino
Médio, esses três domínios são:
Compostos orgânicos de baixa polaridade, como o p-diclorodifenil-tricloro-etano
(DDT), são pouco solúveis em água e muito
solúveis no tecido adiposo.
Quando um pesticida com polaridade semelhante ao DDT passa
da solução aquosa para a gordura dos animais pode ocorrer o
processo apresentado no esquema a seguir.
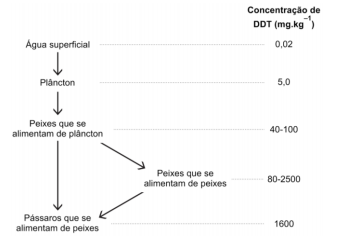
O processo é denominado
Foi detectada a presença de 32µg de dióxido de enxofre em 100L
de ar de um recinto fechado que se encontra a 25°C (a 1 atm).
A composição em ppm (v/v) desse poluente no recinto,
considerando o comportamento ideal dos gases, é
aproximadamente igual a
Dados: Constante dos gases = 0,082 atm.L.mol–1.K–1. Massa molares
(g.mol–1): S = 32 e O = 16
Usinas alimentadas por combustíveis fósseis (gás natural, diesel e
carvão) emitem grandes quantidades de CO2
.
Considerando as emissões de CO2 por kWh (quilowatt hora)
produzido, o combustível menos poluente e o mais poluente são,
respectivamente:
Todas as afirmações sobre as propriedades dos elementos químicos e a tabela periódica estão corretas, EXCETO.
Ao realizar uma inspeção em um depósito de materiais reciclados, um fiscal encontrou uma estátua fabricada em cobre puro, cuja massa é de 612g. Sabendo-se que a massa molar do cobre é de 63,55 g.mol-1, quantos mols de cobre contém a estátua?
Ao realizar-se a vistoria em um aterro sanitário, o fiscal
verificou que o aterro utilizava o gás metano produzido
para queima, gerando calor em um forno. Para assar um
bolo, foram consumidos 3.500g de metano. Determine qual
a quantidade de calor (em módulo) produzida no forno
para assar o bolo.
Dados:
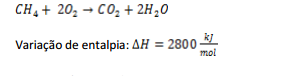
Massas atômicas relativas:
C = 12
H = 1
Um estudo realizado na reserva Yanomami (RR), coordenado pela Fundação Oswaldo Cruz e o Instituto Socioambiental (ISA), mostra que em algumas aldeias indígenas 92% das pessoas examinadas estão contaminadas por mercúrio. Nesse estudo, a análise das concentrações de metilmercúrio em peixes carnívoros e peixes onívoros, que constituem uma das principais fontes de exposição humana ao metilmercúrio, sobretudo em populações ribeirinhas, mostrou que a média da concentração de mercúrio nos peixes carnívoros foi de 0,14 µg.g-1, enquanto nos peixes onívoros essa média foi de 0,10 µg.g-1. O resultado para a concentração de metilmercúrio nos peixes é coerente, pois:
A grafite, também chamada chumbo negro ou plumbagina, tem múltiplas e importantes aplicações industriais, embora seja mais conhecida popularmente por sua utilização como mina do lápis. Quantos átomos de carbono são encontrados em uma massa de 1,02g de grafite? (Dado: número de Avogadro = 6,02x1023)
Uma mistura de dois líquidos imiscíveis entre si
podem ser separadas pela técnica denominada:
Considerando a teoria dos gases julgue as
afirmativas a seguir:
I.Em um processo isotérmico, o volume de um gás
aumenta de modo diretamente proporcional ao
aumento da pressão.
II.As moléculas de um gás ideal se chocam de
modo perfeitamente elástico sem perda de
energia cinética média.
III.Um gás real aproxima-se do comportamento de
um gás ideal a pressões baixas e temperaturas
altas.
IV.As moléculas de um gás ideal se movimentam de
modo ordenado e a velocidades baixas.
V.Em um processo isobárico, o volume de um gás
aumenta de modo diretamente proporcional ao
aumento da temperatura.
Está correto apenas o que se afirma em:
Atenção: As questões de números 31 a 34 referem-se ao conteúdo de Noções de Gás Natural.
Em comparação ao Gás Liquefeito de Petróleo − GLP, o gás natural tem uma maior capacidade de se dissipar na atmosfera. Isso se deve, basicamente

