A seguir, são apresentadas quatro projeções de Newman de moléculas orgânicas.
As projeções que não formam um par de estereoisômeros, ou seja, que representam a mesma molécula, são:
Em virtude de características estruturais e eletrônicas, algumas espécies químicas orgânicas são classificadas como aromáticas. Na figura a seguir estão apresentadas algumas estruturas de moléculas ou íons orgânicos
As espécies químicas aromáticas são aquelas representadas pelos números
Uma quantidade de sulfato cúprico foi adicionada em uma célula eletroquímica. Em seguida, aplicou-se uma corrente elétrica de 2,0 A durante 10 min. Considerando a constante de Faraday igual a 96.500 C mol-1 e a massa molar do cobre igual a 63,5 g mol-1, a massa, em gramas, do metal depositado na superfície de um dos eletrodos foi, aproximadamente, igual a
Uma solução foi preparada pela dissolução de 2,00 g de NaOH (40 g mol-1), com pureza igual a 90%, em água até se obter um volume final de 500 mL. Nesse caso, a concentração da solução, em mol L-1, é igual a
A solubilidade do cloreto de chumbo, em água a 25 °C, é 1,6x10-2 mol L-1. Portanto, a constante do produto de solubilidade é, aproximadamente, igual a
O texto contém tanto palavras do registro informal do trabalhador braçal quanto palavras do registro formal do conhecimento científico. Há palavras desses dois registros em:
O cartum acima explora e amplia a metáfora “estrada da vida” com base na
Na segunda estrofe, omite-se a seguinte expressão do início do terceiro verso:
Para uma molécula com mais de dois átomos o momento de dipolo depende tanto das polaridades das ligações individuais quanto da geometria da molécula. Considerando as seguintes moléculas poliatômicas, BF3, CO, SO2, CF4, NCl3 e SF2, quais são polares?
Substâncias no equilíbrio que estejam em fases diferentes dão origem aos equilíbrios heterogêneos. Um exemplo é representado pela equação a seguir:
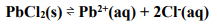
A expressão da constante de equilíbrio que representa a referida equação é:
Um analista precisa preparar 500 mL de uma solução aquosa 0,2 mol L -1 de ácido clorídrico a partir de uma solução comercial da qual extrai-se do rótulo do recipiente as seguintes informações: Teor mínimo = 37% (m/m); Densidade = 1,18 g mL-1; Massa molar = 36,5 g mol-1 .
O volume da solução comercial, em mL, a ser utilizado pelo analista, deve ser de, aproximadamente,
Os compostos que possuem o grupo carbonila (C=O), em razão da natureza de suas moléculas, apresentam diferentes reatividades em reações de adição nucleofílica.
Nessas reações, a molécula mais reativa é a de
Os rótulos dos reagentes contêm etiquetas apropriadas para indicar os riscos químicos, apresentados na forma de losango com quatro áreas coloridas. As cores azul, vermelha e amarela indicam, respectivamente, riscos associados à
Uma solução de HCl 5x10 -8 mol L-1 foi preparada em água à temperatura ambiente. Considerando o valor da constante do produto iônico da água (Kw) igual a 1x10-14, a percentagem de íons H+ proveniente da solução de HCl é igual a
Uma mistura equimolar de acetato de sódio e ácido acético foi preparada em água para formar uma solução tampão. Considerando o Ka do ácido acético igual a 2x10-5, o pH da solução preparada apresentou valor igual a







