Sobre as ligações químicas, assinale a afirmativa INCORRETA.
Os compostos binários, cujo elemento mais eletronegativo é o oxigênio, classificam‐se em: óxidos, peróxidos e superóxidos, em função do valor no número de oxidação (Nox) do átomo de oxigênio. Assinale a alternativa que apresenta somente peróxidos. (Considere apenas o conceito, independente de sua estabilidade ou não.)
Considere que os compostos com NaCl, LiBr, K2SO4, entre outros, são iônicos e formados a partir de íons (cátions e ânions) que se juntam para formar essas substâncias. São características (ou propriedades) típicas atribuídas aos compostos iônicos, EXCETO:
Bohr introduziu um único número quântico para descrever a estrutura eletrônica dos
átomos. A mecânica quântica usa três números quânticos para descrever um orbital.
Numere a COLUNA II de acordo com a COLUNA I, fazendo a relação entre as
informações que podemos obter desses números quânticos e o número quântico
relacionado.

Assinale a alternativa que apresenta a sequência CORRETA.
Um recipiente fechado de 10 litros contém 1 mol de molécula de nitrogênio e 3 mols de
moléculas de hidrogênio a 25 ºC.
Dado: R = 8,2 x 10–2 L.atm.K–1.mol–1
Considerando–se a hipótese de a mistura dos gases ser perfeita, qual é o valor
aproximado da pressão total no interior do recipiente?
Considere uma amostra de gás de moléculas de oxigênio, contida em um recipiente
fechado, mas que se pode controlar o volume. O gás inicialmente nas CNTP é
comprimido para um volume menor à temperatura constante.
Com relação aos efeitos ocasionados pela variação do volume do recipiente, é
INCORRETO afirmar que
À temperatura próxima de 800 °C, o vapor passado sobre o coque (uma forma de carbono
obtida a partir do carvão) quente reage para formar gases de CO e H2.
Observe a seguinte equação química.
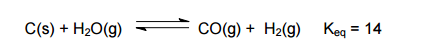
A mistura de gases resultante é um importante combustível industrial chamado gás
d'água.
Dado: R = 0,082 atm.L/mol.K
Se tenho, inicialmente, carbono sólido e 0,1 mol de H2O(g) em um recipiente de 1 L, é
CORRETO afirmar que a pressão parcial de equilíbrio do gás CO é aproximadamente
igual a
Em 1989, um adolescente em Ohio foi envenenado com vapor de mercúrio derramado. O
nível de mercúrio determinado em sua urina, que é proporcional a sua concentração no
organismo, foi de 1,54 mg.L–1 . O Hg2+ é eliminado do organismo por um processo de
primeira ordem que tem meia–vida de 6 dias (6D).
Após 30 dias (30D), se medidas terapêuticas não fossem tomadas, é CORRETO afirmar
que a expressão matemática que deduzirá a concentração de Hg2+ na urina do paciente,
em mg L–1 será
As cadeias de átomos de carbono de compostos orgânicos podem chegar a
comprimentos muito grandes e dar origem a macromoléculas. Os polímeros são
compostos macromoleculares, em que redes de unidades repetitivas pequenas formam
moléculas gigantes.
Numere COLUNA II de acordo com a COLUNA I, relacionando o tipo de polimerização e
o monômero gerador do polímero.

Assinale a alternativa que apresenta a sequência CORRETA.
A acrilonitrila é empregada na síntese de fibras acrílicas (poliacrilonitrilas). Sua estrutura
química é a seguinte:
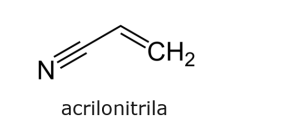
Com relação a essa estrutura, um químico descreveu sobre os orbitais híbridizados de
cada átomo de carbono da acrilonitrila no sentido da esquerda para a direita.
No sentido indicado, é CORRETO afirmar que os orbitais hibridizados dos átomos de
carbono são, respectivamente:
Na titulação de neutralização de 20,00 mL de ácido acético (CH3COOH) 0,100 mol/L com
10,00 mL de solução de NaOH 0,200 mol/L, é CORRETO afirmar que o pH da solução
titulada será aproximadamente igual a
Considere que Ka = 1,8×10–5; log2 = 0,3; log3 = 0,5
Considere os seguintes compostos: GeO44–; K4Ge4Te10 e Ca4GeO5.
Os números de oxidação do germânio nos compostos citados são, respectivamente:
Os elementos do bloco d da tabela periódica têm suas propriedades intermediárias entre
os elementos do bloco s e os do bloco p, o que explica a denominação para esses
elementos de metais de transição.
Sobre esses metais, assinale a alternativa INCORRETA.
O excesso em massa de iodeto de sódio (NaI) foi adicionado a 50 mL de uma solução de
AgNO3 e formou–se um precipitado de 1,5 g de AgI.
Nessas condições, é CORRETO afirmar que a concentração inicial da solução de AgNO3
é aproximadamente, de
O pentafluoreto de fósforo é um composto reativo que se
apresenta como gás incolor em pressão e temperatura ambiente.
As configurações eletrônicas das camadas mais externas dos
átomos de Flúor e Fósforo são, respectivamente, 2s2 2p5 e 3s2
3p3. Assim sendo, a estrutura do PF5 apresenta

