O estudo da Bioquímica tem por objetivo possibilitar a compreensão dos princípios básicos das biomoléculas, bem como suas interações intermoleculares responsáveis por manter o estado vital.Com relação à química das biomoléculas, leia as afirmativas a seguir:
I. Os aminoácidos apresentam em sua estrutura um grupo amino, um grupo carboxila, uma cadeia lateral (grupo R) e um hidrogênio ligados a um carbono. O que difere um aminoácido do outro é a cadeia lateral R.
II. As proteínas são biomoléculas resultantes da ligação de centenas de aminoácidos. A ligação entre dois aminoácidos é denominada de ligação glicosídica, onde o grupo carboxila de um aminoácido se liga ao grupo amino de outro.
III. Os carboidratos, de acordo com o tamanho e a organização molecular, são classificados em monossacarídeos, oligossacarídeos e polissacarídeos. Os oligossacarrdeos mais comuns são os dissacarídeos, como a maltose, que possui em sua estrutura uma molécula de glicose ligada a outra de fruto se.
IV. Os ácidos graxos são ácidos carboxnicos com cadeias hidrocarbonadas, classificados em saturados ou insaturados. Para a formação de um triglicerídeo, três ácidos graxos ligam-se a uma molécula de glicerol.
Assinale a alternativa que apresenta somente as afirmativas CORRETAS:
As enzimas são catalisadores biológicos que aumentam a velocidade das reações necessárias para a manutenção da vida. Os processos de digestão dos alimentos, envio de sinais nervosos e contração muscular, por exemplo, ocorreriam lentamente na ausência de catálise. As enzimas atuam proporcionando um ambiente específico adequado para que uma dada reação possa ocorrer mais rapidamente. Com relação ao estudo das enzimas, avalie as afirmativas a seguir e marque V para as verdadeiras e F para as falsas:
( ) Durante a reação o substrato liga-se em um fenda na estrutura da enzima, denominada sítio ativo.
( ) Para catalisar a reação, algumas enzimas necessitam de um componente adicional em sua estrutura, denominado de cofator se for uma molécula orgânica, ou de coenzima se for um íon inorgânico.
( ) As enzimas são classificadas de acordo com o tipo de reação que catalisam. As "transferases" participam de reações onde ocorre a transferência de elétrons.
( ) A velocidade de uma reação catalisada por enzimas aumenta com o aumento da concentração do substrato até que ocorra a saturação da enzima. Após a saturação, a velocidade da reação permanece constante.
( ) As enzimas possuem uma temperatura ótima de funcionamento, onde a velocidade da reação é máxima. Acima desta temperatura ocorre a desnaturação da enzima e, portanto, a diminuição da velocidade da reação.
Marque a opção que contenha a sequência CORRETA, de cima para baixo:
Em 1937 ocorreu o desastre do Hindenburg em Nova Jersey. O dirigível alemão, cheio de hidrogênio gasoso, foi destruído em um incêndio de grandes proporções. São dadas as seguintes proposições sobre o fenômeno.
I. Trata-se de uma reação exotérmica, na qual a energia de ativação é diretamente proporcional a quantidade de matéria presente, onde o total de entalpia liberada é igual ao produto da quantidade de matéria pelo volume total do dirigível.
II. A variação de entropia do sistema em questão (dirigível), ao entrar em combustão, é dado pela quantidade de calor produzida acrescida do trabalho realizado para expansão dos gases durante a explosão.
III. Considerando comportamento do hidrogênio como um gás ideal e a invariabilidade do volume do dirigível, antes da explosão não há realização de trabalho por parte do gás. São CORRETAS as alternativas:
Atualmente existe uma diversidade de técnicas analíticas para a se determinar a composição química, mineralógica e microestrutural de compostos orgânicos e inorgânicos. Com relação aos métodos instrumentais de análise marque V para as afirmativas verdadeiras e F, para as falsas.
( ) Os espectros de absorção de radiação no ultravioleta e no visível são um instrumento que pode ser usado para a identificação de compostos orgânicos insaturados e também na elucidação de suas estruturas.
( ) A difração de Raio-X usa a lei de Bragg para calcular a distância entre camadas atômicas em um cristal. Esta técnica é de grande interesse para identificação dos elementos químicos presentes em uma amostra e para obtenção de estruturas moleculares e cristalinas.
( ) A espectroscopia de energia dispersiva pode ser utilizada para a determinação qualitativa e quantitativa da composição de amostras sólidas e líquidas, esta usa o princípio de identificação pelo raio-X emitido através da interação inelástica do feixe eletrônico com a amostra.
( ) A fluorescência de Raio-X é uma técnica não destrutiva que envolve o uso da emissão de RaioX para se obter uma análise elementar quantitativa de materiais no estado sólido e Hquido.
( ) A cromatografia gasosa pode ser usada para análises qualitativas e quantitativas. Na cromatografia gás-líquido a fase móvel é um gás, enquanto a fase estacionária é um líquido retido na superfície de um sólido inerte por adsorção ou ligação química.
Assinale a alternativa que contém a sequência CORRETA de cima para baixo.
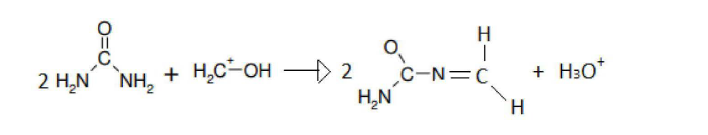
A síntese de resinas Ureia-Formaldeído para indústria madeireira é normalmente um processo conduzido em um mesmo reator. O mecanismo da reação de polimerização entre a ureia e o formaldeído envolve várias etapas. Uma das etapas está representada na equação abaixo:
Assinale a alternativa que contém a afirmação INCORRETA em relação as etapas e o processo de polimerização.
A decomposição do KClO 3 geralmente é usada para produzir pequenas quantidades de O2 no laboratório a partir da seguinte reação balanceada: 2KClO3 (s) → 2KCl (s)+3 O2 (g). Quantos gramas de O2, aproximadamente, podem ser preparados a partir de 9,0 g de KClO3?
Quando o benzeno é ingerido ou inalado, converte-se enzimaticamente em um:
Analise as afrmativas abaixo sobre Química Ambiental e assinale a alternativa correta: I. Água dura é água rica em sais de cálcio e magnésio, o que facilita a reação de saponifcação. II. Água deionizada é uma água da qual são retirados os componentes orgânicos e inorgânicos, inclusive metais pesados. III. DBO (Demanda Bioquímica de Oxigênio) é a quantidade de oxigênio necessária para oxidar a matéria orgânica biodegradável sob condições aeróbicas. Está correto o que se afrma em:
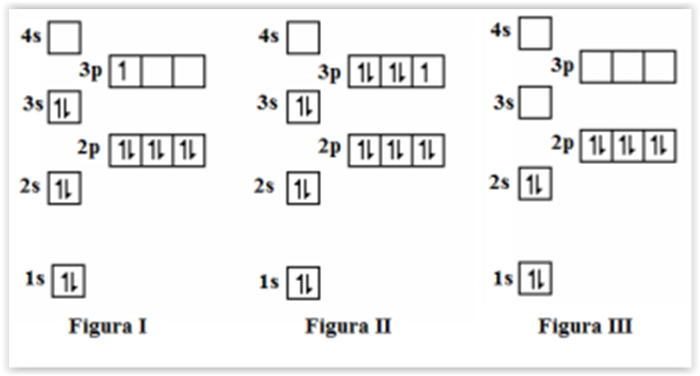
As figuras I, II e III, abaixo, representam as
configurações eletrônicas no estado fundamental de três
espécies químicas denominadas X, Y e Z,
respectivamente:
Com base na distribuição eletrônica apresentada,
assinalar a alternativa CORRETA:
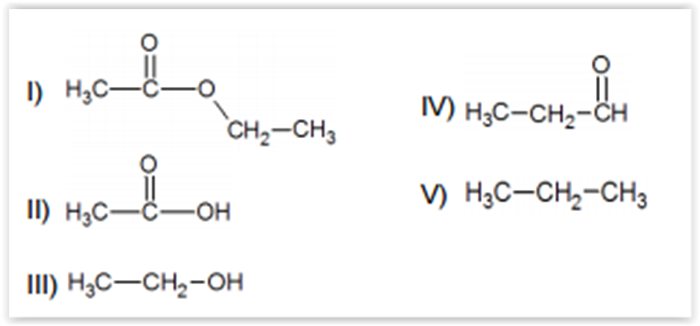
Considerando-se as estruturas abaixo, assinalar a
alternativa CORRETA:
A figura a seguir representa diluições de uma solução aquosa básica de Ca(OH)2 a partir da solução inicial A.
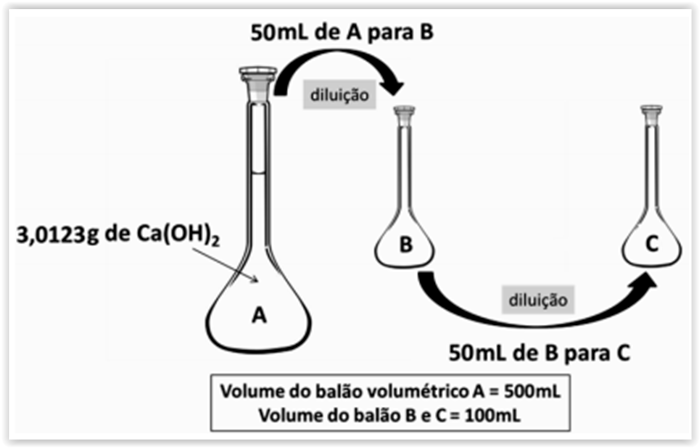
Entende-se que, após o preparo da solução A, coletou-se 50mL do frasco A para o frasco B, completando-o com água
destilada até que o menisco inferior do nível do líquido tangenciasse a linha de aferição do gargalo do balão. Após
homogeneização, coletou-se 50mL de B e passou-se para C, completando C com água destilada até a linha de aferição.
Diante do exposto, assinalar a alternativa CORRETA:
Dados: Ca = 40,078g/mol; O = 15,999g/mol; H = 1,008g/mol.
Com relação à segurança no laboratório, assinalar a alternativa CORRETA:
Com relação aos significados de mistura, molécula e substância, julgue os itens a seguir.
Molécula é a menor porção de um composto, com um
grupo variável de átomos ligados em um arranjo mutável
e eletricamente neutro.
Artefatos de aço inoxidável são resistentes à corrosão devido a um fenômeno conhecido como passivação, que é a
formação de uma fina camada de óxido de cromo na superfície, por ação do ar ou de oxidantes químicos. Sabendo-se que
o ácido nítrico (HNO3) na concentração de 1,6 mol/L pode ser usado como agente passivante, qual volume de HNO3
concentrado (em litros) deve ser utilizado para a obtenção de 100 L de solução passivante?
(Dados: MM(HNO3) = 63,0 g/mol; HNO3 concentrado: d = 1,40 g/mL; teor máximo = 65%(m/m))
O ácido fosfórico (H3PO4) de alta pureza é obtido por vIa seca ou térmica, pela combustão do fósforo elementar e posterior
hidratação do P2O5, de acordo com as reações abaixo:
Nesse pr°Cesso, de acordo com as equações acima, assinale a alternativa que apresenta a quantidade de calor liberado
na formação do H3PO4 (em kcal/mol).