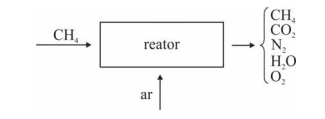
Em um reator ideal, de processo contínuo, que opera em
estado estacionário, a combustão de CH4 ocorre com uma
conversão de 90% do reagente limitante. Esse reator é alimentado
com CH4 e ar a taxas de 16 kg/h e 300 kg/h, respectivamente,
conforme ilustrado no esquema apresentado.
Considerando que, nessa situação, a combustão do CH4 seja
completa e que a composição do ar que alimenta o reator seja de
24%, em massa, de O2 (g) e, o restante, de N2 (g), julgue o item
subsequente.
A porcentagem, em massa, de CO2 na corrente de saída do
reator é superior a 10%.
Uma célula eletroquímica realiza a eletrólise de uma solução aquosa
de NaCR operando com uma corrente constante de 100,0 A e com
rendimento de 100% para a formação de Cl2. Considerando que a
massa molar do Cl2 seja igual a 70,9 g/mol e que a constante de
Faraday seja igual a 96.500 g/mol, julgue os próximos itens.
O tempo necessário para a formação de 709 g de Cl2, a partir
da eletrólise da solução aquosa de NaCL, é superior a 2 h.

Considerando que as reações de hidrogenação sejam exotérmicas,
que todos os gases envolvidos apresentem comportamento ideal e
que o produto da constante universal dos gases pela temperatura
absoluta (R×T) seja igual a 2.500 J/mol, julgue os itens que se
seguem.
A constante de equilíbrio para a reação de hidrogenação do
C2H4 (g) a 100 ºC é maior que a 25 ºC.
As bombas são máquinas que adicionam energia a uma corrente
fluida quando o escoamento é líquido ou pastoso. Com relação a
esses equipamentos, julgue os itens a seguir.
Para a escolha de uma bomba, deve–se considerar a
necessidade de vazão do fluido que se deseja transportar, além
de sua natureza e condições. A perda de carga a ser vencida
pelo bombeamento não interfere nessa escolha.
Com referência ao processo de filtração e a parâmetros relacionados
a esse processo, julgue os itens que se seguem.
Força motriz da filtração é a diferença de pressão que pode ser
causada por ação da gravidade (coluna hidrostática), força
centrífuga e aplicação de pressão ou vácuo.
A respeito de análise granulométrica e peneiramento, julgue os
próximos itens.
O peneiramento industrial de insumos sólidos garante a
manutenção da qualidade do produto final, contudo, no que se
refere ao tamanho de partícula do material que será
processado, pouco influencia o processo industrial e a
eficiência dos equipamentos de produção.
No que se refere a mecanismos de troca de calor, julgue os itens a
seguir.
A taxa de convecção de calor pode ser calculada com base na
temperatura do fluido em movimento, observada na distância
equivalente à espessura da camada limite turbulenta, sendo a
temperatura da superfície desconsiderada na equação de
transporte.
Acerca de trocadores de calor, julgue os itens que se seguem.
Os trocadores de calor são tipicamente classificados com base
nas suas características construtivas e no modo como os fluidos
escoam nesses aparelhos, que pode ser laminar ou turbulento.
Acerca dos processos físicos que ocorrem por difusão de massa,
julgue os itens seguintes.
Em geral, a conservação de massa total requer que o somatório
dos fluxos difusivos de todas as espécies seja maior que um.
O etileno ― o alceno mais simples e um dos mais importantes
produtos orgânicos fabricados industrialmente ― é utilizado na
síntese de polietileno, de etanol, de ácido acético e de outros
compostos. O polietileno é um dos polímeros mais versáteis
existentes no mercado. A respeito das matérias–primas e de aspectos
relacionados à produção de etileno (eteno) e de polietileno, julgue
os itens a seguir.
Na síntese de etileno, pode–se utilizar butano, que se decompõe
em dois radicais etila; cada um deles, ao perder um átomo de
hidrogênio, gera duas moléculas de etileno.
As estações de tratamento de água industrial ou potável têm a
finalidade de transformar a água denominada bruta em água própria
para uso na indústria ou em água potável para o consumo humano.
Acerca do tratamento de água, julgue os itens subsequentes.
A intensidade da turbidez da água depende da granulometria e
da concentração das partículas: partículas menores, em
concentrações elevadas, causam pequena turbidez, ao passo
que partículas grandes, nas mesmas concentrações, causam
maior turbidez.
Considerando que sistemas de controle de processo são utilizados
para assegurar a estabilidade e otimizar o desempenho econômico
desse processo, julgue os itens seguintes, relativos a instrumentação
e controle de processo.
O controle de temperatura de um líquido em um tanque pode
ser feito por meio de um manômetro, utilizado para medir a
temperatura, e de um controlador feedback, que usa o valor
medido de temperatura para avaliar o valor do desvio em
relação a um valor preestabelecido (set point).
Acerca da prova e do laudo pericial, julgue os próximos itens.
Em uma ação judicial na área cível, os meios de prova
admissíveis restringem–se àqueles que estão expressamente
previstos em lei, ou seja, a confissão, o depoimento pessoal, o
interrogatório, as testemunhas, os documentos, a perícia e a
inspeção judicial.
Uma empresa, diante da elevação dos preços da energia
elétrica e das descobertas de grandes reservas de gás de xisto nas
proximidades de suas instalações, resolveu investir na geração
própria de energia termoelétrica. O gás de xisto é composto
principalmente por metano (CH4), cuja equação de combustão é
CH4 (g) + 2O2 (g) –> CO2 (g) + 2H2O (l). A tabela a seguir mostra
os dados termodinâmicos, a 25 ºC, relativos aos compostos
envolvidos na equação apresentada.
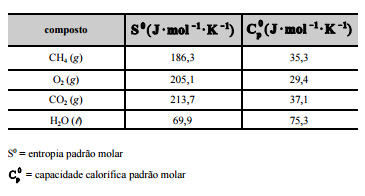
Com relação a essa situação hipotética, julgue os itens
subsequentes, considerando que a combustão do CH4 ocorra de
forma completa; que a entalpia padrão de combustão do CH4 (g), a
25 ºC, seja igual a –890 kJ/mol; e que as massas molares, em g/mol,
do C, do H e do O sejam iguais a 12,0, 1,0 e 16,0, respectivamente.
Se o consumo mensal de energia elétrica da referida empresa
for de 1,0 × 1012 J, a combustão do CH4 (g), sob pressão
constante de 1 bar e a 25 ºC, produzirá mais de 40 toneladas de
CO2 para suprir as necessidades mensais de energia da
empresa.
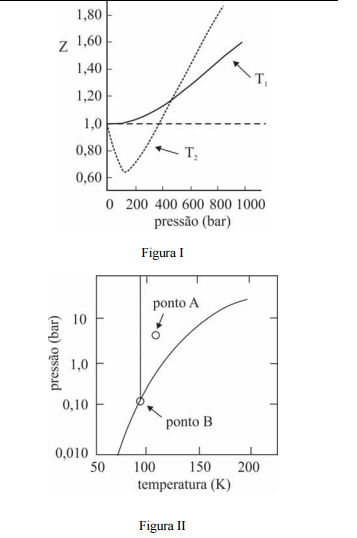
A figura I ilustra o gráfico do coeficiente de compressibilidade (Z)
do CH4 (g) em função da pressão para duas temperaturas distintas
(T1 e T2), e a figura II representa o diagrama de fases desse mesmo
composto. A partir das figuras apresentadas, julgue os itens que se
seguem.
Na temperatura e pressão correspondentes ao ponto A da
figura II, o potencial químico do metano gasoso é superior ao
do metano líquido.

