Assinale a alternativa que apresenta apenas compostos inorgânicos.
De acordo com o modelo de Rutheford-Bohr, assinale a alternativa correta.
No que tange aos sistemas biológicos, assinale a alternativa correta.
A natureza é repleta de fenômenos físicos e químicos. Esses fenômenos se diferenciam uma vez que fenômenos químicos sofrem alteração da constituição das substâncias envolvidas.
Assinale a alternativa que não representa um indício de um fenômeno químico:
A velocidade de uma reação química é a taxa de variação da concentração de reagentes e produtos em um determinado momento.
Vários fatores afetam as velocidades das reações, assinale a alternativa incorreta sobre os fatores que afetam a velocidade de uma reação:
Observe a pilha representada na imagem e baseado nos seus conhecimentos de eletroquímica julgue a veracidade das informações abaixo:
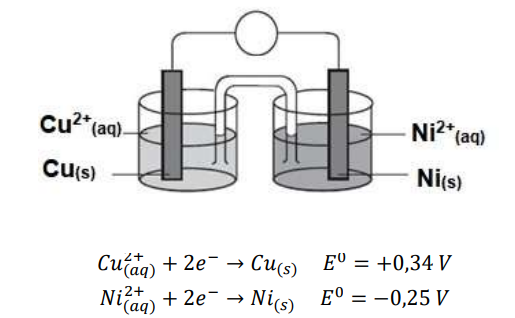
I. A região que sofre redução é o cátodo.
II. A placa de cobre que atua com ânodo e sofre corrosão.
III. O fluxo de elétrons do sistema vai da placa cobre para a placa de níquel
As afirmações verdadeiras são:
Julgue os itens a seguir, a respeito de soluções, densidade, concentração de soluções, diluição de soluções e volumetria.
Sabendo-se que um mol de bário pesa 56 g, um de oxigênio pesa 16 g e um de hidrogênio pesa 1 g, um litro de uma solução 0,2 mol/L de Ba(OH)2 contém 18 g dessa base.
No que concerne ao estado físico da matéria, julgue os itens subsequentes.
A entropia de uma mesma substância é maior em estado líquido do que em estado sólido.
No dia 15 de junho de 2022, os bombeiros de Maringá-PR fizeram um treinamento na Catedral Basílica Menor Nossa Senhora da Glória. Com formato cônico de diâmetro de 38 metros e altura de 114 metros, sustentando uma cruz de 10m perfazendo um total de 124m, a Catedral é o 10° monumento em altura do mundo. Durante o treinamento, os bombeiros desciam com o auxílio de uma corda com os pés em contato com a parede externa da edificação, com velocidade constante. Sendo a massa de um deles 75kg e considerando a aceleração da gravidade no local 9,8m/s2, determine a resultante das forças atuantes sobre o bombeiro durante a descida.
Analise as seguintes reações:
I. CH4 (g) + O2 (g) → CO2 (g) + H2O (g)
II. CaO (s) + CO2 (g) → CaCO3 (s)
III. PbCO3 (s) → PbO (s) + CO2 (g)
IV. 2N2 (g) + 3H2 (g) → 2NH3 (g)
V. Fe (s) + 2HCl (aq) → FeCl2 (aq) + H2 (g)
Assinale a alternativa que classifica corretamente a reação apresentada.
Os alimentos são ingeridos, digeridos e absorvidos por um conjunto de órgãos, que formam o sistema digestório.
Na ilustração a seguir, são mostrados alguns dos órgãos Adesse sistema.
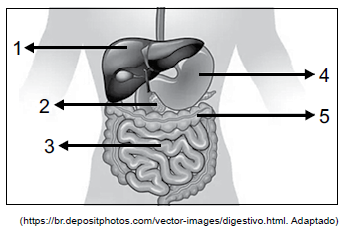
Sabe-se que o processo de digestão dos alimentos é realizado por diferentes enzimas presentes nas secreções produzidas pelos órgãos do sistema digestivo. No entanto, uma dessas secreções é desprovida de enzimas digestivas.
Esse é o caso da secreção produzida pelo órgão indicado pelo número
O ambiente de trabalho deve oferecer condições para o bem-estar físico e psíquico do trabalhador. Para isso, os equipamentos de proteção coletiva (EPC) visam proteger a todos os trabalhadores, expostos a determinados riscos. São exemplos de EPC:
O metanoato de sódio (HCOONa) é um composto utilizado na indústria para a obtenção do ácido fórmico (HCOOH) por meio de uma reação com ácido sulfúrico (H2SO4). A reação está apresentada abaixo.
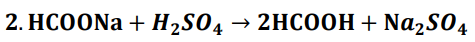
Uma solução aquosa foi preparada a partir da dissolução de 6,8 g de metanoato de sódio em 100 ml de água. Essa solução preparada reagiu com uma solução de ácido sulfúrico com centração de 0,2 mol/L para formação do ácido fórmico. Sabendo que a quantidade de solução de ácido sulfúrico foi a quantidade estequiométrica para completar a reação de síntese, a concentração da solução de metanoato de sódio preparada e a quantidade de solução de ácido sulfúrico adicionada, respectivamente, foram:
Massa molar: Na=23 g/mol; C=12 g/mol; O=16 g/mol; H=1 g/mol.
Considere a tabela de temperaturas de fusão (TF) e temperaturas de ebulição (TE) de algumas
substâncias hipotéticas, todas sujeitas às mesmas condições de pressão.
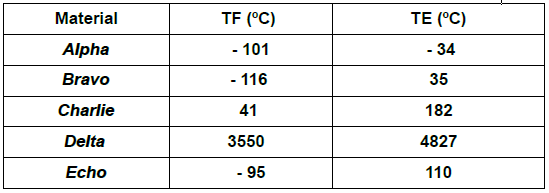
Acerca desta tabela e de seus dados, são feitas as seguintes afirmativas:
I – À temperatura de 25 ºC, o material Alpha está no estado sólido.
II – À temperatura de 50 ºC, os materiais Bravo e Delta estão no estado líquido.
III – À temperatura de 30 ºC, os materiais Charlie e Echo estão no estado gasoso.
IV – À temperatura de 145 ºC, os materiais Alpha, Bravo e Echo estão no estado gasoso.
V – À temperatura de 1450 ºC, o material Delta está no estado sólido.
Das afirmativas feitas, estão corretas apenas
Leia o texto a seguir e resolva a questão:

Atividades físicas intensas promovem a perda de água e de eletrólitos. Para repor essas perdas, soldados podem consumir um repositor hidroeletrolítico durante a atividade de campanha. Esses repositores são constituídos de uma solução aquosa contendo várias substâncias químicas, principalmente sais.
Considere um repositor que possua as seguintes especificações: cada porção de 200 mL contém 90 mg de íons sódio, 24 mg de íons potássio e 84 mg de íons cloreto. Baseado nestas informações, são feitas as seguintes afirmativas:
I) A concentração de íons sódio na solução é de 0,45 g L-1.
II) Cada litro do repositor possui aproximadamente 3,1 x 10-3 mol de íons potássio.
III) A temperatura de congelamento de uma porção de repositor é maior do que a temperatura de congelamento da água pura nas mesmas condições.
IV) Para se obter 0,2 mol de íons cloreto, seriam necessários aproximadamente 100 litros de repositor.
Das afirmativas feitas, estão corretas apenas

