À medida que aumenta a consciência sobre os impactos ambientais relacionados ao uso da energia, cresce a importância de se criar políticas de incentivo ao uso de combustíveis mais eficientes. Nesse sentido, considerando-se que o metano, o butano e o octano sejam representativos do gás natural, do gás liquefeito de petróleo (GLP) e da gasolina, respectivamente, então, a partir dos dados fornecidos, é possível concluir que, do ponto de vista da quantidade de calor obtido por mol de CO2 gerado, a ordem crescente desses três combustíveis é
A formação de chuva mais ou menos ácida depende não só da concentração do ácido formado, como também do tipo de ácido. Essa pode ser uma informação útil na elaboração de estratégias para minimizar esse problema ambiental. Se consideradas concentrações idênticas, quais dos ácidos citados no texto conferem maior acidez às águas das chuvas?
Uma medida que poderia contribuir para acabar definitivamente com o problema da poluição ambiental por metais pesados relatado no texto seria
A utilização de combustíveis fósseis interfere no ciclo do carbono, pois provoca
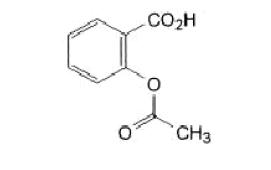
O ácido acetilsalicílico (AAS) é uma substância
utilizada como fármaco analgésico no alívio das dores
de cabeça. A figura abaixo é a representação
estrutural da molécula do AAS.
Considerando–se essa representação, é correto
afirmar que a fórmula molecular do AAS é
Os clorofluorcarbonetos (CFCs) são
substâncias formadas por moléculas que contêm
átomos de carbono, flúor e cloro. Descobertos em
1930, eram considerados uma maravilha, pois
substituíam, com grande eficiência, a amônia, utilizada
em refrigeradores. A amônia é tóxica e tem odor
desagradável, ao passo que os CFCs são inertes e
não causam problemas aos seres humanos.
Consequentemente, as fábricas de geladeiras
rapidamente passaram a utilizar os CFCs. No entanto,
em 1974, dois químicos — Mário Molina e Sherwood
Rowland — descobriram que esses gases reagiam
com o O3 da camada de ozônio, causando sérios
problemas ambientais e aos seres vivos.
O que pode ser feito para evitar problemas ambientais
devido à utilização dos clorofluorcarbonetos?
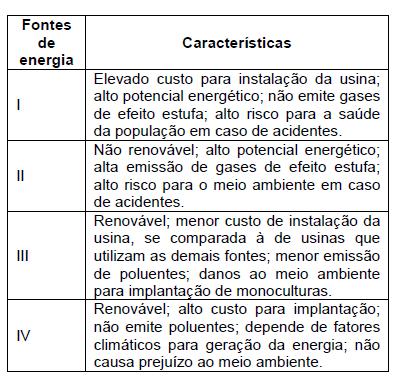
O quadro a seguir mostra algumas características de
diferentes fontes de energia.
No quadro, as características de I a IV, referem–se,
respectivamente, às seguintes fontes de energia:
O lixo radioativo ou nuclear é resultado da manipulação de materiais radioativos, utilizados hoje na agricultura, na indústria, na medicina, em pesquisas científicas, na produção de energia etc. Embora a radioatividade se reduza com o tempo, o processo de decaimento radioativo de alguns materiais pode levar milhões de anos. Por isso, existe a necessidade de se fazer um descarte adequado e controlado de resíduos dessa natureza. A taxa de decaimento radioativo é medida em termos de um tempo característico, chamado meia-vida, que é o tempo necessário para que uma amostra perca metade de sua radioatividade original. O gráfico seguinte representa a taxa de decaimento radioativo do rádio-226, elemento químico pertencente à família dos metais alcalinos terrosos e que foi utilizado durante muito tempo na medicina.
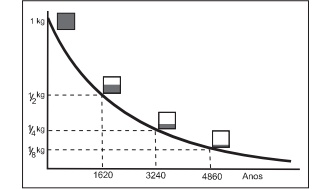
As informações fornecidas mostram que
De acordo com as considerações do texto, qual das moléculas apresentadas a seguir é a mais adequada para funcionar como molécula ativa de protetores solares?
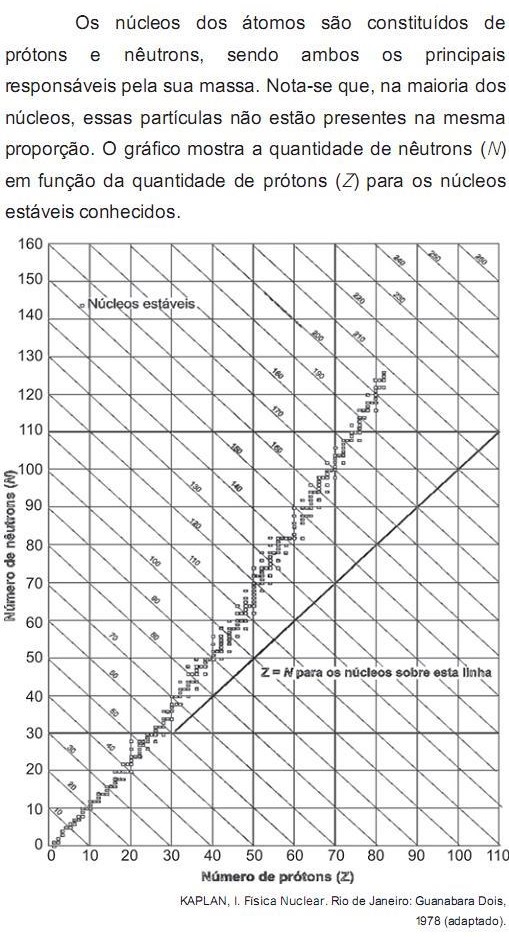
O antimônio é um elemento químico que possui 50 prótons e possui vários isótopos ? átomos que só se diferem pelo número de nêutrons. De acordo com o gráfico, os isótopos estáveis do antimônio possuem
As informações sobre obtenção e transformação dos recursos naturais por meio dos processos vitais de fotossíntese e respiração, descritas no texto, permitem concluir que

A Companhia de Tecnologia de Saneamento Ambiental do Estado de São Paulo (CETESB) divulga continuamente dados referentes à qualidade do ar na região metropolitana de São Paulo. A tabela apresentada corresponde a dados hipotéticos que poderiam ter sido obtidos pela CETESB em determinado dia. Se esses dados fossem verídicos, então, seria mais provável encontrar problemas de visibilidade
Duas matérias-primas encontradas em grande quantidade no Rio Grande do Sul, a quitosana, um biopolímero preparado a partir da carapaça do camarão, e o poliol, obtido do óleo do grão da soja, são os principais componentes de um novo material para incorporação de partículas ou princípios ativos utilizados no preparo de vários produtos. Este material apresenta viscosidade semelhante às substâncias utilizadas atualmente em vários produtos farmacêuticos e cosméticos, e fabricadas a partir de polímeros petroquímicos, com a vantagem de ser biocompatível e biodegradável. A fórmula estrutural da quitosana está apresentada em seguida.
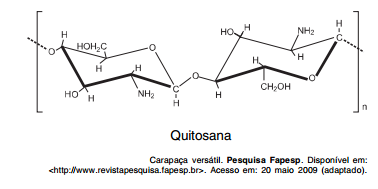
Com relação às características do material descrito, pode-se afirmar que
Pilhas e baterias são dispositivos tão comuns em nossa sociedade que, sem percebermos, carregamos vários deles junto ao nosso corpo; elas estão presentes em aparelhos de MP3, relógios, rádios, celulares etc. As semirreações descritas a seguir ilustram o que ocorre em uma pilha de óxido de prata.
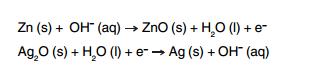
Pode-se afirmar que esta pilha
Considerando o texto, uma alternativa viável para combater o efeito estufa é