A China comprometeu-se a indenizar a Rússia
pelo derramamento de benzeno de uma indústria
petroquímica chinesa no rio Songhua, um afluente do rio
Amur, que faz parte da fronteira entre os dois países.
O presidente da Agência Federal de Recursos de Água da
Rússia garantiu que o benzeno não chegará aos dutos de
água potável, mas pediu à população que fervesse a água
corrente e evitasse a pesca no rio Amur e seus afluentes.
As autoridades locais estão armazenando centenas de
toneladas de carvão, já que o mineral é considerado eficaz
absorvente de benzeno.
Internet:
Levando-se em conta as medidas adotadas para a
minimização dos danos ao ambiente e à população, é
correto afirmar que
De acordo com a legislação brasileira, são tipos de água
engarrafada que podem ser vendidos no comércio para o
consumo humano:
- água mineral: água que, proveniente de fontes naturais
ou captada artificialmente, possui composição química ou
propriedades físicas ou físico-químicas específicas, com
características que lhe conferem ação medicamentosa;
- água potável de mesa: água que, proveniente de fontes
naturais ou captada artificialmente, possui características
que a tornam adequada ao consumo humano;
- água purificada adicionada de sais: água produzida
artificialmente por meio da adição à água potável de
sais de uso permitido, podendo ser gaseificada.
Com base nessas informações, conclui-se que
Ao beber uma solução de glicose (C6H12O6), um corta-cana
ingere uma substância
As florestas tropicais úmidas contribuem muito para a manutenção da vida no planeta, por meio do chamado seqüestro de carbono atmosférico. Resultados de observações sucessivas, nas últimas décadas, indicam que a floresta amazônica é capaz de absorver até 300 milhões de toneladas de carbono por ano. Conclui-se, portanto, que as florestas exercem importante papel no controle
Chuva ácida é o termo utilizado para designar precipitações com valores de pH inferiores a 5,6. As principais substâncias que contribuem para esse processo são os óxidos de nitrogênio e de enxofre provenientes da queima de combustíveis fósseis e, também, de fontes naturais. Os problemas causados pela chuva ácida ultrapassam fronteiras políticas regionais e nacionais. A amplitude geográfica dos efeitos da chuva ácida está relacionada principalmente com
O funcionamento de uma usina nucleoelétrica típica
baseia-se na liberação de energia resultante da divisão do
núcleo de urânio em núcleos de menor massa, processo
conhecido como fissão nuclear. Nesse processo, utiliza-se
uma mistura de diferentes átomos de urânio, de forma a
proporcionar uma concentração de apenas 4% de material
físsil. Em bombas atômicas, são utilizadas concentrações
acima de 20% de urânio físsil, cuja obtenção é trabalhosa,
pois, na natureza, predomina o urânio não-físsil.
Em grande parte do armamento nuclear hoje existente,
utiliza-se, então, como alternativa, o plutônio, material físsil
produzido por reações nucleares no interior do reator das
usinas nucleoelétricas. Considerando-se essas informações, é correto afirmar que
Para se obter 1,5 kg do dióxido de urânio puro, matériaprima para a produção de combustível nuclear, é necessário extrair-se e tratar-se 1,0 tonelada de minério. Assim, o rendimento (dado em % em massa) do tratamento do minério até chegar ao dióxido de urânio puro é de
Texto para as questões 17 e 18. Na investigação forense, utiliza-se luminol, uma substância que reage com o ferro presente na hemoglobina do sangue, produzindo luz que permite visualizar locais contaminados com pequenas quantidades de sangue, mesmo em superfícies lavadas. É proposto que, na reação do luminol (I) em meio alcalino, na presença de peróxido de hidrogênio (II) e de um metal de transição (Mn+), forma-se o composto 3-amino ftalato (III) que sofre uma relaxação dando origem ao produto final da reação (IV), com liberação de energia (hν) e de gás nitrogênio (N2). (Adaptado. Química Nova, 25, no 6, 2002. pp. 1003-1011.)
Na análise de uma amostra biológica para análise forense, utilizou-se 54 g de luminol e peróxido de hidrogênio em excesso, obtendo-se um rendimento final de 70%. Sendo assim, a quantidade do produto final (IV) formada na reação foi de
Texto para as questões 17 e 18. Na investigação forense, utiliza-se luminol, uma substância que reage com o ferro presente na hemoglobina do sangue, produzindo luz que permite visualizar locais contaminados com pequenas quantidades de sangue, mesmo em superfícies lavadas. É proposto que, na reação do luminol (I) em meio alcalino, na presença de peróxido de hidrogênio (II) e de um metal de transição (Mn+), forma-se o composto 3-amino ftalato (III) que sofre uma relaxação dando origem ao produto final da reação (IV), com liberação de energia (hν) e de gás nitrogênio (N2). (Adaptado. Química Nova, 25, no 6, 2002. pp. 1003-1011.)
Na reação do luminol, está ocorrendo o fenômeno de
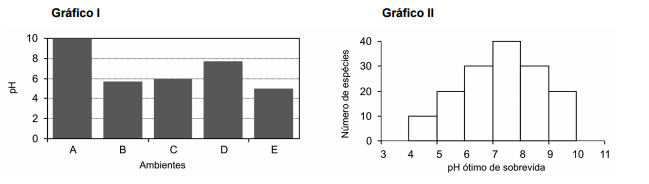
Um estudo caracterizou 5 ambientes aquáticos, nomeados de A a E, em uma região, medindo parâmetros físicoquímicos
de cada um deles, incluindo o pH nos ambientes. O Gráfico I representa os valores de pH dos 5 ambientes.
Utilizando o gráfico II, que representa a distribuição estatística de espécies em diferentes faixas de pH, pode-se
esperar um maior número de espécies no ambiente:
Na fabricação de qualquer objeto metálico, seja um parafuso, uma panela, uma jóia, um carro ou um foguete, a metalurgia está
presente na extração de metais a partir dos minérios correspondentes, na sua transformação e sua moldagem. Muitos dos
processos metalúrgicos atuais têm em sua base conhecimentos desenvolvidos há milhares de anos, como mostra o quadro:

Podemos observar que a extração e o uso de diferentes metais ocorreram a partir de diferentes épocas. Uma das razões para
que a extração e o uso do ferro tenham ocorrido após a do cobre ou estanho é
Há estudos que apontam razões econômicas e ambientais para que o gás natural possa vir a tornar-se, ao longo deste século, a
principal fonte de energia em lugar do petróleo. Justifica-se essa previsão, entre outros motivos, porque o gás natural
Em setembro de 1998, cerca de 10.000 toneladas de ácido sulfúrico (H2SO4) foram derramadas pelo navio Bahamas no litoral
do Rio Grande do Sul. Para minimizar o impacto ambiental de um desastre desse tipo, é preciso neutralizar a acidez resultante.
Para isso pode-se, por exemplo, lançar calcário, minério rico em carbonato de cálcio (CaCO3), na região atingida.
A equação química que representa a neutralização do H2SO4 por CaCO3, com a proporção aproximada entre as massas
dessas substâncias é:
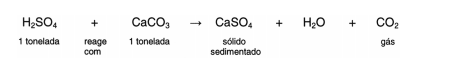
Pode-se avaliar o esforço de mobilização que deveria ser empreendido para enfrentar tal situação, estimando a quantidade de
caminhões necessária para carregar o material neutralizante. Para transportar certo calcário que tem 80% de CaCO3, esse
número de caminhões, cada um com carga de 30 toneladas, seria próximo de
Ferramentas de aço podem sofrer corrosão e enferrujar. As etapas químicas que correspondem a esses processos podem ser
representadas pelas equações:
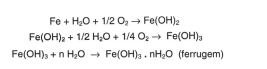
Uma forma de tornar mais lento esse processo de corrosão e formação de ferrugem é engraxar as ferramentas. Isso se justifica
porque a graxa proporciona
Os gases liberados pelo esterco e por alimentos em decomposição podem conter sulfeto de hidrogênio (H2S ), gás
com cheiro de ovo podre, que é tóxico para muitos seres vivos. Com base em tal fato, foram feitas as seguintes
afirmações:
I. Gases tóxicos podem ser produzidos em processos naturais;
II. Deve-se evitar o uso de esterco como adubo porque polui o ar das zonas rurais;
III. Esterco e alimentos em decomposição podem fazer parte no ciclo natural do enxofre (S ).
Está correto, apenas, o que se afirma em

