A chuva em locais não poluídos é levemente ácida. Em locais
onde os níveis de poluição são altos, os valores do pH da chuva
podem ficar abaixo de 5,5, recebendo, então, a denominação de
"chuva ácida". Este tipo de chuva causa prejuízos nas mais
diversas áreas: construção civil, agricultura, monumentos
históricos, entre outras.
A acidez da chuva está relacionada ao pH da seguinte forma:
concentração de íons hidrogênio = 10-pH , sendo que o pH pode
assumir valores entre 0 e 14
Ao realizar o monitoramento do pH da chuva em Campinas (SP)
nos meses de março, abril e maio de 1998, um centro de
pesquisa coletou 21 amostras, das quais quatro têm seus valores
mostrados na tabela:

A análise da fórmula e da tabela permite afirmar que:
I. da 6ª para a 14ª amostra ocorreu um aumento de 50% na
acidez.
II. a 18ª amostra é a menos ácida dentre as expostas.
III. a 8ª amostra é dez vezes mais ácida que a 14ª.
IV. as únicas amostras de chuvas denominadas ácidas são a
6ª e a 8ª.
São corretas apenas as afirmativas
Para testar o uso do algicida sulfato de cobre em tanques para criação de camarões, estudou-se, em aquário, a resistência
desses organismos a diferentes concentrações de íons cobre (representados por Cu2+). Os gráficos relacionam a mortandade
de camarões com a concentração de Cu2+ e com o tempo de exposição a esses íons.
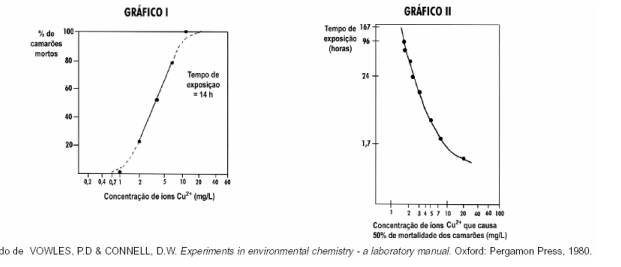
Se os camarões utilizados na experiência fossem introduzidos num tanque de criação contendo 20.000 L de água tratada com
sulfato de cobre, em quantidade suficiente para fornecer 50 g de íons cobre, estariam vivos, após 24 horas, cerca de
Comparando as características das quatro áreas de coleta às respectivas concentrações médias anuais de mercúrio nas
corvinas capturadas, pode-se considerar que, à primeira vista, os resultados
A tabela mostra a evolução da frota de veículos leves, e o gráfico, a emissão média do poluente monóxido de carbono (em
g/km) por veículo da frota, na região metropolitana de São Paulo, no período de 1992 a 2000

Comparando-se a emissão média de monóxido de carbono dos veículos a gasolina e a álcool, pode-se afirmar que
I. no transcorrer do período 1992-2000, a frota a álcool emitiu menos monóxido de carbono.
II. em meados de 1997, o veículo a gasolina passou a poluir menos que o veículo a álcool.
III. o veículo a álcool passou por um aprimoramento tecnológico.
É correto o que se afirma apenas em
Quando definem moléculas, os livros geralmente apresentam
conceitos como: "a menor parte da substância capaz de
guardar suas propriedades". A partir de definições desse tipo,
a idéia transmitida ao estudante é a de que o constituinte
isolado (moléculas) contém os atributos do todo.
É como dizer que uma molécula de água possui densidade,
pressão de vapor, tensão superficial, ponto de fusão, ponto
de ebulição, etc. Tais propriedades pertencem ao conjunto,
isto é, manifestam-se nas relações que as moléculas mantêm
entre si.
Adaptado de OLIVEIRA, R. J. O Mito da Substância. Química Nova na
Escola, n. º 1, 1995
O texto evidencia a chamada visão substancialista que ainda
se encontra presente no ensino da Química. Abaixo estão
relacionadas algumas afirmativas pertinentes ao assunto.
I. O ouro é dourado, pois seus átomos são dourados.
II. Uma substância "macia" não pode ser feita de moléculas
"rígidas".
III. Uma substância pura possui pontos de ebulição e fusão
constantes, em virtude das interações entre suas
moléculas.
IV. A expansão dos objetos com a temperatura ocorre
porque os átomos se expandem.
Dessas afirmativas, estão apoiadas na visão substancialista
criticada pelo autor apenas
O Protocolo de Kyoto — uma convenção das Nações Unidas que
é marco sobre mudanças climáticas, — estabelece que os países
mais industrializados devem reduzir até 2012 a emissão dos
gases causadores do efeito estufa em pelo menos 5% em
relação aos níveis de 1990. Essa meta estabelece valores
superiores ao exigido para países em desenvolvimento. Até
2001, mais de 120 países, incluindo nações industrializadas da
Europa e da Ásia, já haviam ratificado o protocolo. No entanto,
nos EUA, o presidente George W. Bush anunciou que o país não
ratificaria "Kyoto", com os argumentos de que os custos
prejudicariam a economia americana e que o acordo era pouco
rigoroso com os países em desenvolvimento.
Adaptado do Jornal do Brasil, 11/04/2001
Na tabela encontram-se dados sobre a emissão de CO2
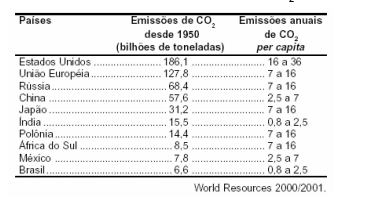
Considerando os dados da tabela, assinale a alternativa que
representa um argumento que se contrapõe à justificativa dos
EUA de que o acordo de Kyoto foi pouco rigoroso com países em
desenvolvimento.
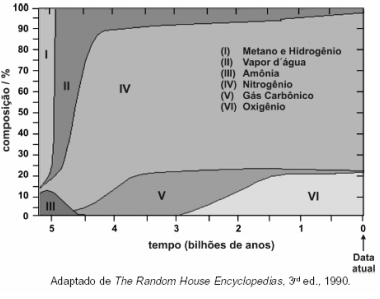
No que se refere à composição em volume da atmosfera terrestre há 2,5 bilhões de anos, pode-se afirmar que o volume de oxigênio, em valores percentuais, era de, aproximadamente,
Considere os seguintes acontecimentos ocorridos no Brasil:
- Goiás, 1987 - Um equipamento contendo césio radioativo, utilizado em medicina
nuclear, foi encontrado em um depósito de sucatas e aberto por pessoa que
desconhecia o seu conteúdo. Resultado: mortes e conseqüências ambientais sentidas
até hoje.
- Distrito Federal, 1999 - Cilindros contendo cloro, gás bactericida utilizado em
tratamento de água, encontrados em um depósito de sucatas, foram abertos por pessoa
que desconhecia o seu conteúdo. Resultado: mortes, intoxicações e conseqüências
ambientais sentidas por várias horas.
Para evitar que novos acontecimentos dessa natureza venham a ocorrer, foram feitas as
seguintes propostas para a atuação do Estado:
I. Proibir o uso de materiais radioativos e gases tóxicos.
II. Controlar rigorosamente a compra, uso e destino de materiais radioativos e de
recipientes contendo gases tóxicos.
III. Instruir usuários sobre a utilização e descarte destes materiais.
IV. Realizar campanhas de esclarecimentos à população sobre os riscos da radiação e da
toxicidade de determinadas substâncias.
Dessas propostas, são adequadas apenas
Atualmente, sistemas de purificação de emissões poluidoras estão sendo exigidos por lei em
um número cada vez maior de países. O controle das emissões de dióxido de enxofre
gasoso, provenientes da queima de carvão que contém enxofre, pode ser feito pela reação
desse gás com uma suspensão de hidróxido de cálcio em água, sendo formado um produto
não poluidor do ar.
A queima do enxofre e a reação do dióxido de enxofre com o hidróxido de cálcio, bem como
as massas de algumas das substâncias envolvidas nessas reações, podem ser assim
representadas:
enxofre (32 g) + oxigênio (32 g) → dióxido de enxofre (64 g)
dióxido de enxofre (64 g) + hidróxido de cálcio (74 g) → produto não poluidor
Dessa forma, para absorver todo o dióxido de enxofre produzido pela queima de uma
tonelada de carvão (contendo 1% de enxofre), é suficiente a utilização de uma massa de
hidróxido de cálcio de, aproximadamente,
Algumas atividades humanas interferiram significativamente no ciclo natural do enxofre,
alterando as quantidades das substâncias indicadas no esquema. Ainda hoje isso ocorre,
apesar do grande controle por legislação.
Pode-se afirmar que duas dessas interferências são resultantes da
Numa rodovia pavimentada, ocorreu o tombamento de um caminhão que transportava ácido
sulfúrico concentrado. Parte da sua carga fluiu para um curso d'água não poluído que deve
ter sofrido, como conseqüência,
I. mortandade de peixes acima da normal no local do derrame de ácido e em suas
proximidades.
II. variação do pH em função da distância e da direção da corrente de água.
III. danos permanentes na qualidade de suas águas.
IV. aumento momentâneo da temperatura da água no local do derrame.
É correto afirmar que, dessas conseqüências, apenas podem ocorrer
O ciclo representado mostra que a atmosfera, a litosfera, a hidrosfera e a biosfera,
naturalmente,
I. são poluídas por compostos de enxofre.
II. são destinos de compostos de enxofre.
III. transportam compostos de enxofre.
IV. são fontes de compostos de enxofre.
Dessas afirmações, estão corretas, apenas,
Pelas normas vigentes, o litro do álcool hidratado que abastece os veículos deve ser
constituído de 96% de álcool puro e 4% de água (em volume). As densidades desses
componentes são dadas na tabela.

A partir desses dados, o técnico pôde concluir que estavam com o combustível adequado
somente os postos
Uma região industrial lança ao ar gases como o dióxido de enxofre e óxidos de nitrogênio,
causadores da chuva ácida. A figura mostra a dispersão desses gases poluentes.

Considerando o ciclo da água e a dispersão dos gases, analise as seguintes possibilidades:
I. As águas de escoamento superficial e de precipitação que atingem o manancial
poderiam causar aumento de acidez da água do manancial e provocar a morte de
peixes.
II. A precipitação na região rural poderia causar aumento de acidez do solo e exigir
procedimentos corretivos, como a calagem.
III. A precipitação na região rural, embora ácida, não afetaria o ecossistema, pois a
transpiração dos vegetais neutralizaria o excesso de ácido.
Dessas possibilidades,
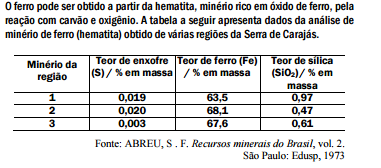
No processo de produção do ferro, a sílica é removida do minério por reação
com calcário (CaCO3). Sabe-se, teoricamente (cálculo estequiométrico), que
são necessários 100 g de calcário para reagir com 60 g de sílica.
Dessa forma, pode-se prever que, para a remoção de toda a sílica presente em
200 toneladas do minério na região 1, a massa de calcário necessária é,
aproximadamente, em toneladas, igual a: