O flúor é usado de forma ampla na prevenção de
cáries. Por reagir com a hidroxiapatita [Ca10(PO4)6(OH)2] presente nos esmaltes dos dentes, o flúor forma a
fluorapatita [Ca10(PO4)6F2], um mineral mais resistente
ao ataque ácido decorrente da ação de bactérias
específicas presentes nos açúcares das placas que
aderem aos dentes.
Disponível em: http://www.odontologia.com.br. Acesso em: 27 jul. 2010 (adaptado).
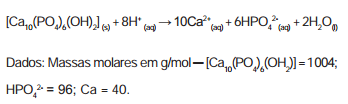
A reação de dissolução da hidroxiapatita é:
Supondo–se que o esmalte dentário seja constituído
exclusivamente por hidroxiapatita, o ataque ácido que
dissolve completamente 1 mg desse material ocasiona
a formação de, aproximadamente,
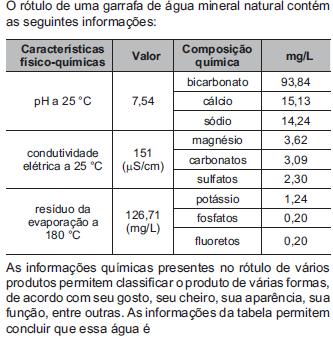


Todos os organismos necessitam de água e grande parte deles vive em rios, lagos e oceanos. Os processos bio - lógicos, como respiração e fotossíntese, exercem profunda influência na química das águas naturais em todo o planeta. O oxigênio é ator dominante na química e na bioquímica da hidrosfera. Devido a sua baixa solubilidade em água (9,0 mg/l a 20ºC) a disponibilidade de oxigênio nos ecossistemas aquáticos estabelece o limite entre a vida aeróbica e anaeróbica. Nesse contexto, um parâmetro chamado Demanda Bioquímica de Oxigênio (DBO) foi definido para medir a quantidade de matéria orgânica presente em um sistema hídrico. A DBO corresponde à massa de O2 em miligramas necessária para realizar a oxidação total do carbono orgânico em um litro de água.
BAIRD, C. Química Ambiental. Ed. Bookman, 2005 (adaptado).
Dados: Massas molares em g/mol: C = 12; H = 1; O = 16.
Suponha que 10 mg de açúcar (fórmula mínima CH2O e massa molar igual a 30 g/mol) são dissolvidos em um litro de água; em quanto a DBO será aumentada?

O Brasil é um dos países que obtêm melhores resultados na reciclagem de latinhas de alumínio. O esquema a seguir
representa as várias etapas desse processo:

A temperatura do forno em que o alumínio é fundido é útil também porque
Às vezes, ao abrir um refrigerante, percebe–se que uma
parte do produto vaza rapidamente pela extremidade do
recipiente. A explicação para esse fato está relacionada à
perturbação do equilíbrio químico existente entre alguns
dos ingredientes do produto, de acordo com a equação:
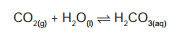
A alteração do equilíbrio anterior, relacionada ao
vazamento do refrigerante nas condições descritas, tem
como consequência a
O pH do solo pode variar em uma faixa significativa
devido a várias causas. Por exemplo, o solo de áreas com
chuvas escassas, mas com concentrações elevadas do
sal solúvel carbonato de sódio (Na2CO3), torna–se básico
devido à reação de hidrólise do íon carbonato, segundo
o equilíbrio:

Esses tipos de solos são alcalinos demais para fins
agrícolas e devem ser remediados pela utilização de
aditivos químicos.
BAIRD, C. Química ambiental. São Paulo: Artmed, 1995 (adaptado).
Suponha que, para remediar uma amostra desse tipo
de solo, um técnico tenha utilizado como aditivo a cal
virgem (CaO). Nesse caso, a remediação
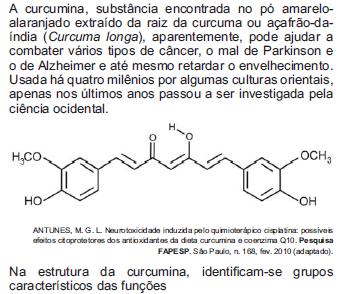
A curcumina, substância encontrada no pó amareloalaranjado
extraído da raiz da curcuma ou açafrão–da–
índia (Curcuma longa), aparentemente, pode ajudar a
combater vários tipos de câncer, o mal de Parkinson e
o de Alzheimer e até mesmo retardar o envelhecimento.
Usada há quatro milênios por algumas culturas orientais,
apenas nos últimos anos passou a ser investigada pela
ciência ocidental.
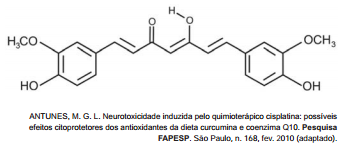
Na estrutura da curcumina, identificam–se grupos
característicos das funções
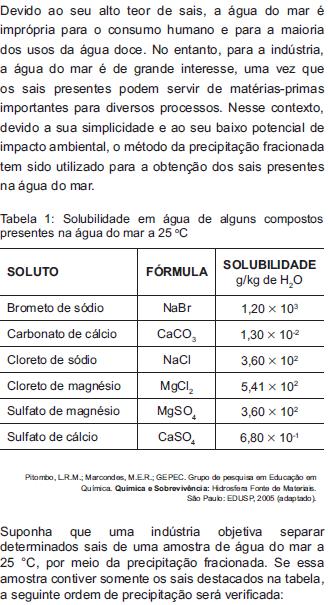
Devido ao seu alto teor de sais, a água do mar é
imprópria para o consumo humano e para a maioria
dos usos da água doce. No entanto, para a indústria,
a água do mar é de grande interesse, uma vez que
os sais presentes podem servir de matérias–primas
importantes para diversos processos. Nesse contexto,
devido a sua simplicidade e ao seu baixo potencial de
impacto ambiental, o método da precipitação fracionada
tem sido utilizado para a obtenção dos sais presentes
na água do mar.
Tabela 1: Solubilidade em água de alguns compostos
presentes na água do mar a 25ºC
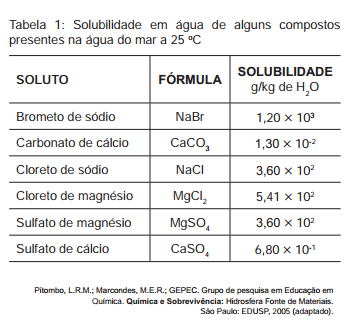
Suponha que uma indústria objetiva separar
determinados sais de uma amostra de água do mar a
25 ºC, por meio da precipitação fracionada. Se essa
amostra contiver somente os sais destacados na tabela,
a seguinte ordem de precipitação será verificada: