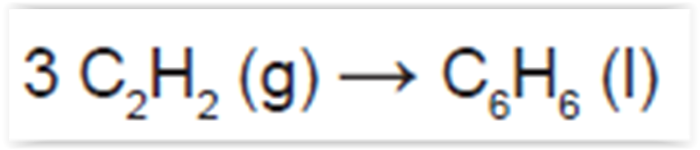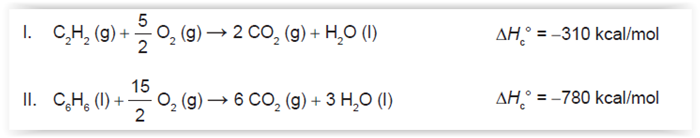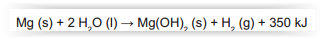O carro flex é uma realidade no Brasil. Estes veículos estão equipados com motor que tem a capacidade de funcionar com mais de um tipo de combustível. No entanto, as pessoas que têm esse tipo de veículo, na hora do abastecimento, têm sempre a dúvida: álcool ou gasolina? Para avaliar o consumo desses combustíveis, realizou-se um percurso com um veículo flex, consumindo 40 litros de gasolina e no percurso de volta utilizou-se etanol. Foi considerado o mesmo consumo de energia tanto no percurso de ida quanto no de volta.
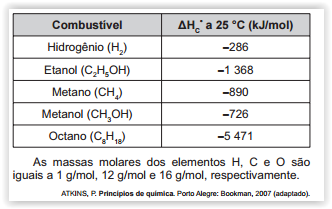
O quadro resume alguns dados aproximados sobre esses combustíveis.
O volume de etanol combustível, em litro, consumido no percurso de volta é mais próximo de
No que se refere à termoquímica, a reações exotérmicas e endotérmicas e à variação de entalpia, julgue o item a seguir.
A termoquímica é o ramo da química sobre a relação entre calor e transformações químicas. A quantidade de calor liberado ou absorvido em um sistema reagente depende da natureza da reação, das quantidades dos reagentes e das condições impostas na mistura reagente.
Na oxidação de 1,0 grama de glicose, a energia obtida para atividade muscular, em quilojoule, é mais próxima de
O metanol líquido pode ser obtido a partir da reação de síntese entre monóxido de carbono e gás hidrogênio. As entalpias de formação das substâncias citadas são, respectivamente, -238,4 kJ.mol-1 e -110,5 kJ.mol-1 .
O valor da variação de entropia da vizinhança desse sistema a 25°C, em J.K-1, é:
No que se refere à termoquímica, a reações exotérmicas e endotérmicas e à variação de entalpia, julgue o item a seguir.
Um processo endotérmico ocorre com absorção de calor (ΔH < 0), como, por exemplo, no processo de congelamento da água. Um processo exotérmico ocorre com liberação de calor (ΔH > 0), como, por exemplo, no processo de vaporização da água.
No que se refere à termoquímica, a reações exotérmicas e endotérmicas e à variação de entalpia, julgue o item a seguir.
Quando uma reação química se realiza à pressão constante, a quantidade de calor liberado ou absorvido é expressa pela variação da entalpia do sistema. Seu sinal algébrico indica se a reação é endotérmica ou exotérmica.
Assinale a opção correta com relação a soluções, termoquímica e cinética química.
Termoquímica é o ramo da química que estuda os calores de reações e a energia envolvida em transformações químicas. A partir dessa informação, considerem‐se as duas equações químicas a seguir, que representam a reação de combustão do metano, com dois diferentes conjuntos de produtos, em que são indicadas as respectivas variações de entalpia (ΔH).
Assinale a alternativa que apresenta a relação entre essas variações de entalpia.
Acerca da termoquímica, da espontaneidade de reações e da
ação de catalisadores, julgue os itens a seguir.
Um processo é espontâneo se é acompanhado por uma diminuição na entropia total do sistema e das vizinhanças. Dessa forma, os processos espontâneos à temperatura e pressão constantes são acompanhados por um aumento da energia livre, ou seja, a direção da mudança espontânea é a direção do aumento da energia livre.
Acerca da termoquímica, da espontaneidade de reações e da
ação de catalisadores, julgue os itens a seguir.
Pela Lei de Hess, uma entalpia de reação é a soma das entalpias de qualquer sequência de reações, quando realizadas nas mesmas condições de temperatura e pressão, em que a reação total pode ser dividida.
O ferro é encontrado na natureza na forma de seus minérios, tais como a hematita (α-Fe2O3)' a magnetita (Fe3O4) e a wustita (FeO). Na siderurgia, o ferro-gusa é obtido pela fusão de minérios de ferro em altos fornos em condições adequadas. Uma das etapas nesse processo é a formação de monóxido de carbono.O CO (gasoso) é utilizado para reduzir o FeO (sólido), conforme a equação química:
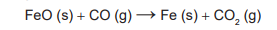
Considere as seguintes equações termoquímicas:
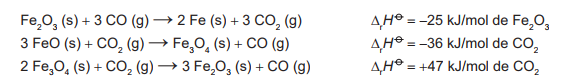
O valor mais próximo de Δt H , em kJ/mol de FeO, para a reação indicada do FeO (sólido) com o CO (gasoso) é
, em kJ/mol de FeO, para a reação indicada do FeO (sólido) com o CO (gasoso) é
Os combustíveis de origem fóssil, como o petróleo e o gás natural, geram um sério problema ambiental, devido à liberação de dióxido de carbono durante o processo de combustão. O quadro apresenta as massas molares e as reações de combustão não balanceadas de diferentes combustíveis.
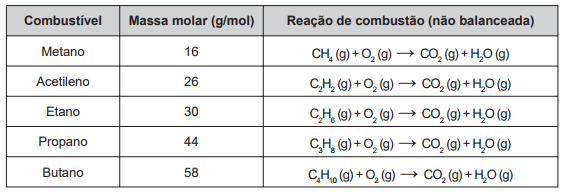
Considerando a combustão completa de 58 g de cada um dos combustíveis listados no quadro, a substância que emite mais CO2 é o
Para comparara eficiência de diferentes combustíveis, costuma-se determinar a quantidade de calor liberada na combustão por mal ou grama de combustível. O quadro mostra o valor de energia liberada na combustão completa de alguns combustíveis.
Qual combustível apresenta maior liberação de energia por grama?
O benzeno, um importante solvente para a indústria química, é obtido industrialmente pela destilação do
petróleo. Contudo, também pode ser sintetizado pela trimerização do acetileno catalisada por ferro metálico sob altas
temperaturas, conforme a equação química:
A energia envolvida nesse processo pode ser calculada indiretamente pela variação de entalpia das reações de
combustão das substâncias participantes, nas mesmas condições experimentais:
A variação de entalpia do processo de trimerização, em kcal, para a formação de um mol de benzeno é mais próxima de
Atualmente, soldados em campo, seja em treinamento ou em combate, podem aquecer suas refeições, prontas e embaladas em bolsas plásticas, utilizando aquecedores químicos, sem precisar fazer fogo. Dentro dessas bolsas existe magnésio metálico em pó e, quando o soldado quer aquecer a comida, ele coloca água dentro da bolsa, promovendo a reação descrita pela equação química:
O aquecimento dentro da bolsa ocorre por causa da