Considerando-se uma reação de ordem zero e uma de primeira ordem, se ao se dobrar a quantidade de reagentes, respectivamente, a consequência é que
Com relação à velocidade de reação química, a fatores que a influenciam e a assuntos correlatos, julgue o item a seguir.
A velocidade de uma reação química depende, essencialmente, do número total de colisões por unidade de tempo entre as partículas (átomos,moléculas ou íons) das espécies que participam da reação, bem como da fração de tais colisões que, efetivamente, promove a reação química.
Os alquenos são matéria-prima de grande importância na indústria porque podem ser facilmente transformados em uma vasta gama de compostos químicos. Exemplos típicos são as reações de hidratação e de polimerização catalisadas por ácido. Com relação às reações de alquenos, julgue o item subsequente.
Se a reação de desidratação de um alqueno ocorre de acordo com uma cinética de pseudoprimeira ordem, então o gráfico da concentração do alqueno em função do tempo terá aspecto conforme indicado no gráfico a seguir.
Do ponto de vista prático, mais importante que a velocidade das reações químicas, tradicionalmente estudadas na cinética química, é a velocidade dos processos que incluem, além da reação química, outras condições, como, por exemplo, a velocidade de difusão dos reagentes até o locus de reação. Nesse contexto, a Figura 1 mostra o gráfico da combustão da vela n.º 1 (11 gramas e 2 cm de raio), que apresenta o tempo de consumo em ambiente aberto (com circulação de ar) e fechado (sem circulação de ar) e a regressão linear para ambos os ambientes. A Figura 2 apresenta o gráfico do processo de combustão em ambiente aberto e fechado e a regressão linear de ambos os ambientes para a vela n.º 3 (17 gramas e 2 cm de raio).
Acerca da variação na velocidade de queima das velas, assinale a alternativa correta.
Com relação à velocidade de reação química, a fatores que a influenciam e a assuntos correlatos, julgue o item a seguir.
A velocidade de uma reação química é calculada pela multiplicação da variação de concentração de uma substância pelo intervalo de tempo em que a variação considerada ocorre, levando em conta o coeficiente estequiométrico da substância.
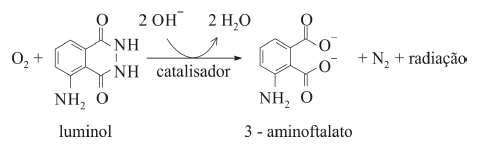
O composto conhecido como luminol é empregado para a detecção de sangue em perícias criminais. Em meio básico, em presença de peróxido de hidrogênio (H 2O2) e de um catalisador adequado, o luminol é oxidado ao ânion 3-aminoftalato, o qual é obtido inicialmente em um estado excitado, mas que rapidamente libera o excesso de energia emitindo radiação na faixa do azul.
A oxidação do luminol é realizada pelo O 2 (g) formado a partir da decomposição do peróxido de hidrogênio (H2O2), de acordo com a equação:
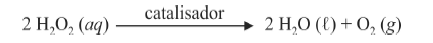
Sem a presença de um catalisador, a decomposição em questão é bastante lenta. Entretanto, o ferro presente na hemoglobina do sangue catalisa a decomposição e o O 2 (g) formado rapidamente oxida o luminol, ocasionando a característica luminescência azul.
Com relação à reação apresentada e às espécies nela envolvidas, e considerando a primeira constante de ionização ácida do H 2O2 igual a 2,4 × 10-12, julgue o item a seguir.
A quantidade de calor liberada por mol de moléculas de H2O2 decompostas é maior na reação realizada em presença do catalisador do que na reação não catalisada.
Qual a diferença entre o tempo de meia vida de uma reação de primeira ordem e de segunda ordem?
Bebidas podem ser refrigeradas de modo mais rápido utilizando-se caixas de isopor contendo gelo e um pouco de sal grosso comercial. Nesse processo ocorre o derretimento do gelo com consequente formação de líquido e resfriamento das bebidas. Uma interpretação equivocada, baseada no senso comum, relaciona esse efeito à grande capacidade do sal grosso de remover calor do gelo. Do ponto de vista científico, o resfriamento rápido ocorre em razão da
Os alquenos são matéria-prima de grande importância na indústria porque podem ser facilmente transformados em uma vasta gama de compostos químicos. Exemplos típicos são as reações de hidratação e de polimerização catalisadas por ácido. Com relação às reações de alquenos, julgue o item subsequente.
De acordo com a teoria das colisões, um aumento na temperatura de reação ocasiona aumento no número total de colisões entre as espécies reagentes e na fração de colisões efetivas.
Com relação à velocidade de reação química, a fatores que a influenciam e a assuntos correlatos, julgue o item a seguir.
Catalisador é a substância ou espécie que aumenta a velocidade de reação, não é consumida e fornece um mecanismo alternativo de baixa energia de ativação para a reação. Um catalisador é capaz de afetar a constante de equilíbrio da reação considerada, por modificar a velocidade da reação direta, aumentando o tempo requerido para o estabelecimento do equilíbrio.
Assinale a opção correta com relação a soluções, termoquímica e cinética química.
Os alquenos são matéria-prima de grande importância na indústria porque podem ser facilmente transformados em uma vasta gama de compostos químicos. Exemplos típicos são as reações de hidratação e de polimerização catalisadas por ácido. Com relação às reações de alquenos, julgue o item subsequente.
O efeito da adição do catalisador ácido é o de reduzir a energia de ativação da reação e, com isso, aumentar a fração de colisões efetivas.
A reação entre metanol e ácido bromídrico segue o seguinte mecanismo:
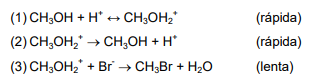
A partir deste mecanismo, indique a alternativa que apresenta a lei de velocidade de formação do brometo de metila, d[CH3Br]/dt, por meio da citada reação.
Se a taxa de formação de gás nitrogênio no enchimento de um airbag é de 156,8 L (nas CNTP) a cada vigésimo de segundo, a taxa de consumo de azoteto de sódio, aproximadamente em mols por segundo, de acordo com a seguinte reação 2NaN3(s) → 2Na(s) + 3N2(g) é
A velocidade é constante e não depende da concentração dos reagentes. Não existe uma relação direta entre os coeficientes e a ordem da reação. Essas são características cinéticas de reação de