O uso crescente de fibras ópticas para a construção de redes de
telecomunicações em banda larga levou a avanços consideráveis
na tecnologia da fabricação de vidros (...). Os vidros têm estrutura
em rede baseada em um óxido de ametal, normalmente a sílica
(SiO2), fundida juntamente com óxidos de metais que agem como
“modificadores de rede" e alteram o arranjo das ligações do
sólido (...). O vidro resiste ao ataque da maior parte dos
reagentes. Entretanto, a sílica do vidro reage com ácido
fluorídrico para formar íons fluoro‐silicatos:

Na reação apresentada
Os óxidos de nitrogênio são os componentes principais das
névoas, um fenômeno ao qual os habitantes das grandes cidades
estão habituados. O óxido nítrico forma‐se em pequenas
quantidades nos cilindros de combustão interna dos motores
pela combinação direta de nitrogênio e oxigênio:
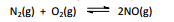
A constante de equilíbrio para essa reação aumenta de
aproximadamente 10–15 a 300K para cerca de 0,05 a 2400 K
(temperatura aproximada no cilindro de um motor em
funcionamento).
Com relação à reação entre o gás nitrogênio e o gás oxigênio,
assinale a afirmativa correta.
A água contendo uma concentração relativamente alta de íons Ca2+, Mg2+ e outros cátions divalentes é chamada de água dura. Em alguns lugares é necessário que se realize o abrandamento da água para evitar depósitos indesejáveis de sais insolúveis em sistemas de água quente. O abrandamento da água pode ser realizado por troca iônica. Este método consiste em fazer a água dura passar por um leito de resina de troca iônica que pode ser constituída por pérolas de plástico com grupos aniônicos do tipo fosfato. Essa resina captura os íons Ca2+ e Mg2+, substituindo‐os por íons que formarão compostos solúveis. O fosfato utilizado nesse tipo de resina tem como cátion
Alumínio metálico pode ser produzido eletroliticamente pelo processo Hall-Heroult em que o A603 é dissolvido em criolita fundida, Na3AiF6.
Nesse processo o Ion alumínio é reduzido a alumínio metálico e o ion 02 é oxidado a 02, que reage com os anodos de carbono gerando CO2.
A massa de aluminio obtida nessa eletrolise por uma corrente de 8,0A durante 3 horas e 20 minutos e rendimento de 100%, é de:
Dados: Massa molar (g.mor-1): Ai= 27 1F = 96500C
As etapas de tratamento da água de um município, que
apresenta dureza elevada, estão relacionadas a seguir.
I.Aeração e remoção de solutos voláteis;
II.Adição de óxido de cálcio;
III.Decantação em decantador primário;
IV.Coagulação com a adição de sulfato de ferro (III) e sulfato de
alumínio;
V.Cloração e filtração.
De acordo com essas etapas, o sulfeto de hidrogênio, o metano e
o metanotiol são retirados na etapa:
Um químico analisou uma amostra pura de um monoálcool
saturado que apresentou temperatura de ebulição 118C, massa
molar igual a 74 g.mol–1 e reagiu com dicromato de potássio em
meio ácido produzindo um ácido carboxílico. O espectro de
massas deste composto apresentou o pico do íon molecular
pouco intenso, os picos de maiores abundâncias relativas
apresentaram m/z em 56, 43, 41 e 31. Não foram observados
picos em m/z 59 e m/z 15.
O álcool presente na amostra é o
Dados: Massa molares (g.mol–1) H = 1 C = 12 O = 16
O dióxido de enxofre é um gás utilizado na produção do ácido
sulfúrico. Esse gás é emitido na queima de combustíveis e pode
ser muito prejudicial à saúde e ao meio ambiente. Para analisar a
presença de dióxido de enxofre em um determinado local, uma
amostra de ar foi borbulhada em 500 mL de um meio que
promoveu a conversão total do dióxido de enxofre em sulfato.
A amostra resultante foi analisada em um cromatógrafo iônico
em condições apropriadas, na mesma temperatura,
demonstrando que a concentração de sulfato presente
corresponde a 1 mmol . L–1.
A massa (em mg) de dióxido de enxofre presente na amostra é:
Dados: Massa molares (g.mol–1) S = 32 e O = 16
Segundo o Decreto n. 1.171/94 — Código de Ética Profissional do Servidor Public° Civil do Poder Executivo Federal —, analise as afirmativas a seguir.
I.E dever fundamental do servidor public° desempenhar a tempo, as atribuições do cargo, função ou emprego publico de que seja titular.
II.E dever fundamental do servidor public° tratar cuidadosamente os usuários dos serviços aperfeiçoando o processo de comunicação e contato com o public°.
III.E dever fundamental do servidor public° dificultar a fiscalização de todos os atos ou serviços por quem de direito. Assinale:
O boro-hidreto é um agente redutor útil, pois a semirreação
esquematizada a seguir, apresenta baixo potencial de redução:
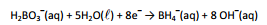
O íon boro-hidreto pode ser utilizado na deposição de níquel a
partir de uma solução contendo Ni2+.
A reação entre o íon boro-hidreto e o Ni2+ ocorre
A Lei de Efusão de Gases, escrita por Graham em 1846, afirma:
“a velocidade de efusão de um gás é inversamente proporcional à
raiz quadrada de sua densidade,ou de seu peso molecular."
A velocidade de um gás hipotético X2, através de um orifício,
corresponde a 0,315 vezes à velocidade do gás hidrogênio (H2),
formado apenas por isótopos de número de massa 1,0 através do
mesmo orifício nas mesmas condições de temperatura e pressão.
O valor do número de massa de X determinado pela Lei de
Graham é aproximadamente:
Dado: √ = 1,414
Para o preparo em laboratório de uma solução 4% (massa/volume) de hidróxido de sódio a partir de 50 mL de uma solução 5 mol . L-1
dessa base, é necessário Dados: Massa molar (g.mor-1): Na = 23 0 = 16 H = 1
Um químico preparou, para neutralizar o rejeito de uma reação,
uma solução básica de hidróxido de sódio dissolvendo óxido de
sódio puro em água, em um balão volumétrico de 250 mL. Uma
alíquota de 25 mL desta solução foi transferida para outro balão
volumétrico e diluída com água até 500 mL. A solução resultante
apresentou pH igual a 13.
No preparo da solução básica, a massa de óxido de sódio (em
gramas) dissolvida foi igual a
Dados: Massa molar (g.mol–1): H = 1 O = 16 Na = 23
A benzofenona é um composto orgânico utilizado em cosméticos para prevenir a degradação desses produtos pela luz ultravioleta e também pode ser adicionada a embalagens plásticas com o objetivo de bloquear os raios UV e proteger o produto. Para avaliar a contaminação de uma amostra de benzofenona com fenil-propanona foi utilizada a técnica de infravermelho. Considerando as absorções na região do infravermelho, os dois compostos podem ser distinguidos através da deformação
O Bi3+ pode ser determinado através da formação de BiOI
(oxiiodeto), neste método a solução fria contendo nitrato de
bismuto (III) deve ser levemente acidulada com ácido nítrico e em
seguida deve ser feita lentamente e com agitação, a adição de
iodeto de potássio na forma de pó para que ocorra formação do
BiI3 (triiodeto de bismuto) que em seguida é fervido com água
quente. Neste procedimento é formado um precipitado de BiOI
cor de cobre que deve ser filtrado, lavado com água e secado a
cerca de 110o
C até peso constante e em seguida pesado.
Utilizando o método descrito em condições apropriadas, a
quantidade de Bi3+ em uma amostra contendo nitrato de bismuto
(III) foi determinada através da formação de um precipitado de
BiOI, que após lavagem e secagem pesou 0,1g. Nestas condições,
a massa (em miligramas) de Bi3+ presente na amostra é,
aproximadamente:
Dados: Massa molares (g.mol–1) Bi = 209; Bi(NO3)3 = 395 e BiOI = 352
Em um recipiente de volume constante foi efetuada a reação de
decomposição:
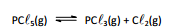
Inicialmente a pressão parcial do pentacloreto de fósforo era de
2,0 bar. A atingir o equilíbrio foi constatada uma porcentagem de
decomposição de 98%.
Se esse sistema em equilíbrio for perturbado pela adição de
0,01 mol de gás cloro, mantendo-se constante as condições
anteriores, quando o novo equilíbrio for atingido

