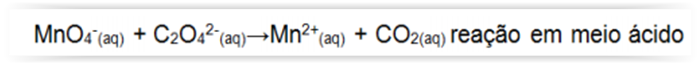Acerca de eletroquímica e de processos de oxidação e redução, julgue o item a seguir.
Eletroquímica é a parte da química que trata do uso das reações químicas para produzir eletricidade, das capacidades relativas de oxidação e redução e do uso da eletricidade para produzir uma transformação química.
O rompimento de uma adutora de 700 mm de diâmetro na tarde de quinta-feira do dia 22 de março de 2018, localizada no quilômetro 59 da via marginal da Anhanguera, afetou o abastecimento de água em alguns bairros de Jundiaí (SP).
(Adaptado de: https://g1.globo.com)
Esse evento pode ocorrer devido à corrosão eletroquímica. Em tubulações de ferro é adequado fazer proteção catódica, utilizando ânodos fixados na tubulação que fica submersa no solo.
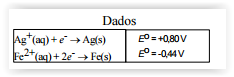
Considere os seguintes potenciais de redução, a 25,0 °C:

O metal mais apropriado como ânodo é o
Sobre a reação a seguir é CORRETO afirmar:
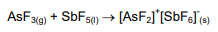
Os potenciais padrões de redução de meia célula são apresentados em uma escala de potencial elétrico em que o zero corresponde ao Zn
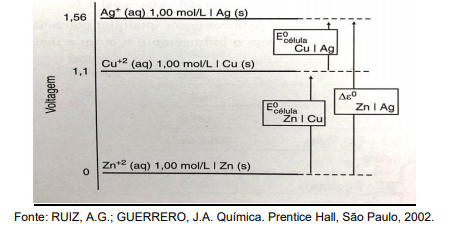
Uma pilha formada por Cu e Ag e outra entre Zn e Cu fornecerão os seguintes potenciais, respectivamente:
Acerca de eletroquímica e de processos de oxidação e redução, julgue o item a seguir.
Em uma célula eletroquímica, ânodo é o eletrodo no qual ocorre a oxidação e cátodo é o eletrodo no qual ocorre a redução.
Considere a pilha de Daniell

Em relação a essa célula eletroquímica, é falso afirmar que:
Um estudante administrou a eletrólise de sulfato de sódio aquoso usando eletrodos inertes e ao final identificou os produtos como hidrogênio
A notação padrão de uma pilha de Daniel composta por zinco e cobre, considerando-se os potencias padrões de redução à 25ºC, E oZn2+= -0,76V e EoCu2+ = +0,34V, será
Considerando-se a reação de oxirredução a seguir, assinalar a alternativa CORRETA
Nas células eletroquímicas, a ponte salina é usada para conectar as semicélulas de oxidação e redução e é constituída por uma solução eletrolítica. A função da ponte salina é de
O eletrodo padrão de hidrogênio (EPH) é considerado como o eletrodo de referência universal. O arranjo físico desse eletrodo consiste na imersão de um fio de platina em uma solução ácida que contém íons H+ na presença de gás hidrogênio borbulhado à pressão constante. No EPH, a função da platina é promover a
Qual o potencial da célula, em V, para o processo
eletroquímico no qual o ferro pode reduzir os íons prata?
Com relação à corrosão, analise as afrmativas. I. Na corrosão eletroquímica, os elétrons são cedidos em determinada região e recebidos em outras, aparecendo uma pilha de corrosão. II. Os aços inoxidáveis sofrem corrosão. III. O ácido sulfúrico concentrado é mais corrosivo que o mesmo ácido diluído. Está correto o que se afrma em:
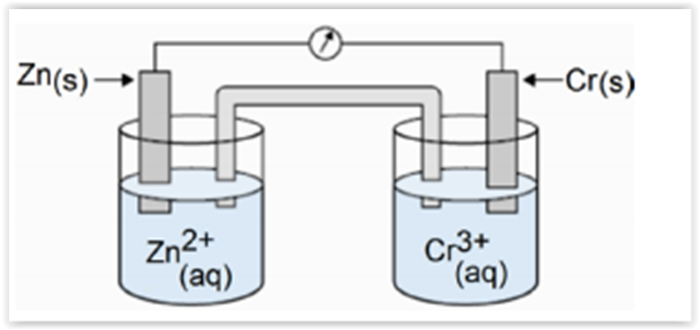
Uma pilha é definida como um equipamento que consegue converter energia química em energia elétrica. Para isso,
ela precisa conter dois eletrodos, o cátodo e o ânodo, formados por diferentes metais, por onde os elétrons irão fluir,
gerando a corrente elétrica. Diante do exposto, considerar a pilha galvânica apresentada na figura abaixo:
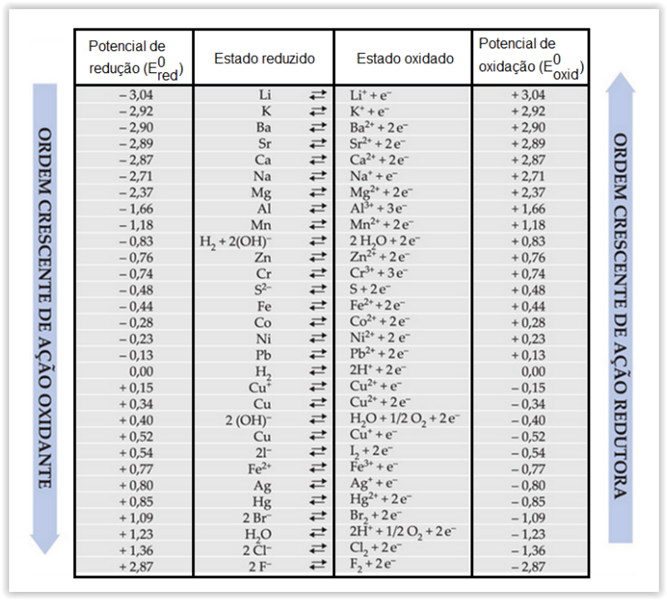
Considerando-se também a tabela de potenciais-padrão de redução, apresentados na tabela abaixo em V, assinalar a
alternativa que apresenta a força eletromotriz desse sistema em mV:
Com base nos conceitos de eletroquímica e de radioquímica,
julgue os próximos itens.
Agente oxidante é uma espécie que fornece elétrons a uma substância que está sendo reduzida (e ela própria sendo oxidada) em uma reação de oxirredução. Agente redutor é a espécie que remove elétrons da espécie que está sendo oxidada (e ele próprio é reduzido) em uma reação de oxirredução.