Em “Vemos as pessoas com quem discutimos como um adversário" (6º§), nota-se uma adequação de regência verbal em relação à norma. Desse modo, assinale a alternativa em que, na reescritura, NÃO se registra tal adequação.
Observe o emprego da concordância verbal em “Por essa razão, a maioria das pessoas acha que pode viver perfeitamente bem sem a metáfora." (1º§). Assinale a alternativa que apresenta um exemplo de concordância justificado pela mesma razão do trecho em destaque.
A frase “Eles governam também a nossa atividade cotidiana até nos detalhes mais triviais.” (2º§) estaria pontuada INADEQUADAMENTE com a seguinte reescritura:
De acordo com a lógica proposicional, a negação da frase “O advogado não foi convincente e a petição foi cancelada”
Leia o relato a seguir:

Sobre a influência indígena e Negra na formação Cultural Mato-Grossense, assinale a alternativa incorreta:
Assinale, das alternativas abaixo, a única que identifica corretamente uma das características técnicas básicas da Intranet:
Considerando as disposições da Lei Complementar de Mato Grosso nº 04/1990 (Estatuto do Servidor Público Estadual), assinale a alternativa INCORRETA sobre a posse no cargo público.
Quais são as espécies predominantes nas soluções aquosas descritas abaixo?
Solução I: solução aquosa de HCl (ácido forte)
Solução II: solução aquosa de NaOH (base forte)
Solução III: solução aquosa de HCN (ácido fraco)
Analise as seguintes afirmativas e a seguir assinale a alternativa correta:
I. A 300 K as pressões de equilíbrio de CO2, CO e O2 são, respectivamente, 0,6 atm, 0,4 atm e 0,2 atm. A constante de equilíbrio Kp para a reação representada por 2 CO2(g) 2 CO(g) + O2(g) é kp = 0,0889.
II. O valor de Kp a 2000 K para o equilíbrio: CO2(g) + H2(g) CO(g) + H2O(g) é 4,40. O valor de Kc nessas mesmas condições é kc = 4,40.
III. A constante de equilíbrio kc para a reação: 2SO2(g) + O2(g) 2SO3(g) é 249 a uma dada temperatura. Uma análise do conteúdo do recipiente que contém os três componentes nesta temperatura num determinado momento apresentou os seguintes resultados: [SO3] = 2,62 mol L-1, [SO2] = 0,149 mol L-1 e [O2] = 0,449 mol L-1. O sistema está em equilíbrio.
IV. A solubilidade molar do PbBr2 em água a partir do valor de kPS = 2,1x10-6 é 0,0081 mol L-1.
V. A 25°C a solubilidade molar do Ag3PO4 é 1,8x10-5 mol L-1. O kPS desse sal é kPS = 2,8x10-18
Assinale a alternativa correta:
Considerando a fórmula molecuar C 5H10O2 e as afirmações a seguir, assinale a alternativa correta:
I. A fórmula molecular C5H10O2 pode representar isômeros geométricos.
II. A fórmula molecular C5H10O2 não pode representar isômeros ópticos.
III. A fórmula molecular C5H10O2 pode representar isômeros de função.
IV. A fórmula molecular C5H10O2 pode representar isômeros de funções mistas.
V. A fórmula molecular C5H10O2 pode representar compostos cíclicos.
Assinale a alternativa correta:
Considere as seguintes afirmativas sobre os compostos de carbono e assinale a alternativa correta:
I. Os compostos orgânicos são muito mais numerosos do que os compostos que não contêm este elemento, pois o carbono pode, dentre outros fatores, formar ligações múltiplas, formar cadeias longas, curtas, lineares, ramificadas, cíclicas, saturadas e insaturadas, ligar-se a diferentes elementos.
II. A ligação insaturada de determinado hidrocarboneto é mais curta e mais forte que qualquer ligação simples de seu determinado análogo saturado, pois a hibridização sp3 de quaisquer dos carbonos do composto saturado não os permite sobrepor seus orbitais com os dos carbonos vizinhos.
III. A hibridização do carbono, dentre outros fatores, afeta a sua estrutura e, portanto, as suas propriedades, sendo as propriedades físicas mais amplamente afetadas que as propriedades químicas.
IV. A reatividade de um carbono terciário é sempre menor que a de um carbono primário, devido ao impedimento estéreo.
V. Compostos contendo ligações triplas, em geral, são mais reativos que seus compostos isólogos.
Assinale a alternativa correta:
Sobre a teoria atômica, considere as seguintes afirmações e assinale a alternativa correta:
I. Dalton chegou à conclusão da existência de átomos com base em observações químicas macroscópicas e não teve evidências diretas da existência de átomos.
II. Os experimentos de Thomson sobre o comportamento dos raios catódicos em campos magnéticos e elétricos proporcionaram a descoberta dos elétrons e permitiram que sua razão carga-massa fosse medida.
III. Os estudos de Rutherford mostraram que o átomo tinha um núcleo denso, carregado positivamente.
IV. De Broglie, Heisenberg, Born, Bohr e Planck foram cientistas que colaboraram para a teoria quântica moderna.
V. A dualidade onda-partícula, o princípio da incerteza, as funções de onda, a equação de Schrödinger, o princípio da exclusão de Pauli são contribuições recentes para a teoria atômica.
Assinale a alternativa correta:
Balanceie as equações químicas de I a V e na sequência assinale a alternativa correta:
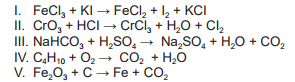
Assinale a alternativa que corresponde aos balanceamentos corretos das equações de I a V, considerando somente os mínimos números inteiros:
O gráfico p = f( V ) a seguir representa uma série de transformações para um mol de um gás de comportamento ideal.
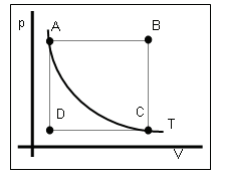
Identifique as transformações representadas por A→B, B→C, C→D, D→A e A→C e assinale a alternativa correta:
Ordene, de forma crescente, as forças de interação em:
I. Cristal de cloreto de sódio
II. Água pura
III. Acetona
IV. n-butano
V. Cloreto de sódio dissolvido em água
Agora assinale a alternativa que corresponde correta e respectivamente, à ordem crescente de força de interação das substâncias elencadas de I a V, anteriormente:


