Quanto às teclas de atalho do Microsoft Word 2016 (em inglês) e suas respectivas ações assinale, de cima para baixo, o preenchimento correto entre os parênteses, considerando a letra V para verdadeiro e a letra F para falso:
( ) Ctrl + E centralizar texto
( ) Ctrl + U sublinhado
( ) Ctrl + O fechar
Considere a reação 2CI
2(g) + 2H2O(g)  4HCI(g) + O2(g) (ΔH = 113 kJ.mol-1) e admita que o sistema está em equilíbrio. O que ocorre ao número de moléculas de H2O no recipiente se:
4HCI(g) + O2(g) (ΔH = 113 kJ.mol-1) e admita que o sistema está em equilíbrio. O que ocorre ao número de moléculas de H2O no recipiente se:
I - For adicionado O2 ?
II - For adicionado Cl2?
III - O volume do recipiente for diminuído?
IV - A temperatura for diminuída?
Assinale a alternativa que responde corretamente as perguntas acima:
O diagrama abaixo representa a variação de energia durante a reação: A  B. Assinale a alternativa que corresponde à sequência correta para preenchimento das lacunas:
B. Assinale a alternativa que corresponde à sequência correta para preenchimento das lacunas:

( ) corresponde à entalpia da reação direta
( ) corresponde à energia de ativação da reação direta
( ) corresponde à entalpia da reação inversa
( ) corresponde à energia de ativação da reação inversa
Assinale a alternativa correta:
Analise as afirmativas abaixo e assinale a alternativa correta. Um dos primeiros relatos da literatura que indicava a relevância da estereoquímica, mais particularmente da configuração absoluta na atividade biológica de fármacos, deve-se a Piutti em 1886, que descreveu o isolamento e as diferentes propriedades gustativas dos enantiômeros da asparagina. Essas diferenças de propriedades organolépticas expressavam modos diferenciados de reconhecimento molecular do ligante pelo sítio receptor, neste caso, localizado nas papilas gustativas, traduzindo sensações distintas. Entretanto, a importância da configuração absoluta na atividade biológica permaneceu obscura até a década de 60, quando ocorreu a tragédia da talidomida, decorrente do uso da sua forma racêmica, indicada para a redução do desconforto matinal em gestantes, resultando no nascimento de cerca de 12.000 crianças com deformações congênitas. Posteriormente, o estudo do metabolismo da talidomida permitiu evidenciar que o enantiômero ( S ) era seletivamente oxidado, levando à formação de espécies eletrofílicas reativas do tipo areno-óxido, que reagem com nucleófilos bioorgânicos, induzindo teratogenicidade, enquanto a antípoda ( R ) era responsável pelas propriedades sedativas e analgégicas. Esse episódio foi o marco da nova era do desenvolvimento de novos fármacos. Então, a quiralidade passou a ter destaque, e a investigação cuidadosa do comportamento de fármacos quirais ou homoquirais frente a processos capazes de influenciar tanto na farmacocinética como (i.e., absorção, interação fármaco-receptor) passou a ser fundamental antes de sua liberação para uso clínico.
I. Apesar do modelo chave-fechadura ser útil na compreensão dos eventos envolvidos no reconhecimento molecular ligante-receptor, caracteriza-se como uma representação parcial da realidade, uma vez que as interações entre as biomacromoléculas e a micromolécula apresentam características tridimensionais dinâmicas.
II. Dessa forma, o volume molecular do ligante, as distâncias interatômicas e o arranjo espacial entre os grupamentos farmacofóricos* compõem aspectos fundamentais na compreensão das diferenças na interação fármaco-receptor.
III. Sendo moléculas de estruturas definidas, absolutas, fatores como pH e temperatura têm pouca influência na ação e reatividade de fármacos quirais, uma vez que tais condições não são capazes de levar a sua isomerização.
IV. A presença da talidomida ( S ) numa mistura racêmica pode ser comprovada por espectroscopia de absorção no infravermelho, desde que antes seja separada de seu isômero por cromatografia líquida de alta resolução em coluna aquiral.
*Grupo farmacofórico é o conjunto de características eletrônicas e estéricas que caracterizam um ou mais grupos funcionais ou subunidades estruturais, necessários ao melhor reconhecimento molecular pelo receptor e, portanto, para o efeito farmacológico desejado
Assinale a alternativa correta:
As reações de adição a alcenos:
I. São reações eletrofílicas, onde a ligação dupla se comporta como uma base, já que participa com seus elétrons nas reações.
II. Seguem, em geral, a orientação de Markovnikov, mas adição de peróxidos pode mudar a sua estereoquímica, sobretudo na reação com cloro.
III. Seguem sempre um mecanismo em uma etapa, onde não há a formação de intermediários.
IV. Devido à alta reatividade dos alcenos, não necessitam de catálise.
V. Não apresentam rearranjos.
Assinale a alternativa correta:
Sobre a tabela periódica, em particular sobre energia de ionização, considere as afirmações a seguir:
I. A primeira energia de ionização é maior para os elementos próximos do hélio e menor para os próximos do césio.
II. A segunda energia de ionização é maior do que a primeira energia de ionização do mesmo elemento.
III. Os metais são encontrados à esquerda da tabela periódica porque esses elementos têm baixa energia de ionização e podem perder elétrons facilmente.
IV. Elementos com energias de ionização altas não devem formar cátions facilmente ou conduzir eletricidade.
V. A energia de ionização é a energia necessária para remover um elétron de um átomo na fase gás. De certo modo ela é de fundamental importância para entender como as ligações químicas são formadas e, portanto, sobre as propriedades físicas das moléculas.
Assinale a alternativa correta:
Considere as reações abaixo, as afirmativas a seguir e assinale a alternativa correta:

I. Segundo a teoria de Brønsted-Lowry, o íon bicarbonato na Reação 1 é um ácido.
II. Segundo a teoria de Lewis, a amônia na Reação 2 é uma base, pois ela doa elétrons.
III. Segundo a teoria de Lewis, o íon bicarbonato na Reação 1 é anfótero.
IV. Segundo Brønsted-Lowry, o íon carbonato na Reação 1 é uma base, chamada de base conjugada do íon bicarbonato.
V. Todas as bases de Brønsted-Lowry mostradas nas equações são também consideradas bases de Lewis.
Assinale a alternativa correta:
Analise as afirmativas abaixo e assinale a alternativa em que a obtenção do ferro a partir da hematita pode ser descrita pela equação: Fe2O3 + 3CO → 2Fe + 3CO2.
I. A massa de ferro que será obtida a partir de 0,04 mol de óxido férrico é 4,48 g.
II. A quantidade de CO necessários para produzir 7 mol de ferro é 10,5 mol.
III. A massa de gás carbônico obtida partindo-se de 20 kg de óxido de ferro III será 16,5 g.
IV. A quantidade de monóxido de carbono necessária para reagir com 600 g de óxido férrico é 11,25 mol.
V. O volume de CO, medidos nas CNTP, consumido na obtenção de 60 kg de ferro será ~3,6 104 L.
Após analisar as afirmativas de I a V, assinale a alternativa correta:
Entre os vocábulos destacados em “é mais uma questão de linguagem extraordinária do que de linguagem ordinária."(1º§), percebe-se uma relação semântica de:
A metáfora como figura de linguagem, apresentada no texto I, está explicitada no texto II por meio da aproximação do seguintes termos:
Analise as afirmativas abaixo e assinale a alternativa correta.
I. Segundo o antropólogo Lévi-Strauss (2000), a passagem da natureza à cultura foi produzida pela instauração da lei, pela proibição do incesto, mediante a qual se estabeleceram as relações de parentesco e de aliança e o mundo humano, simbólico, foi construído. Essa orientação normativa da conduta, no entanto, é exterior ao indivíduo, de modo que a adequação ou não à norma estabelecida, bem como a variação de tempo e lugar, é que acaba definindo se o ato é moral ou imoral.
II. A moral é apenas um conjunto de regras impostas aos indivíduos, mas a livre e consciente adesão a elas, razão pela qual um ato só pode ser considerado moral se passar pela aceitação da norma, ou seja, não é verdadeiramente moral o ato que for cumprido ou não mediante ameaça de sanções, o que não significa que uma norma não possa ser questionada, mas também não pode ser persistentemente interrogada, porque isto pode levar à destruição da moral.
III. Segundo Gianotti, a flexibilidade existe, porém não pode levar a um relativismo em todas as formas de conduta: os direitos do homem, tais como em geral têm sido enunciado a partir do século XVIII, estipulam condições mínimas do exercício da moralidade. Por certo, cada um não deixará de aferrar-se à sua moral; deve, entretanto, aprender a conviver com outras, reconhecer a unilateralidade de seu ponto de vista.
IV. Para ser moral um ato não deve ser livre, consciente, intencional e responsável. Isso cria um compromisso de reciprocidade e compromisso com a comunidade. o sujeito, assim, deve saber o que e por que faz, não deve ser coagido ou obrigado a fazer algo e, além disso, deve assumir a autoria do seu ato, reconhecendo-o como seu e respondendo pelas consequências de sua ação.
Estão corretas as afirmativas:
Sobre as consequências da Guerra do Paraguai (1864- 1870) para o Império do Brasil e a província do Mato Grosso assinale a alternativa incorreta:
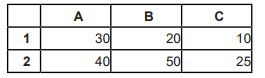
Com base na planilha do Excel abaixo, assinale a alternativa que apresenta a fórmula correta que está embutida na célula C2:
Quanto às ferramentas e aplicativos de navegação e de correio eletrônico, analise as afirmativas abaixo, dê valores Verdadeiro ( V ) ou Falso ( F ) e assinale a alternativa que apresenta a sequência correta (de cima para baixo):
( ) enquanto o protocolo SMTP é para envio, o POP3 é para receber e-mails.
( ) o correio eletrônico é tipicamente uma ferramenta de comunicação síncrona.
( ) o IP (Internet Protocol) possui atualmente somente as versões IPv4 e IPv6.





