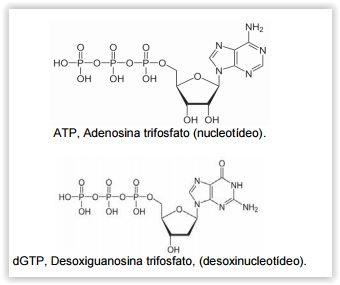
A seguir estão representadas as estruturas de alguns compostos orgânicos:
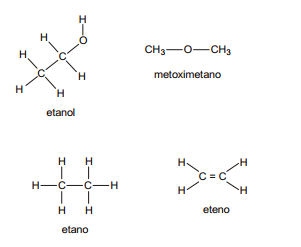
A maior solubilidade em água é observada para o
A mudança de cor de um indicador ácido-base ocorre segundo o princípio de Le Chatelier. Considere o seguinte sistema para
uma infusão contendo chá mate:
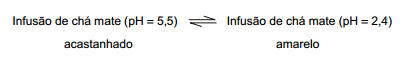
É observada a cor amarela quando se adiciona à infusão
As seguintes formas de abordagem são sugeridas na Proposta Curricular do Estado de Minas Gerais, para o ensino de Química:
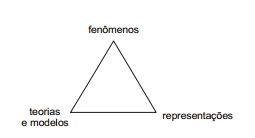
O desenvolvimento, nos alunos, da habilidade analisar resultados necessita que o trabalho do professor ocorra na seguinte sequência de abordagens:
Uma das formas de obter a entalpia de uma reação é por meio de diagramas de energia, como o representado a seguir para a
reação 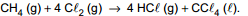
A entalpia da reação

Realizou-se um estudo da influência da temperatura em uma reação na qual a concentração inicial dos reagentes foi igual em todos os experimentos. O resultado desse estudo está no gráfico.
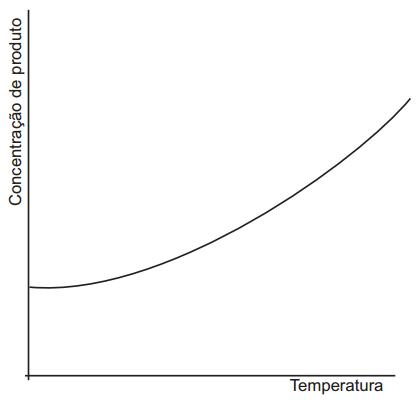
Considere as afirmativas que se referem a esse estudo.
I - O aumento da temperatura favorece a formação de produtos.
II - A constante de equilíbrio da reação não varia com o aumento da temperatura.
III - A concentração de reagentes, no final dos experimentos, é sempre a mesma.
IV - A diminuição da temperatura desloca o equilíbrio no sentido inverso.
Estão corretas APENAS as afirmativas:
Considere o texto a seguir para responder às questões
de nºs 30 e 31.
O petróleo é formado majoritariamente por hidrocarbonetos.
Compostos sulfurados estão presentes em pequenas
quantidades, porém são causadores de corrosão, envenenamentos
de catalisadores e poluição do meio ambiente.
Uma das técnicas utilizadas para se reduzir a quantidade
de sulfurados no petróleo é o chamado tratamento
merox, que consiste na extração de compostos sulfurados
corrosivos (I), utilizando-se solução de hidróxido de sódio
e posterior transformação em compostos sulfurados menos
agressivos (II), como fica evidenciado nas reações
apresentadas abaixo.
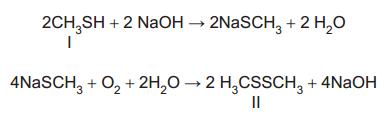
As funções químicas presentes nos compostos I e II são, respectivamente,
A figura representa a piridina, um dos compostos orgânicos nitrogenados, presente em pequenas quantidades no petróleo bruto.
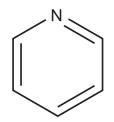
Os compostos orgânicos nitrogenados, como a piridina representada acima, estão presentes em pequenas quantidades no petróleo bruto.
Em relação à piridina, verifica-se que ela
A massa específica de um gás varia com a altura da forma ρ = α P, onde α = 2,0 x 10-5kg x Pa/m3 é uma constante, e P é a pressão. A densidade varia como ρ = ρ0 e-gah, onde ρ0é a densidade da atmosfera na superfície da Terra.
Ao se calcular, em Pa, a pressão a 10,0 km da superfície da Terra, encontra-se
Dados:
g = 10,0 m/s2
Pressão na superfície da Terra P0 = 1,0 ×105 Pa
e = 2,7
A temperatura da atmosfera é constante
Considere o texto abaixo para responder às questões
de nºs 56 e 57.
A gasolina e o óleo diesel são exemplos de combustíveis
obtidos a partir do petróleo. No Brasil, a gasolina, juntamente
com o etanol, é a opção de combustível de veículos
de pequeno porte, como carros de passeio e motocicletas.
Já veículos pesados, como caminhões e ônibus,
normalmente operam com o diesel. Apesar da mesma
origem, os motores que usam diesel são bem diferentes
daqueles que usam gasolina.
Na separação das frações do petróleo, a faixa de temperatura de destilação dos componentes da gasolina, em relação à dos componentes do óleo diesel, é
A figura apresenta substâncias orgânicas.
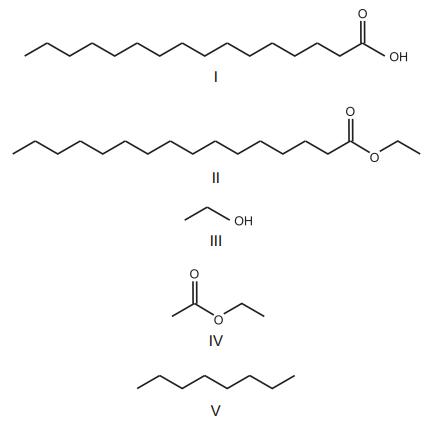
Considerando-se essas substâncias, verifica-se que os biocombustíveis estão representados em:
DNA e RNA são biopolímeros. O DNA é sintetizado
a partir de desoxinucleotídeos e o RNA
por nucleotídeos.
Considere a fórmula estrutural plana de dois
tipos de moléculas que são utilizados na síntese
desses biopolímeros:
Baseado nas informações fornecidas e nos conceitos
químicos, analise as afirmações a seguir.
l Ambas as moléculas possuem a função química
amida em sua estrutura.
ll Na molécula ATP, não existem elétrons p em ressonância.
lll Ambas as moléculas possuem ao menos uma
amina terciária
lV Na molécula dGTP existe uma carbonila.
Todas as afirmações corretas estão em:
Com relação aos conceitos sobre equilíbrios
químicos, analise as afirmações a seguir.
l Alterando a concentração dos participantes de um
equilíbrio químico, Kc não altera, mas poderá
ocorrer a variação do α.
ll Alterando a temperatura de um equilíbrio químico,
Kc é alterado, assim como α.
lll Em um equilíbrio químico a adição de um catalisador
não altera Kc assim como α.
lV Nos equilíbrios que envolvem gases, uma altera-
ção na pressão total não altera Kc nem Kp mas
varia α.
Dados:
Kc = constante de equilíbrio em função da concentração dos
participantes em mol/L.
Kp = constante de equilíbrio em função da pressão parcial dos
participantes gasosos.
α = grau de dissociação do equilíbrio (%).
Todas as afirmações corretas estão em:
Qual a energia liberada na combustão completa
de 138g de CH3CH2OH(l), a 25ºC e 1 atm?
Dados: Entalpias de formação das substâncias a 25ºC e 1
atm: CH3CH2OH(l) = - 278 kJ/mol; CO2(g) = - 394 kJ/mol; H2O(g)
= - 242 kJ/mol. C: 12 g/mol, O: 16 g/mol, H: 1 g/mol.
Assinale a alternativa que corretamente apresenta a geometria para as moléculas de CH4 e PCl5, respectivamente.
Assinale a alternativa correta.