Observe as ilustrações a respeito dos símbolos/pictogramas de perigo a serem adotadas nos rótulos dos produtos químicos, de acordo com o sistema de padronização e harmonização da classificação e rotulagem preventiva de produtos químicos globalmente aceito e correlacione-as com as informações a seguir.

( ) Usada para indicar: risco à saúde, de carcinogenicidade, mutagenicidade, toxicidade para a reprodução, sensibilização respiratória, toxicidade no órgão-alvo, perigo por aspiração.
( ) Usada para indicar: risco à saúde, de irritação (pele e olhos), sensibilização cutânea, irritação das vias aéreas superiores, efeito narcótico, toxicidade aguda (nocivo), perigo à camada de ozônio.
( ) Usada para indicar: líquidos oxidantes.
( ) Usada para indicar: gases sob pressão.
A sequência correta, de cima para baixo, é:
A medida precisa de volume é tão importante para um método analítico quanto a medida precisa da massa. Entretanto, medidas confiáveis de volume exigem uma série de cuidados no uso dos aparatos volumétricos. A respeito do uso adequado das pipetas volumétricas analise as sentenças, e em seguida, assinale a alternativa correta.
O cálcio apresenta elevada abundância em solos e águas naturais, e diversas metodologias analíticas podem ser empregadas para a sua adequada quantificação. Desde a década de 50 até os dias atuais, o método titrimétrico de complexação do cálcio com EDTA, em meio alcalino, tem sido empregado com êxito para essa finalidade. Acerca das titulações de complexação com o EDTA, assinale a alternativa correta.
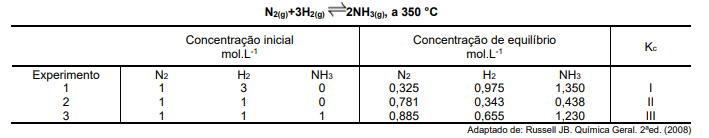
De acordo com a equação a seguir e as informações hipotéticas da tabela apresentada, referentes a três diferentes experimentos que usaram concentrações diferentes de N2(g) e 3H2(g) na produção de 2NH3(g), a 350ºC, assinale a alternativa que apresenta a correta relação das constantes de equilíbrio (I, II, III) de concentração (Kc) entre os diferentes experimentos.
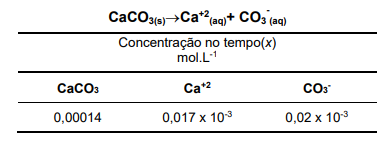
Quando um sal sólido se dissolve formando seus íons constituintes em solução, é possível medir o seu produto de solubilidade (Kps) no estado de equilíbrio. Observe a equação a seguir e as informações hipotéticas da tabela apresentada a respeito do produto de solubilidade do CaCO3 em água a 25°C e assinale a alternativa correta. Considere Kps de CaCO3 a 25ºC igual a 3,4×10-9.
O gás amônia, perigoso aos seres humanos, é de uso comum nas indústrias alimentícias, petroquímicas e metalúrgicas com várias aplicações. Mesmo exigindo o uso adequado de equipamentos de proteção individual e procedimentos de segurança, uma indústria teve o gás amônia recentemente citado em um vazamento de gás que levou centenas de seus funcionários a procurar atendimento médico com sintomas característico de intoxicação. A respeito da produção do gás amônia apresentado na equação a seguir, assinale a alternativa que apresenta o volume do gás NH3 obtido a partir de 12 L de N2(g).
Considere todos os gases nas condições normais de temperatura e pressão (CNTP).
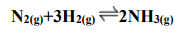
Qual a concentração em mol.L-1 de uma solução obtida pela dissolução de 750 mg de cloreto de potássio (KCl) em 500 mL de água destilada?
(Dados: massa atômica K=39,1; Cl=35,5)
Correlacione as cadeias carbônicas apresentadas a seguir com as suas respectivas classificações.
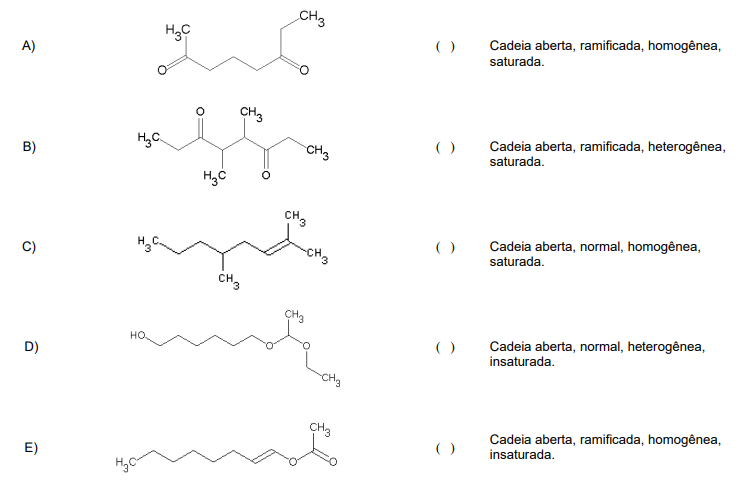
A sequência correta, de cima para baixo, é:
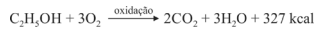
Sabendo que a reação apresentada mostra o processo de oxidação do etanol — em que são liberadas 327 kcal por mol de energia — e que as massas atômicas do carbono, do oxigênio e do hidrogênio são, respectivamente, iguais a 12, 16 e 1, julgue o item a seguir.
A massa de 1 mol de etanol é 46 g
Ocorrendo acidentalmente o derramamento de pequena quantidade de um hidrocarboneto líquido derivado de petróleo sobre a bancada de trabalho, deve-se de imediato
Entre os ácidos inorgânicos, cujas fórmulas são citadas, o único classificado como diácido é o
Com base nas seguintes informações, responda a questão.
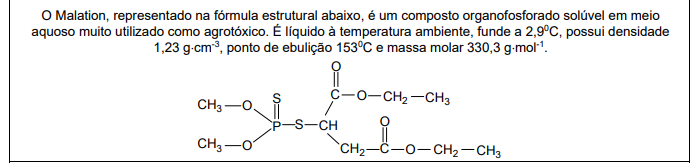
Na molécula desse composto há
A tabela periódica é uma das realizações mais notáveis da Química porque ajuda a organizar a extensa quantidade de propriedades dos elementos, que, de outra forma, seria um arranjo confuso. A tabela periódica pode ser usada na previsão de um grande número de propriedades, muitas das quais são cruciais para a compreensão das características químicas e físicas dos compostos.
Sobre as propriedades periódicas dos átomos, pode-se afirmar que
Em condições ideais, pequenas quantidades de gás cloro podem ser geradas em laboratório pela reação do óxido de manganês (MnO2) com ácido clorídrico (HCl), conforme a equação química a seguir não balanceada.
HCl(aq) + MnO2(s) → H2O(L) + MnCl2(s) + Cl2(g)
A partir dessas informações, quantas moléculas de gás cloro, aproximadamente, podem ser produzidas quando 10 g de óxido de manganês com grau de pureza de 87% são colocados para reagir completamente com excesso de ácido clorídrico?
Dado: Número de Avogadro (N) = 6 x 1023
A maior parte da produção de amônia, nos dias atuais, é utilizada para a produção de fertilizantes. Esse processo é conhecido como Haber-Bosch. Parte de nitrogênio (N2) e Hidrogênio (H2) formando a amônia (NH3). A reação é executada entre 400 e 450° C e 600 atm (atmosferas) e pode ser representada pela equação abaixo.
____N2(g)+_____H2(g) ⇔ _____ NH3(g)
Assinale a alternativa que completa correta e respectivamente as lacunas nos balanceamentos da reação acima.

