Julgue os seguintes itens, em relação à eletroquímica.
O potencial da semirreação representada a seguir não depende do pH.
![]()
Julgue os próximos itens, a respeito da equação de Nernst e de potencial de eletrodo, eletrodos indicadores e medidas de pH.
Potencial de eletrodo é a medida do potencial individual de um eletrodo reversível no estado-padrão, ou seja, solutos em concentração de 1 mol/kg e gases à pressão de 1 bar, ambos a 273 K.
Julgue os próximos itens, a respeito da equação de Nernst e de potencial de eletrodo, eletrodos indicadores e medidas de pH.
Para determinar a capacidade de um metal em atuar como anodo de sacrifício, é adequado montar um eletrodo com o referido metal, com potencial desconhecido, ligá-lo a um eletrodo de potencial conhecido e medir a diferença de potencial entre os eletrodos. Nesse contexto, pode-se usar, para a avaliação, um eletrodo de zinco metálico (Zn), que, em uma célula eletroquímica com solução 1 mol/L de ZnSO4, apresenta a seguinte semirreação no anodo.
Zn (s) → Zn2+ (aq) + 2 e−
Julgue os seguintes itens, em relação à eletroquímica.
Os potenciais-padrão das semirreações de oxirredução são medidos com base no eletrodo-padrão de hidrogênio, cujo
valor estabelecido é 0,00 V.
Julgue os seguintes itens, em relação à eletroquímica.
Considerando-se os potenciais de redução ![]() , é correto afirmar que um prego de ferro colocado em uma solução de HCl 1 mol/L permanece em seu estado inalterado.
, é correto afirmar que um prego de ferro colocado em uma solução de HCl 1 mol/L permanece em seu estado inalterado.
Julgue os próximos itens, a respeito da equação de Nernst e de potencial de eletrodo, eletrodos indicadores e medidas de pH.
A equação de Nernst tem por finalidade prever o potencial de uma pilha durante o seu funcionamento, correlacionando a variação do potencial da pilha em certo instante da reação com a variação das concentrações de produtos e reagentes.
Julgue os seguintes itens, em relação à eletroquímica.
Segundo a IUPAC, a dupla barra vertical na notação das pilhas eletroquímicas representa a ponte salina.
2 H2O ⇌ 2 H2 + O2
Considerando a reação de eletrólise da água mostrada acima, e sabendo que ZH = 1, ZO = 8, ZP = 15, MH = 1,0 g/mol, MO = 16,0 g/mol e que R = 0,082 atm ∙ L ∙ K−1 ∙ mol−1 é a constante universal dos gases perfeitos, julgue os itens que se seguem.
Supondo que todo o oxigênio produzido na eletrólise seja lançado na atmosfera, então, a 1 atm de pressão e 298 K de temperatura, uma tonelada de água submetida à eletrólise lançará mais de 500.000 L de oxigênio na atmosfera.
Julgue o seguinte item, relativo a fundamentos de eletromagnetismo.
Uma corrente elétrica que percorre um condutor gera, em torno desse condutor, um campo magnético com direção determinada pela regra da mão esquerda.
2 H2O ⇌ 2 H2 + O2
Considerando a reação de eletrólise da água mostrada acima, e sabendo que ZH = 1, ZO = 8, ZP = 15, MH = 1,0 g/mol, MO = 16,0 g/mol e que R = 0,082 atm ∙ L ∙ K−1 ∙ mol−1 é a constante universal dos gases perfeitos, julgue os itens que se seguem.
Uma tonelada de água produzirá menos de 120 kg de hidrogênio em uma eletrólise.
Observe a pilha representada na imagem e baseado nos seus conhecimentos de eletroquímica julgue a veracidade das informações abaixo:
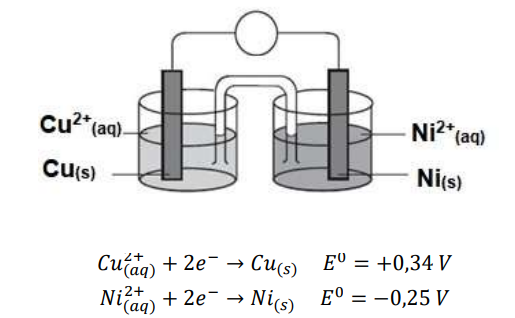
I. A região que sofre redução é o cátodo.
II. A placa de cobre que atua com ânodo e sofre corrosão.
III. O fluxo de elétrons do sistema vai da placa cobre para a placa de níquel
As afirmações verdadeiras são:
A estabilidade de coloides liófobos envolve um balanço complexo de interações entre partículas que pode ser perturbado por uma alteração externa. Um processo indicado para separar partículas coloidais de um sol aquoso é a
“Em 1836, o químico inglês John Frederic Daniell construiu uma pilha usando metais e soluções aquosas de sais. A pilha funcionava a partir de dois eletrodos interligados. O eletrodo é, geralmente, um sistema constituído por um metal imerso em uma solução aquosa de um sal formado pelos cátions desse metal.”
*Adaptado de: FONSECA, Martha Reis Marques. Química. São Paulo: Editora FTD, 2007. v. 2: Físico-Química. p. 276.
Considere a representação da notação química da pilha de Daniell (usando eletrodos de cobre e zinco), de acordo com a União Internacional de Química Pura e Aplicada (IUPAC):
Zn (s) | Zn2+ (aq) (1 mol L-1) || Cu2+ (aq) (1 mol L-1) | Cu (s).
Dados os potenciais padrão de redução E0 Zn = - 0,76 V e E0 Cu = + 0,34 V, e considerando o funcionamento da referida pilha em condições padrão, afirma-se que
I – no eletrodo de cobre dessa pilha ocorre a corrosão da placa metálica de cobre.
II – a diferença de potencial (d.d.p.) teórica dessa pilha é de + 1,10 V.
III – nessa pilha os elétrons fluem no circuito externo, do eletrodo de zinco para o eletrodo de cobre.
IV – o símbolo de duas barras paralelas ( || ) representa a ponte salina (ou uma membrana porosa), cuja finalidade é manter as duas semicelas eletricamente neutras, por meio da migração de íons (corrente iônica).
V – a equação da reação global dessa pilha é Zn2+ (aq) + Cu (s) → Zn (s) + Cu2+ (aq).
Das afirmativas feitas, estão corretas apenas
Leia os textos a seguir e resolva a questão:

Considere a seguinte equação de reação química de oxidorredução não balanceada:
As2S3 + NH4OH + H2O2 → (NH4)3AsO4 + (NH4)2SO4 + H2O
Acerca desta reação química de oxidorredução e de suas espécies, são feitas as seguintes afirmativas:
I – O peróxido de hidrogênio é o agente redutor.
II – Após o devido balanceamento, o coeficiente estequiométrico da água é 20.
III – O arsênio da substância As2S3 é reduzido, enquanto o enxofre é oxidado.
IV – O (NH4)2SO4 é um sal cujo nome é sulfito de amônio.
V – Após o devido balanceamento, a soma de todos os coeficientes estequiométricos da equação é igual a 52.
Das afirmativas feitas, estão corretas apenas
Em meados do século XX, as pilhas alcalinas surgiram como uma alternativa muito mais eficiente energeticamente em comparação às pilhas tradicionais. Como mostra a seguinte figura, a pilha alcalina utiliza os mesmos eletrodos da tradicional, porém o seu eletrólito é uma solução aquosa de hidróxido de sódio concentrada (~30% em massa) contendo uma dada quantidade de óxido de zinco ― daí a denominação alcalina para essa pilha.
Durante o funcionamento dessa pilha, o

