Água dura é aquela que contém concentrações relativamente altas de íons Ca2+ e Mg2+ dissolvidos. Apesar de esses íons não representarem risco para a saúde, eles podem tornar a água imprópria para alguns tipos de consumo doméstico ou industrial. Objetivando reduzir a concentração de íons Ca2+ e Mg2+ de uma amostra de água dura ao mínimo possível, um técnico em química testou os seguintes procedimentos no laboratório:
I — Decantação da amostra de água
II — Filtração da amostra de água.
III — Aquecimento da amostra de água.
IV — Adição do solvente orgânico CCl4 à amostra de água.
V — Adição de CaO e Na2CO3 à amostra de água. BROWN, T. L. et al. Química, a ciência central. São Paulo: Pearson Prentice Hall, 2005 (adaptado).
O método considerado viável para tratar a água dura e aumentar seu potencial de utilização é o(a)
O cobre, muito utilizado em fios da rede elétrica e com considerável valor de mercado, pode ser encontrado na natureza na forma de calcocita, Cu2S (s), de massa molar 159 g/mol. Por meio da reação Cu2S (s) + 02 (g) -> 2 Cu (s) + S02 (g), é possível obtê-lo na forma metálica. A quantidade de matéria de cobre metálico produzida a partir de uma tonelada de calcocita com 7,95% (m/m) de pureza é
Fertilizantes químicos mistos, denominados NPK, são utilizados para aumentar a produtividade agrícola, por fornecerem os nutrientes nitrogênio, fósforo e potássio, necessários para o desenvolvimento das plantas. A quantidade de cada nutriente varia de acordo com a finalidade do adubo. Um determinado adubo NPK possui, em sua composição, as seguintes substãncias: nitrato de amõnio (NH4NO3), ureia (CO(NH2)2) nitrato de potássio (KNO3), fosfato de sódio (Na3PO4) e cloreto de potássio (KCI).
A adição do adubo descrito provocou diminuição no pH de um solo. Considerando o caráter ácido/básico das substãncias constituintes desse adubo, a diminuição do pH do solo deve ser atribuída à presença, no adubo, de uma quantidade significativa de
Grande quantidade dos maus odores do nosso dia a dia está relacionada a compostos alcalinos. Assim, em vários desses casos pode-se utilizar o vinagre, que contém entre 3,5% e 5% de ácido acético, para diminuir ou eliminar o mau cheiro. Por exemplo, lavar as mãos com vinagre e depois enxaguá-las com água elimina o odor de peixe, já que a molécula de piridina (C5H5N) é uma das substâncias responsáveis pelo odor característico de peixe podre.
SILVA, V. A.; BENITE, A. M. C.; SOARES, M.H.F.B. Algo aqui não cheira bem. A química do mau cheiro.
A eficiência do uso do vinagre nesse caso se explica pela:
O estudo de compostos orgânicos permite aos analistas definir propriedades físicas e químicas responsáveis pelas características de cada substância descoberta. Um laboratório investiga moléculas quirais cuja cadeia carbônica seja insaturada, heterogênea e ramificada.
A fórmula que se enquadra nas características da molécula investigada é:
O principal processo industrial utilizado na produção de fenol é a oxidação do cumeno (isoprilbenzeno). A equação mostra que esse processo envolve a formação do hidroperóxido de cumila, que em seguida é decomposto em fenol e acetona, ambos usados na indústria química como precursores de moléculas mais complexas. Após o processo de síntese, esses dois insumos devem ser separados para comercialização individual.
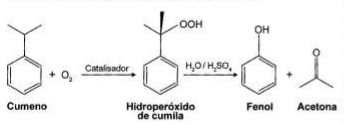
Considerando as características físico-químicas dos dois insumos formados, o método utilizado para a separação da mistura, em escala industrial, é a
Alguns materiais poliméricos não podem ser utilizados para a produção de certos tipos de artefatos, seja por limitações das propriedades mecânicas,
seja pela facilidade com que sofrem degradação, gerando subprodutos indesejáveis para aquela aplicação. Torna-se importante, então, a fiscalização, para
determinar a natureza do polímero utilizado na fabricação do artefato. Um dos métodos possíveis baseia-se na decomposição do polímero para a geração dos
mon6meros que lhe deram origem. A decomposição controlada de um artefato gerou a diamina H2N(CH2)6NH2 e o diácido HO2C(CH2)4CO2H.
Logo, o artefato era feito de
Você já ouviu essa frase: rolou uma química entre nos! O amoré frequentemente associado a um fenômeno mágico ou espiritual,
porem existe a atuação de alguns compostos em nosso corpo, que provocam sensações quando estamos perto da pessoa amada, como coração acelerado
e aumento da frequência respiratória.
Essas sensações são transmitidas por neurotransmissores, tais como adrenalina, noradrenalina, feniletilamina, dopamina e as serotoninas.
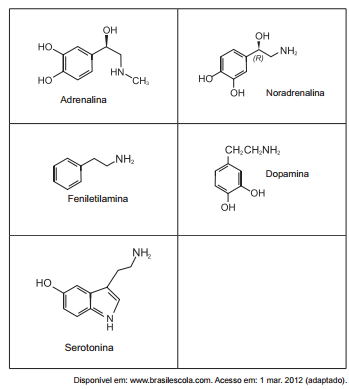
Os neurotransmissores citados possuem em grupo funcional característico da função
Uma forma de poluição natural da água acontece em regiões ricas em dolomita (CaCO3MgCO3).
Na presença de dióxido de carbono (dissolvido na água) a
dolomita a convertida em Ca(HCO3)2 e MgCO3, elevando a concentração de íons Ca2+ e Mg2+ na água.
Uma forma de purificação dessa água, denominada água dura, é adicionar Ca(OH)2 e Na2CO3 a ela.
Dessa forma, ocorre uma serie de reagoes quimicas gerando como produto final CaCO3 e Mg(OH)2,
que são menos solúveis que Ca(HCO3)2 e MgCO3.
Uma técnica apropriada para obtenção da água pura após o abrandamento
No Brasil e no mundo têm surgido movimentos e leis para banir o uso de sacolas plásticas, em supermercados, feitas de polietileno. Obtida a partir do petróleo, a matéria-prima do polietileno é o gás etileno, que depois de polimerizado dá origem ao plástico, composto essencialmente formado pela repetição de grupos —CH2—. O principal motivo do banimento é a poluição, pois se estima que as sacolas levam cerca de 300 anos para se degradarem no meio ambiente, sendo resistentes a ataques químicos, à radiação e a microrganismos.
O motivo pelo qual essas sacolas demoram muito tempo para se degradarem é que suas moléculas
A escolha de uma determinada substãncia para ser utilizada como combustível passa pela análise da poluição que ela causa ao ambiente e pela quantidade de energia liberada em sua combustão completa. O quadro apresenta a entalpia de combustão de algumas substãncias. As massas molares dos elementos H, C e O são, respectivamente, iguais a 1 g/mol, 12 g/mol e 16 g/mol.

Levando-se em conta somente o aspecto energético, a substãncia mais eficiente para a obtenção de energia, na combustão de 1 kg de combustível, é o
Parte do gás carbônico da atmosfera é absorvida pela água do mar. O esquema representa reações que ocorrem naturalmente, em equilíbrio, no sistema ambiental marinho. O excesso de dióxido de carbono na atmosfera pode afetar os recifes de corais.
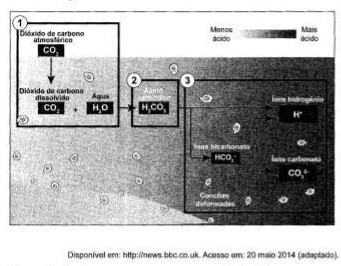
O resultado desse processo nos corais é o(a)
Diesel é uma mistura de hidrocarbonetos que também apresenta enxofre em sua composição. Esse enxofre é um componente indesejável, pois o trióxido de enxofre gerado é um dos grandes causadores da chuva ácida. Nos anos 1980, não havia regulamentação e era utilizado óleo diesel com 13 000 ppm de enxofre. Em 2009, o diesel passou a ter 1 800 ppm de enxofre (S1800) e, em seguida, foi inserido no mercado o diesel S500 (500ppm). Em 2012, foi difundido o diesel S50, com 50 ppm de enxofre em sua composição. Atualmente, é produzido um diesel com teores de enxofre ainda menores.
Os impactos da má qualidade do óleo diesel brasileiro. Disponível em www.cnt.org.br
Acesso em 20 dez.: 2012 (adaptado).
A substituição do diesel usados nos anos 1980 por aquele difundido em 2012 permitiu uma redução percentual de emissão SO3 de
Um método para determinação do teor de etanol na gasolina consiste em misturar volumes conhecidos de água e de gasolina em um frasco específico. Após agitar o frasco e aguardar um período de tempo, medem-se os volumes das duas fases imiscíveis que são obtidas: uma orgânica e outra aquosa. O etanol, antes miscível com a gasolina, encontra-se agora miscível com a água.
Para explicar o comportamento do etanol antes e depois da adição de água, é necessário conhecer
O entendimento de como as ligações químicas se formam a um dos assuntos fundamentais da ciência.
A partir desses fundamentos, pode-se entender como são desenvolvidos novos matérias. Por exemplo, de acordo com a regra do octeto,
na formação de uma ligação covalente, os átomos tendem a completar seus octetos pelo compartilhamento de elétrons (atingir configuração de gás nobre,
ns2 np6). Porem, quando o átomo central de uma molécula tem orbitais d vazios, ele pode acomodar 10, 12 ou ate mais elétrons.
Os elétrons desta camada de Valencia expandida podem estar como pares isolados ou podem ser usados pelo átomo central para formar ligações.
A estrutura que representa uma molécula com o octeto expandido (exceção a regra do octeto)

