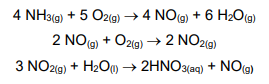Uma docente solicitou ao técnico de laboratório que previsse a quantidade, em massa, de limalhas de ferro para seis experimentos a serem realizados em uma aula de Química Geral. A reação pretendida deverá levar à formação de 0,002 mol de cloreto de ferro/experimento, equivalente ao rendimento de 80%, a partir da interação do ferro metálico com ácido clorídrico. Ao final dos cálculos químicos, o técnico apresentou à docente a seguinte quantidade de limalha de ferro para a aula em questão
O etanol é um combustível renovável obtido da cana-de-açúcar e é menos poluente do que os combustíveis fósseis, como a gasolina e o diesel. O etanol tem densidade ![]() massa molar
massa molar ![]() e calor de combustão aproximado de
e calor de combustão aproximado de ![]() Com o grande aumento da frota de veículos, tem sido incentivada a produção de carros bicombustíveis econômicos, que são capazes de render até
Com o grande aumento da frota de veículos, tem sido incentivada a produção de carros bicombustíveis econômicos, que são capazes de render até ![]() em rodovias, para diminuir a emissão de poluentes atmosféricos.
em rodovias, para diminuir a emissão de poluentes atmosféricos.
O valor correspondente à energia consumida para que o motorista de um carro econômico, movido a álcool, percorra 400 km na condição de máximo rendimento é mais próximo de
O vinagre é um produto alimentício resultante da fermentação do vinho que, de acordo com a legislação nacional, deve apresentar um teor mínimo de ácido acético (Ch3COOH) de 4% (v/v). Uma empresa está desenvolvendo um kit para que a inspeção sanitária seja capaz de determinar se alíquotas de 1 mL de amostras de vinagre estão de acordo com a legislação.
Esse kit é composto por uma ampola que contém uma solução aquosa de Ca(OH)2 0,1 ![]() e um indicador que faz com que a solução fique cor-de-rosa, se estiver básica, e incolor, se estiver neutra ou ácida. Considere a densidade do ácido acético igual a
e um indicador que faz com que a solução fique cor-de-rosa, se estiver básica, e incolor, se estiver neutra ou ácida. Considere a densidade do ácido acético igual a ![]() a massa molar do ácido acético igual a
a massa molar do ácido acético igual a ![]() e a massa molar do hidróxido de cálcio igual a
e a massa molar do hidróxido de cálcio igual a ![]()
Qual é o valor mais próximo para o volume de solução de Ca(Oh)2, em ml, que deve estar contido em cada ampola do kit para garantir a determinação da regularidade da amostra testada?
Na busca por ouro, os garimpeiros se confundem facilmente entre o ouro verdadeiro e o chamado ouro de tolo, que tem em sua composição 90% de um minério chamado pirita (FeS2). Apesar do engano, a pirita não é descartada, pois é utilizada na produção do ácido sulfúrico, que ocorre com rendimento global de 90%, conforme as equações químicas apresentadas.
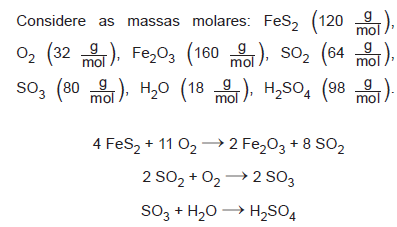
Qual é o valor mais próximo da massa de ácido sulfúrico, em quilograma, que será produzida a partir de 2,0 kg de ouro de tolo?
A equação a seguir sintetiza a reação de combustão entre o salitre, o enxofre e o carvão, substâncias presentes na pólvora.
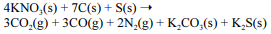
Acerca desse assunto, julgue o próximo item.
A equação apresentada desobedece ao princípio de Lavoisier, uma vez que a massa dos produtos é menor que a massa dos reagentes devido à presença de gases de baixa densidade formados pela reação.
O gás amônia, perigoso aos seres humanos, é de uso comum nas indústrias alimentícias, petroquímicas e metalúrgicas com várias aplicações. Mesmo exigindo o uso adequado de equipamentos de proteção individual e procedimentos de segurança, uma indústria teve o gás amônia recentemente citado em um vazamento de gás que levou centenas de seus funcionários a procurar atendimento médico com sintomas característico de intoxicação. A respeito da produção do gás amônia apresentado na equação a seguir, assinale a alternativa que apresenta o volume do gás NH3 obtido a partir de 12 L de N2(g).
Considere todos os gases nas condições normais de temperatura e pressão (CNTP).
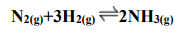
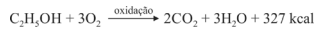
Sabendo que a reação apresentada mostra o processo de oxidação do etanol — em que são liberadas 327 kcal por mol de energia — e que as massas atômicas do carbono, do oxigênio e do hidrogênio são, respectivamente, iguais a 12, 16 e 1, julgue o item a seguir.
A massa de 1 mol de etanol é 46 g
Em condições ideais, pequenas quantidades de gás cloro podem ser geradas em laboratório pela reação do óxido de manganês (MnO2) com ácido clorídrico (HCl), conforme a equação química a seguir não balanceada.
HCl(aq) + MnO2(s) → H2O(L) + MnCl2(s) + Cl2(g)
A partir dessas informações, quantas moléculas de gás cloro, aproximadamente, podem ser produzidas quando 10 g de óxido de manganês com grau de pureza de 87% são colocados para reagir completamente com excesso de ácido clorídrico?
Dado: Número de Avogadro (N) = 6 x 1023
Sabendo-se que a massa molar do ouro (Au) é 197 g mol-1 (gramas por mol), calcule a massa em gramas (g) de 1 átomo desse elemento e assinale a alternativa correta. Utilize o número de Avogadro como sendo 6 x 1023.
As quantidades máximas de oxigênio molecular gasoso e de água líquida que podem ser produzidas na reação de decomposição de 1 litro de uma solução aquosa 0,4 mol.L-1 de peróxido de hidrogênio é:
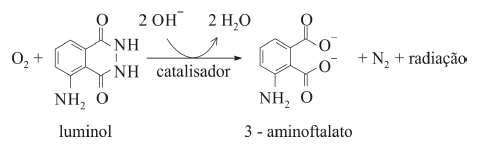
O composto conhecido como luminol é empregado para a detecção de sangue em perícias criminais. Em meio básico, em presença de peróxido de hidrogênio (H 2O2) e de um catalisador adequado, o luminol é oxidado ao ânion 3-aminoftalato, o qual é obtido inicialmente em um estado excitado, mas que rapidamente libera o excesso de energia emitindo radiação na faixa do azul.
A oxidação do luminol é realizada pelo O 2 (g) formado a partir da decomposição do peróxido de hidrogênio (H2O2), de acordo com a equação:
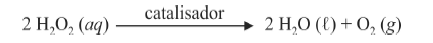
Sem a presença de um catalisador, a decomposição em questão é bastante lenta. Entretanto, o ferro presente na hemoglobina do sangue catalisa a decomposição e o O 2 (g) formado rapidamente oxida o luminol, ocasionando a característica luminescência azul.
Com relação à reação apresentada e às espécies nela envolvidas, e considerando a primeira constante de ionização ácida do H 2O2 igual a 2,4 × 10-12, julgue o item a seguir.
A massa molar da molécula de luminol é superior a 176,0 g/mol.
O ácido nítrico é muito utilizado pela indústria química, principalmente em processos de nitrificação de compostos orgânicos, na fabricação de vernizes, fertilizantes agrícolas, celuloses, salitre (nitrato de potássio), pólvora negra, trinitrotolueno (TNT), nitroglicerina, seda artificial, ácido benzoico, fibras sintéticas, galvanoplastia, ácido pícrico, nylon, entre outros. A produção industrial de ácido nítrico se dá pelo Processo Ostwald, que envolve as seguintes reações químicas:
Supondo-se que o rendimento esperado nesse processo seja de 90% e que a amônia utilizada apresente 20% de impurezas, a massa de amônia, em toneladas, necessária para obtenção de 6,3 t de ácido nítrico será de, aproximadamente:
A equação a seguir sintetiza a reação de combustão entre o salitre, o enxofre e o carvão, substâncias presentes na pólvora.
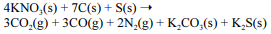
Acerca desse assunto, julgue o próximo item.
A massa molar do composto formado pelo ânion do carbonato de potássio e o cátion do nitrato de alumínio é maior que 250,0 g/mol.
A estimativa de que 70-75% da população mundial podem ser intolerantes à lactose (C12H22O11) levou a uma maior procura por produtos livres desse dissacarídeo naturalmente presente no leite e seus derivados. Esse cenário tem contribuído não apenas com o recente interesse das indústrias de alimentos no desenvolvimento de novos produtos com baixo teor de lactose, mas também impulsionou a recente regulamentação quanto à declaração obrigatória da presença de lactose nos alimentos com mais de 100 miligramas (mg) de lactose para cada 100 gramas ou mililitros do produto. Nesse contexto, assinale a alternativa que apresenta aproximadamente o número de mols de lactose presente em 100 mL de um produto com baixo teor de lactose, contendo 2500 mg de C12H22O11.
(Dados: massas atômicas C=12, H=1, O=16)
Uma mistura de cloreto de cálcio e cloreto de sódio é utilizada para auxiliar no processo de derretimento do gelo em vias públicas de regiões mais frias do Planeta. Um químico, desejando analisar tal mistura, dissolveu 2,4630 g dela em água e precipitou o cálcio com oxalato de sódio. O precipitado foi cuidadosamente filtrado, dissolvido em ácido sulfúrico e titulado com 21,62 mL de solução de permanganato de potássio a 0,10 mol/L. Sabendo que a reação química que ocorre durante a titulação é:
6 H+ + 5 H2C2O4 + 2 MnO4- → 10 CO2 + 2 Mn2+ + 8 H2O
determine a porcentagem em massa de carbonato de cálcio na referida mistura de cloretos.