Oxirredução é um processo em que ocorre transferência de elétrons entre as espécies no decorrer de uma reação química.
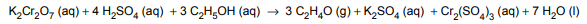
Considerando a reação entre dicromato de potássio (K2Cr2O7) com álcool etílico (C2H5OH) na presença de ácido sulfúrico (H2SO4),
Balanceie as equações químicas de I a V e na sequência assinale a alternativa correta:
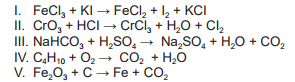
Assinale a alternativa que corresponde aos balanceamentos corretos das equações de I a V, considerando somente os mínimos números inteiros:
Em um laboratório de química analisou-se uma substância orgânica e determinou-se sua composição percentual como segue: C (40,9%), H (4,6%) e O (54,5%). A fórmula mínima da substância é:
Analise as seguintes reações de oxirredução:
I. _ H2 S(g) + _ SO2 (g) → _ S(s) + _ H2 O(l)
II. _ B2 O3 + _ Mg(s) → _ B(s) + _ MgO(s)
A alternativa que representa as equações balanceadas é:
Na determinação de cálcio em águas naturais, a AOAC (Ass°CIation of OfficIal Analytical Chemists/USA) recomenda um
método gravimétrico que consiste em adicionar excesso de ácido oxálico (C2H2O4) a um volume conhecido de amostra e,
em seguida, adicionar a quantidade necessárIa de NH4OH. O precipitado obtido é filtrado, seco, calcinado e pesado, e a
massa de CaO obtida é utilizada para calcular a quantidade de Ca na amostra que, segundo a norma da AOAC, deve ser
expressa como teor de carbonato de cálcio. O método citado é ilustrado pelas equações a seguir. Na análise de uma
amostra de 100,00 mL de água, a massa de CaO obtida foi de 0,2800 g.
Ca+2(aq.) + C2O4-2(aq.) → CaC2O4(s)CaC2O4(s) → CaO(s) + CO + CO2
Dados: Massas molares aproximadas: MM(C2H2O4.2H2O) = 126 g/mol; MM(CaO) = 56 g/mol; MM(CO2) = 44 g/mol, MM(CaCO3) = 100 g/mol;
densidade (H2O) = 1,0 kg/L.
De acordo com os dados apresentados, qual é a concentração de cálcio na amostra de água analisada, expressa em ppm
de CaCO3?
A análise elementar de um composto orgânico resultou em 48,63% de carbono, 43,19% de oxigênio e 8,18% de H. Sabendo-se que o peso molecular desse composto é 222,3 g mol-1, sua fórmula molecular é:
O metano é um dos subprodutos dos aterros sanitários, produzido pela decomposição anaeróbica de resíduos orgânicos. Os produtos de sua combustão são C02 e H2O. Quantos mols de vapor de água podem ser produzidos por 4,0 g de metano?
A pólvora, uma mistura de carvão, salitre e enxofre, foi um dos produtos químicos que tiveram impacto crucial na História da humanidade. A estequiometria da reação de explosão da pólvora pode ser expressa pela reação a seguir:
Os valores dos coeficientes a, b e c, respectivamente, para o correto balanceamento da equação de explosão da pólvora é:
Diversos produtos químicos podem ser utilizados no tratamento da água em ETA’s. As fórmulas químicas que correspondem ao sulfato de alumínio; hipoclorito de cálcio, aluminato de sódio e óxido de cálcio são, respectivamente:
Considerando a decomposição do nitrato
de amônio: NH4 NO3 → X N2 O + Y H2O, os
valores correspondentes a X e Y devem ser,
respectivamente,
Observe a equação da reação química a seguir, onde A, B e
C são valores de coeficientes da equação:
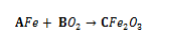
Caso seja feito o balanceamento da equação, os valores
corretos dos coeficientes A, B e C serão:
No processo de floculação em Estações de Tratamento de água, a reação entre o coagulante e a água na presença de cal virgem, forma uma substância gelatinosa, o hidróxido de alumínio (Al(OH)3), que aglutina impurezas formando flocos. A reação da formação deste hidróxido segue abaixo. Assinale a alternativa CORRETA, de acordo com o balanceamento da equação.xAl2(SO4)3 + yH2O → zAl(OH)3 + wH++ vSO42-
Um pilar de extremidades articuladas tem seção transversal quadrada de 2m de comprimento. Esta coluna é constituída de pinho com E = 13GPa e σadm = 12 Mpa para compressão na direção paralela às fibras. Usando um coeficiente de segurança de 2,5 no cálculo da carga crítica de Euler para flambagem, determinar a dimensão, em mm, da seção transversal, de modo que a coluna possa resistir com segurança a uma força de 100KN.
O glifosato é um herbicida não seletivo (mata qualquer tipo de
planta) desenvolvido para matar ervas, principalmente perenes.
Seu efeito no organismo humano é cumulativo e a intensidade da
intoxicação depende do tempo de contato com o produto. O
herbicida pode continuar presente em alimentos num período de
até dois anos após o contato com o produto e em solos por mais
de três anos, dependendo do tipo de solo e clima.
Uma amostra de glifosato 5,07mg apresentou a seguinte
composição: 1,08mg de C; 0,24mg de H; 0,42mg de
N; 0,93mg de P e 2,4mg de O. A fórmula empírica dessa
substância é
Dados: Massa molar H=1g.mol–1 C=12g.mol–1 N=14g.mol–1
O = 16g.mol–1 P = 31g.mol–1
A água mineral e os refrigerantes gaseificados contêm o gás carbônico, que reage com a água, produzindo um meio ácido. O gás carbônico é mais solúvel em água quando submetido a altas pressões. Por esse motivo, se for deixada uma garrafa de refrigerante aberta, parte do gás carbônico escapa, tornando o refrigerante “choco”, ou seja, menos ácido. Esse gás citado também é produzido, quando material rico em carbono entra em combustão. Qual alternativa descreve corretamente a fórmula química e o nome oficial dessa substância?


