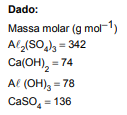Os filmes finos têm sido utilizados em diferentes aplicações como revestimentos óticos e proteção metálica, podendo ser obtidos por meio de diferentes processos.
Os filmes de sílica (SiO2) podem ser obtidos por meio de decomposição de vapor químico. Nesse processo o tetracloreto de silício gasoso (SiCl4) reage com gás hidrogênio (H2) e gás carbônico (CO2). Além do filme de sílica são formados, como subprodutos, os gases cloreto de hidrogênio 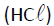 e monóxido de carbono (CO).
e monóxido de carbono (CO).
A transformação química descrita é corretamente representada por:
Um método utilizado para determinar a concentração de ozônio (O3) no ar é passar uma amostra de ar por um borbulhador contendo solução aquosa de iodeto de sódio (NaI). A reação química que ocorre é descrita a seguir.
O3( g) + 2 NaI (aq) + H2O () O2 (g) + I2 (s) + 2 NaOH (aq)
Ao passar uma amostra de ar por um borbulhador, verificou-se o consumo de 1,5 mg de iodeto de sódio. A massa de ozônio, em mg, presente nessa amostra era de
[Massa Molares (g.mol–1): H = 1,0; I = 127,0; O = 16,0; Na = 23,0]
Um marceneiro esqueceu um pacote de pregos ao relento, expostos à umidade do ar e à chuva. Com isso, os pregos de ferro, que tinham a massa de 5,6 g cada, acabaram cobertos por uma camada espessa de ferrugem (Fe2O3•H2O), uma substância marrom insolúvel, produto
da oxidação do ferro metálico, que ocorre segundo a equação química:
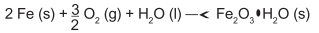
Considere as massas molares (g/mol): H = 1; O = 16; Fe = 56.
Qual foi a massa de ferrugem produzida ao se oxidar a metade (50%) de um prego?
A obtenção de etanol utilizando a cana-de-açúcar envolve a fermentação dos monossacarídeos formadores da sacarose contida no melaço. Um desses formadores é a glicose (C H O ), cuja fermentação produz cerca de 50 g de etanol a partir de 100 g de glicose, conforme a equação química descrita.
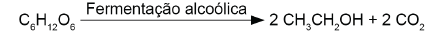
Em uma condição específica de fermentação, obtém-se 80% de conversão em etanol que, após sua purificação, apresenta densidade igual a 0,80 g/mL. O melaço utilizado apresentou 50 kg de monossacarídeos na forma de glicose.
O volume de etanol, em litro, obtido nesse processo é mais próximo de
A obtenção de etanol utilizando a cana-de-açúcar envolve a fermentação dos monossacarídeos formadores da sacarose contida no melaço. Um desses formadores é a glicose (C6H12O6), cuja fermentação produz cerca de 50 g de etanol a partir de 100 g de glicose, conforme a equação química descrita.
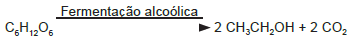
Em uma condição específica de fermentação, obtém-se 80% de conversão em etanol que, após sua purificação, apresenta densidade igual a 0,80 g/mL. O melaço utilizado apresentou 50 kg de monossacarídeos na forma de glicose.
O volume de etanol, em litro, obtido nesse processo é mais próximo de
O volume de etanol, em litro, obtido nesse processo é mais próximo de
A equação obtida a partir da relação entre as equações de Planck e de Balmer-Bohr que pode ser usada para calcular a energia associada ao salto quântico de elétrons mediante a sua excitação energética e que melhor expressa o salto de um elétron da primeira camada para a quarta camada eletrônica de um certo átomo e que foi responsável por emissão de luz de um comprimento especifico de onda. Sabendo-se que h representa a constante de Planck; c , a velocidade da luz e Rh a constante de Rydberg, a equação adequada será:
No livro Desespero, de Stephen King, um dos personagens faz a seguinte afirmação: “A gente tira o cobre da terra com ácido sulfúrico. A melhor maneira de aplicar é com esguichos... parecem grandes molhadores de grama."
Considerando que uma amostra de 2,0 kg, contendo 80% de óxido de cobre II, foi utilizada para reagir com o ácido citado no livro de Stephen King. Admitindo que os outros compostos da amostra não reagem com o ácido, determine a massa aproximada de ácido necessária para que todo o cobre da amostra sofra reação química. Considere as seguintes massas molares em g.mol-1 : Cu = 63,5; O = 16; H = 1 e S = 32.
Um dispositivo analítico, conforme ilustrado na figura precedente, baseado em papel microfluídico (μPAD), foi desenvolvido para a determinação in loco da presença de chumbo, bário, antimônio, ferro, alumínio, zinco e magnésio, em resíduos de explosivos pirotécnicos. Cada canal contém um conjunto específico de reagentes que produz uma mudança de cor após a interação com um sal de metal específico, conforme esquematizado na tabela anterior. Esse novo dispositivo deve ser útil na detecção in loco de resíduos pós-explosão de pirotecnia no campo, devido à sua portabilidade e facilidade de uso.
Tendo como referência a figura e os dados da tabela precedentes, julgue o item a seguir
Na queima do magnésio metálico em presença de oxigênio, ocorre a redução do magnésio com o consequente consumo de 1 mol de elétrons por mol de átomos de magnésio.
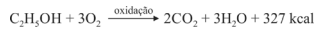
Sabendo que a reação apresentada mostra o processo de oxidação do etanol — em que são liberadas 327 kcal por mol de energia — e que as massas atômicas do carbono, do oxigênio e do hidrogênio são, respectivamente, iguais a 12, 16 e 1, julgue o item a seguir.
A massa de 1 mol de etanol é 46 g
As indústrias de cerâmica utilizam argila para produzir artefatos como tijolos e telhas. Uma amostra de argila contém 45% em massa de sílica (SiO2) e 10% em massa de água (H2O). Durante a secagem por aquecimento em uma estufa, somente a umidade é removida.
Após o processo de secagem, o teor de sílica na argila seca será de
Objetos de prata sofrem escurecimento devido à sua reação com enxofre. Estes materiais recuperam seu brilho característico quando envoltos por papel alumínio e mergulhados em um recipiente contendo água quente e sal de cozinha.
A reação não balanceada que ocorre é:

Utilizando o processo descrito, a massa de prata metálica que será regenerada na superfície de um objeto que contém 2,48 g de Ag2S é
Nas estações de tratamento de água, uma das principais etapas para obtenção de água potável consiste na eliminação das impurezas que se encontram em suspensão, que pode ser realizada a partir da adição de sulfato de alumínio, A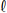
Em um teste piloto de tratamento de 0,50 m3 de água, foram adicionados 3,42 kg de sulfato de alumínio e 0,50 kg de hidróxido de cálcio. Admitindo que não haja variação de volume é correto afirmar que
A concentração de ácido fluorsilícico, H2SiF6, em mg/L, necessária para se obter o teor de 1,2 mg/L de íons fluoreto na água é igual a
Dados:
Massas molares (g/mol)
H = 1
Si = 28
F = 19

Um dispositivo analítico, conforme ilustrado na figura precedente, baseado em papel microfluídico (μPAD), foi desenvolvido para a determinação in loco da presença de chumbo, bário, antimônio, ferro, alumínio, zinco e magnésio, em resíduos de explosivos pirotécnicos. Cada canal contém um conjunto específico de reagentes que produz uma mudança de cor após a interação com um sal de metal específico, conforme esquematizado na tabela anterior. Esse novo dispositivo deve ser útil na detecção in loco de resíduos pós-explosão de pirotecnia no campo, devido à sua portabilidade e facilidade de uso.
Tendo como referência a figura e os dados da tabela precedentes, julgue o item a seguir
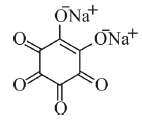
Considere que na reação do bário com o rodizonato de sódio, mostrado na figura a seguir, haja apenas troca de cátions para gerar a coloração laranja. Nessa situação, para formar o composto rodizonato de bário, serão necessários mais de 1.000 μg de rodizonato de sódio para reagir totalmente com 1.306,5 μg de nitrato de bário.
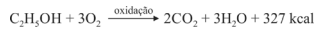
Sabendo que a reação apresentada mostra o processo de oxidação do etanol — em que são liberadas 327 kcal por mol de energia — e que as massas atômicas do carbono, do oxigênio e do hidrogênio são, respectivamente, iguais a 12, 16 e 1, julgue o item a seguir.
Para cada mol de água produzido, a energia liberada é de 109 kcal.