O teor de Fe2+ em uma solução pode ser determinado por titulação com uma solução oxidante de KMnO4. A reação de oxirredução não balanceada é MnO4- + Fe2+→ Mn2+ + Fe3+. Após o balanceamento dessa reação, com quantos mols de Fe2+ reage 1 mol de MnO4-?
Em estudo recente, pesquisadores da Embrapa mostraram
que a pecuária brasileira pode ser uma arma no combate ao
aquecimento global. De acordo com esse estudo, um boi
emite em média cerca de 0,4 toneladas de carbono, mas seu
consumo é de aproximadamente 2,5 toneladas. A 25 °C e 1
atm, qual é o volume de metano que deixa de ir (fixado
pelo animal) para atmosfera?
Considere que todo carbono é proveniente
de metano, que os gases são perfeitos e que
R = 0,0082 L atm K-1 mol-1.
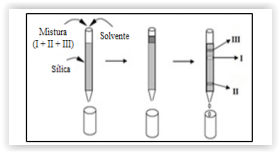
O esquema a seguir mostra a separação cromatográfica das
substâncias I, II e III, utilizando sílica (Si02) como fase
estacionária. Cada faixa representa uma substância.
A mistura analisada é composta de substâncias, com pesos
moleculares equivalentes, das classes: álcool, amina e
hidrocarboneto. Com base nestas informações, as
substâncias I, II e III representam, respectivamente,
compostos das classes:
A análise elementar de um composto orgânico resultou em 48,63% de carbono, 43,19% de oxigênio e 8,18% de H. Sabendo-se que o peso molecular desse composto é 222,3 g mol-1, sua fórmula molecular é:
O metano é um dos subprodutos dos aterros sanitários, produzido pela decomposição anaeróbica de resíduos orgânicos. Os produtos de sua combustão são C02 e H2O. Quantos mols de vapor de água podem ser produzidos por 4,0 g de metano?
Em um experimento, para determinar a massa atômica de um elemento, foi constatado que a massa determinada era 140 vezes mais pesada do que um átomo de hidrogênio. Sabendo que o número de prótons é igual a 59, determine o número de átomos em um 1 kg de amostra desse elemento:Considere que a massa do próton é igual à massa do nêutron e vale 1,7 x 10-27 kg.
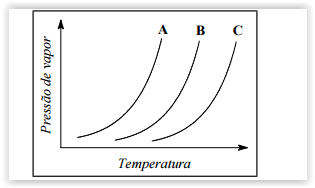
Em uma aula experimental de química, três soluções foram
submetidas à destilação. O gráfico a seguir representa o
comportamento dessas soluções.
Este gráfico evidencia o ponto de ebulição
O processo de oxidação de minérios é comumente empregado
para reduzir seu teor de carbono. Desse modo, qual é a massa
de oxigênio, em kg, necessária para reduzir o teor de carbono
de 5% para 2% em 50 toneladas de minério?
Considere que apenas o dióxido
de carbono é produzido
No processo de mineração do minério de ferro, aminas de éter são empregadas para separar a sílica do minério de ferro. Dentre as alternativas a seguir, a que contém a fórmula molecular de um éter de amina primária é:
Numa aula de Química experimental, o objetivo é determinar a densidade de um sólido metálico poroso, no formato de uma pirâmide irregular. Para alcançar esse objetivo, da forma mais simplificada possível, deve-se:
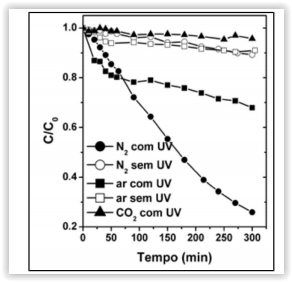
A figura a seguir, adaptada da revista Quim. Nova, v. 38,
1265-1272, 2015, representa o processo de degradação
fotocalítica do azul de metileno obtida com uma amostra de
CaFe em diferentes condições.
Com base nessa figura, a condição na qual a velocidade inicial
é maior é:
Gás hidrogênio pode ser produzido industrialmente a partir
de metano pela reação química CH4(g ) + H2O(g )→ CO(g )
+ 3H2(g ). Qual será o volume, em litros, de gás hidrogênio
produzido ao reagir 1000 L de metano com 500 L de vapor
d’água à 700 oC e 3 atm?
Considere os gases como perfeitos e
R = 0,0082 L atm K-1 mol-1
A constante de acidez do ácido fluorídrico em meio aquoso é 3,5 x 10-4, a 25 °C. Qual é a concentração da solução desse ácido, em mol l-1, que em pH = 3 produz 0,2 mol l-1 de fluoreto?
Em um experimento visando determinar a polaridade de alguns compostos, observou-se que as moléculas de C02, NH3 e BF3 têm diferentes momentos de dipolo. A relação de polaridade entre esses compostos é: