Sabendo–se que a 20 ºC e pressão atmosférica, a massa de 998,204 kg de água ocupa um volume de 1 m3. Dado que a massa molar da água é igual a 18,02 kg/kmol, para uma vazão volumétrica de 100 m3/h escoando em uma tubulação com área transversal de 0,020 m2, o fluxo molar dessa corrente de água expressoemkmol / (s.m2) será:
Opoder calorífico inferior é aquele em que:
Considerando constante a entalpia de um gás durante a expansão de Joule–Thomson (J–T), o coeficiente de Joule–Thomson pode ser definido como o valor limite da relação (numerador / denominador, nesta ordem) entre:
Para que um sistema se encontre em equilíbrio, o potencial químico deverá:
Considerando água fluindo a 3 g/s por um calorímetro de escoamento. Neste processo são gastos 15 000 Watts de potência térmica para evaporar completamente a água. Sendo desprezíveis as variações de altura e velocidade, e sabendo que a água encontra–se inicialmente a 0 ºC, com a entalpia em estado inicial igual a zero e em seu estado final definido por pressão a 3 bar e temperatura de 300 ºC, sua entalpia do vapor será:
O número de Nusselt representa, para a camada limite térmica, o que o coeficiente de atrito representa para a camada limite fluidodinâmica. Esse parâmetro de similaridade sugere:
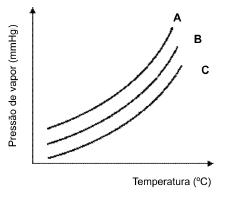
A variação da pressão de vapor, em mmHg, de três
amostras líquidas A, B e C com a temperatura, em ºC,
é mostrada no gráfico que segue.
Analise as afirmativas feitas sobre as amostras.
I. Colocando−se uma gota de cada amostra em
diferentes pontos de um tecido, a amostra A
vaporizará mais rápido.
II. A temperatura de ebulição da amostra B é maior
que da amostra C.
III. As forças intermoleculares na amostra C são,
provavelmente, mais intensas que na amostra A.
IV. Se as amostras forem de água, acetona e álcool,
então pode−se fazer a seguinte associação:
A= água, B= álcool eC= acetona.
V. Se as interações intermoleculares nas amostras
são do mesmo tipo, a molécula da substância da
amostra A é, provavelmente, mais pesada que a
de C.
A alternativa que só contém afirmações verdadeiras
é:
Conforme artigo 5º da Constituição Federal vigente,
são exemplos de direitos e garantias fundamentais:
As informações consideradas ultrassecretas pela Lei
de Acesso à Informação (Lei nº 12.527/2011) têm
prazo máximo de sigilo, contado da data de sua
produção, de:
Considerando a lei dos gases ideais, a temperatura máxima que a massa de 19,9 kg de argônio (massa molar = 39,8 kg / kmol) contida em um recipiente de 1 m pode ser aquecida sem que a pressão manométrica exceda 15 kgf/cm2 será: Dado: Cons tante uni ver sal dos gases , R= 8,3 kJ/(kmol*K)
Sobre o segundo princípio da termodinâmica é correto afirmar que:
Considerando um corpo maciço de 1 kg abandonado em queda de uma altura de 100 metros. Admitindo que não há troca de energia entre este corpo e as suas vizinhanças e considerando a gravidade como 9,81 m/s2 , a energia potencial deste corpo, no exato momento do abandono em relação à base da queda, será:
Areação de reforma a vapor do metano é utilizada em diversos processos químicos na indústria e consiste na reação de vapor d'água com metano em fase gasosa produzindo os gases monóxido de carbono e hidrogênio. Considerando que esta reação encontrase em equilíbrio, para 5 mols de vapor d'água consumidos durante a reunião será(ão) produzido(s):
Água (1000 kg/m3) é bombeada de um tanque para outro a uma distância de 300 metros. O nível de água no segundo tanque está a 40 metros acima do nível do primeiro. Considerando a força gravitacional local de 9,8 m/s2, o aumento da energia potencial específica da água, expresso em J/kg, será:
Conforme a Lei n° 8.429/1992 (Lei de Improbidade Administrativa) se um agente público deixa de praticar, indevidamente, um ato de ofício, sua conduta: