A tabela lista os valores de pH de algumas bebidas consumidas pela população.

Das bebidas listadas na tabela, aquela com menor potencial de desmineralização dos dentes é o
O bisfenol-A é um composto que serve de matéria-prima para a fabricação de polímeros utilizados em embalagens plásticas de alimentos, em mamadeiras e no revestimento interno de latas. Esse composto está sendo banido em diversos países, incluindo o Brasil, principalmente por ser um mimetizador de estrógenos (hormõnios) que, atuando como tal no organismo, pode causar infertilidade na vida adulta. O bisfenol-A (massa molar igual a 228 g/mol) é preparado pela condensação da propanona (massa molar igual a 58 g/mol) com fenol (massa molar igual a 94 g/mol), em meio ácido, conforme apresentado na equação química.
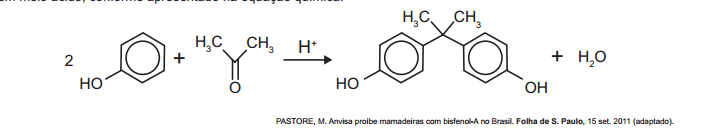
PASTORE, M. Anvisa proíbe mamadeiras com bisfenol-A no Brasil. Folha de S. Paulo, 15 set. 2011 (adaptado).
Considerando que, ao reagir 580 g de propanona com 3 760 g de fenol, obteve-se 1,14 kg de bisfenol-A, de acordo com a reação descrita, o rendimento real do processo foi de
A formação de estalactites depende da reversibilidade de uma reação química. O carbonato de cálcio (CaCO3) é encontrado em depósitos subterrãneos na forma de pedra calcária. Quando um volume de água rica em CO2 dissolvido infiltra-se no calcário, o minério dissolve-se formando íons Ca2+ e HCO3. Numa segunda etapa, a solução aquosa desses íons chega a uma caverna e ocorre a reação inversa, promovendo a liberação de CO2 e a deposição de CaCO3' de acordo com a equação apresentada.

Considerando o equilíbrio que ocorre na segunda etapa, a formação de carbonato será favorecida pelo(a)
Com o objetivo de substituir as sacolas de polietileno, alguns supermercados têm utilizado um novo tipo de plástico ecológico, que apresenta em sua composição amido de milho e uma resina polimétrica termoplástica, obtida a partir de uma fonte petroquímica.
ERENO, D. Plásticos de vegetais. Pesquisa Fapesp, n° 179, jan 2011 (adaptado)
Nesses plásticos, a fragmentação da resina polimérica é facilitada porque os carboidratos presentes:
A liberação dos gases clorofluocarbonos (CFCs) na atmosfera pode provocar depleção de ozônio (O3) na estratosfera. O ozônio estratosférico é responsável por absorver parte da radiação ultravioleta emitida pelo Sol, a qual é nociva aos seres vivos. Esse processo, na camada de ozônio, é ilustrado simplificadamente na figura.
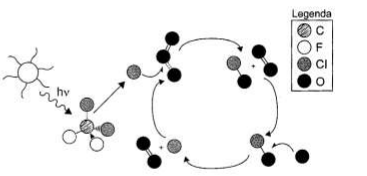
Quimicamente, a destruição do ozônio na atmosfera por gases CFCs é decorrência da
A capacidade de limpeza e a eficiência de uma sabão dependem de sua propriedade de formar micelas estáveis, que arrastam com facilidade as moléculas impregnadas no material a ser limpo. Tais micelas têm em sua estrutura partes capazes de interagir com substâncias polares, como a água, e partes que podem interagir com substâncias apolares, como as gorduras e os óleos.
SANTOS, W. I. P.; MÓL, G. G. (Coords.) Química e sociedade São Paulo: Nova Geração, 2005 (adaptado).
A substância capaz de formar as estruturas mencionadas é
A forma das moléculas, como representadas no papel, nem sempre é planar. Em um determinado fármaco, a moléculas contendo um grupo não planar é biologicamente ativa, enquanto moléculas contendo substituintes planares são inativas.
O grupo responsável pelo bioatividade desse fármaco é
Visando minimizar impactos ambientais, a legislação brasileira determina que resíduos químicos lançados diretamente no corpo receptor tenham pH entre 5,0 e 9,0. Um resíduo líquido aquoso gerado em um processo industrial tem concentração de íons hidroxila igual a 1,0 x 10-10 mol/L. Para atender a legislação, um químico separou as seguintes substâncias, disponibilizadas no almoxarifado da empresa: CH3COOH, Na2SO4, CH3OH, K2CO3 e NH4Cl.
Para que o resíduo possa ser lançado diretamente no corpo receptor, qual substância poderia ser empregada no ajuste do pH?
A baunilha a uma espécie de orquídea. A partir de sua flor, a produzida a vanilina (conforme representação química),
que da origem ao aroma de baunilha.

Na vanilina estão presentes as funções orgânicas
O cianeto de sódio, NaCN, e um poderoso agente complexante, usado em laboratórios químicos e em indústria de extração de ouro.
Quando uma indústria lança NaCN solido nas águas de um rio, ocorre o seguinte equilíbrio químico:

Esse equilíbrio químico é decorrente de uma reação de
As antocianinas (componente natural de frutas roxas, como uva e açaí) são moléculas interessantes para a produção de embalagens inteligentes,
pois tem capacidade de mudar de cor, conforme muda o pH. Em soluções com pH abaixo de 3,0, essas moléculas apresentam uma coloração do laranja
ao vermelho mais intenso. com o aumento do pH para a faixa de 4,0 a 5,0, a coloração vermelha tende a desaparecer. E aumentos adicionais de pH
levam as antocianinas a apresentarem uma coloração entre o verde e o azul.
Disponível em: www.biotecnologia.com.br. Acesso em: 25 nov. 2011 (adaptado).
Estas embalagens são capazes de identificar quando o alimento esta em decomposição, pois se tornam
A água potável precisa ser límpida, ou seja, não deve conter partículas em suspensão, tais como terra ou restos de plantas, comuns nas águas de rios e lagoas. A remoção das partículas é feita em estações de tratamento, onde Ca(OH)2 em excesso e Al2(SO4)3 são adicionados em um tanque para formar sulfato de cálcio e hidróxido de alumínio. Esse último se forma como flocos gelatinosos insolúveis em água, que são capazes de agregar partículas em suspensão. Em uma estação de tratamento, cada 10 gramas de hidróxido de alumínio é capaz de carregar 2 gramas de partículas.
Após decantação e filtração, a água límpida é tratada com cloro e distribuída para as residências. As massas molares dos elementos H, O, AI, S e Ca são, respectivamente, 1 g/mol, 16 g/mol, 27 g/mol, 32 g/mol e 40 g/mol.
Considerando que 1 000 litros da água de um rio possuem 45 gramas de partículas em suspensão, a quantidade mínima de Al2(SO4)3 que deve ser utilizada na estação de tratamento de água, capaz de tratar 3 000 litros de água de uma só vez, para garantir que todas as partículas em suspensão sejam precipitadas, é mais próxima de
Água dura é aquela que contém concentrações relativamente altas de íons Ca2+ e Mg2+ dissolvidos. Apesar de esses íons não representarem risco para a saúde, eles podem tornar a água imprópria para alguns tipos de consumo doméstico ou industrial. Objetivando reduzir a concentração de íons Ca2+ e Mg2+ de uma amostra de água dura ao mínimo possível, um técnico em química testou os seguintes procedimentos no laboratório:
I — Decantação da amostra de água
II — Filtração da amostra de água.
III — Aquecimento da amostra de água.
IV — Adição do solvente orgânico CCl4 à amostra de água.
V — Adição de CaO e Na2CO3 à amostra de água. BROWN, T. L. et al. Química, a ciência central. São Paulo: Pearson Prentice Hall, 2005 (adaptado).
O método considerado viável para tratar a água dura e aumentar seu potencial de utilização é o(a)
O cobre, muito utilizado em fios da rede elétrica e com considerável valor de mercado, pode ser encontrado na natureza na forma de calcocita, Cu2S (s), de massa molar 159 g/mol. Por meio da reação Cu2S (s) + 02 (g) -> 2 Cu (s) + S02 (g), é possível obtê-lo na forma metálica. A quantidade de matéria de cobre metálico produzida a partir de uma tonelada de calcocita com 7,95% (m/m) de pureza é
Fertilizantes químicos mistos, denominados NPK, são utilizados para aumentar a produtividade agrícola, por fornecerem os nutrientes nitrogênio, fósforo e potássio, necessários para o desenvolvimento das plantas. A quantidade de cada nutriente varia de acordo com a finalidade do adubo. Um determinado adubo NPK possui, em sua composição, as seguintes substãncias: nitrato de amõnio (NH4NO3), ureia (CO(NH2)2) nitrato de potássio (KNO3), fosfato de sódio (Na3PO4) e cloreto de potássio (KCI).
A adição do adubo descrito provocou diminuição no pH de um solo. Considerando o caráter ácido/básico das substãncias constituintes desse adubo, a diminuição do pH do solo deve ser atribuída à presença, no adubo, de uma quantidade significativa de

