O biodiesel é um biocombustível obtido a partir de fontes renováveis, que surgiu como alternativa ao uso do diesel de petróleo para motores de combustão interna. Ele pode ser obtido pela reação entre triglicerídeos, presentes em óleos vegetais e gorduras animais, entre outros, e álcoois de baixa massa molar, como o metanol ou etanol, na presença de um catalisador, de acordo com a equação química:
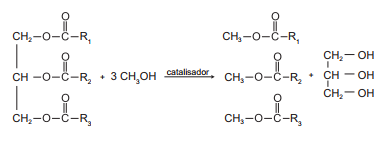
A função química presente no produto que representa o biodiesel é
Em meados de 2003, mais de 20 pessoas morreram no Brasil após terem ingerido uma suspensão de sulfato de bário utilizada como contraste em
exames radiológicos. O sulfato de bário é um sólido pouquíssimo solúvel em água, que não se dissolve mesmo na presença de ácidos. As mortes
ocorreram porque um laboratório farmacêutico forneceu o produto contaminado com carbonato de bário, que é solúvel em meio ácido.Um
simples teste para verificarexistência de íons bário solúveis poderia ter evitado a tragédia. Esse teste consiste em tratar a amostra com
solução
aquosa de HCI e, após filtrar para separar os compostos insolúveis de bário, adiciona-se solução aquosa de H2SO4
sobre o filtrado e observa-se por 30 min.
TUBINO, M ; SIMONI, J.A. Refletindo sobre o caso [email protected]ímica Nova, n. 2, 2007 (adaptado).
A presença de íons bário solúveis na amostra é indicada pela
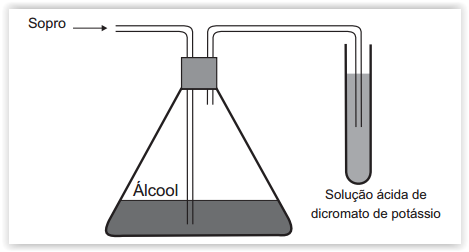
Um bafômetro simples consiste em um tubo contendo uma mistura sólida de dicromato de potássio em sílica umedecida com ácido sulfúrico. Nesse teste, a detecção da embriaguez por consumo de álcool se dá visualmente, pois a reação que ocorre é a oxidação do álcool a aldeído e a redução do dicromato (alaranjado) a cromo(III) (verde) ou cromo(II) (azul).
A equação balanceada da reação química que representa esse teste é:
Na preparação da massa do pão, presente na mesa do café da maioria dos brasileiros, utiliza-se o fungo Saccharomyces cerevisiae vivo, contido no fermento. Sua finalidade é fazer com que a massa cresça por meio da produção de gás carbônico.
Esse processo químico de liberação de gás é causado pela
Os métodos empregados nas análises químicas
são ferramentas importantes para se conhecer a
composição dos diversos materiais presentes no meio
ambiente. É comum, na análise de metais presentes
em amostras ambientais, como água de rio ou de
mar, a adição de um ácido mineral forte, normalmente
o ácido nítrico (HNO3), com a finalidade de impedir a
precipitação de compostos pouco solúveis desses
metais ao longo do tempo.
Na ocorrência de precipitação, o resultado da análise
pode ser subestimado, porque
O cianeto de sódio, NaCN, e um poderoso agente complexante, usado em laboratórios químicos e em indústria de extração de ouro.
Quando uma indústria lança NaCN solido nas águas de um rio, ocorre o seguinte equilíbrio químico:

Esse equilíbrio químico é decorrente de uma reação de
Grandes fontes de emissão do gás dióxido de enxofre são as indústrias de extração de cobre e níquel, em decorrência da oxidação dos minérios sulfurados. Para evitar a liberação desses óxidos na atmosfera e a consequente formação da chuva ácida, o gás pode ser lavado, em um processo conhecido como dessulfurização, conforme mostrado na equação (1).
CaCO3(s) + SO2 (g) à CaSO3 (s) + CO2 (g) (1)
Por sua vez, o sulfito de cálcio formado pode ser oxidado, com o auxílio do ar atmosférico, para obtenção do sulfato de cálcio, como mostrado na equação (2). Essa etapa e de grande interesse porque o produto da reação, popularmente conhecido como gesso, é utilizado para fins agrícolas.
2 Ca SO3 (s) + O2 (g) à 2 CaSO4 (s) (2)
As massas molares dos elementos carbono, oxigênio, enxofre e cáclcio são iguais a 12g/mol, 16g/mol, 32g/mol e 40g/mol, respectivamente.
BAIRD, C. Química Ambiental. Porto Alegre: Bookman, 2002 (adaptado).
Considerando um rendimento de 90% no processo, a massa de gesso obtida, em gramas, por mol de gás retido é mais próxima de
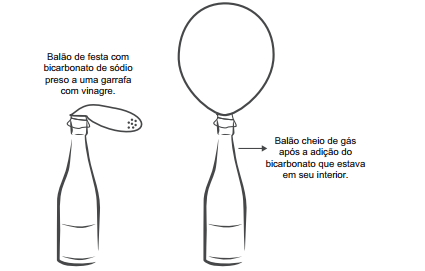
A transformação química em questão é representada pela equação:
Uma das etapas do tratamento da água é a desinfecção, sendo a cloração o método mais empregado. Esse método consiste na dissolução do gás cloro numa solução sob pressão e sua aplicação na água a ser desinfetada. As equações das reações químicas envolvidas são:
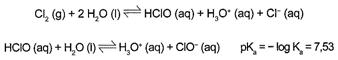
A ação desinfetante é controlada pelo ácido hipocloroso, que possui um potencial de desinfecção cerca de 80 vezes superior ao ânion hipoclorito. O pH do meio é importante, porque influencia na extensão com que o ácido hipocloroso se ioniza.
Para que a desinfecção seja mais efetiva, o pH da água a ser tratada deve estar mais próximo de:
O mármore é um material empregado para revestimento de pisos e um de seus principais constituintes é o
carbonato de cálcio. Na limpeza desses pisos com solução ácida, ocorre efervescência.
Nessa efervescência o gás liberado é o
Para preparar uma massa básica de pão, deve–se
misturar apenas farinha, água, sal e fermento. Parte do
trabalho deixa–se para o fungo presente no fermento: ele
utiliza amido e açúcares da farinha em reações químicas
que resultam na produção de alguns outros compostos
importantes no processo de crescimento da massa. Antes
de assar, é importante que a massa seja deixada num
recipiente por algumas horas para que o processo de
fermentação ocorra.
Esse período de espera é importante para que a massa
cresça, pois é quando ocorre a
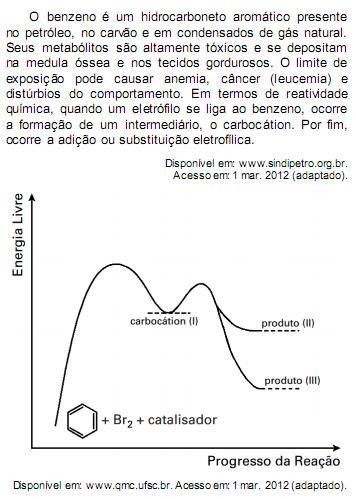
Com base no texto e no gráfico do progresso da reação apresentada, as estruturas químicas encontradas em I, II e III são, respectivamente:
O rótulo de um desodorante aerossol informa ao consumidor que o produto possui em sua composição os gases isobutano, butano e propano, dentre outras substâncias. Além dessa informação, o rótulo traz, ainda, a inscrição Não contém CFC. As reações a seguir, que ocorrem na estratosfera, justificam a não utilização de CFC (clorofluorcarbono ou Freon) nesse desodorante:
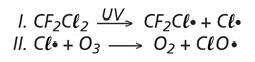
A preocupação com as possíveis ameaças à camada de ozônio (O3) baseia-se na sua principal função: proteger a matéria viva na Terra dos efeitos prejudiciais dos raios solares ultravioleta. A absorção da radiação ultravioleta pelo ozônio estratosférico é intensa o suficiente para eliminar boa parte da fração de ultravioleta que é prejudicial à vida.
A finalidade da utilização dos gases isobutano, butano e propano neste aerossol é
Os tubos de PVC, material organoclorado sintético, são normalmente utilizados como encanamento na construção civil. Ao final da sua vida útil, uma das formas de descarte desses tubos pode ser a incineração. Nesse processo libera-se 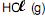 , cloreto de hidrogênio, dentre outras substâncias. Assim, é necessário um tratamento para evitar o problema da emissão desse poluente.
, cloreto de hidrogênio, dentre outras substâncias. Assim, é necessário um tratamento para evitar o problema da emissão desse poluente.
Entre as alternativas possíveis para o tratamento, é apropriado canalizar e borbulhar os gases provenientes da incineração em
A explosão de uma plataforma de petróleo em frente à costa americana e o vazamento de cerca de mil barris de petróleo por dia no mar provocaram um desastre ambiental. Uma das estratégias utilizadas pela Guarda Costeira para dissipar a mancha negra foi um recurso simples: fogo. A queima da mancha de petróleo para proteger a costa provocará seus próprios problemas ambientais, criando enormes nuvens de fumaça tóxica e deixando resíduos no mar e no ar.
HIRST, M. Depois de vazamento, situação de petroleira britânica se complica. BBC. Disponível em: http://www.bbc.co.uk. Acesso em: 1 maio 2010 (adaptado).
Além da poluição das águas provocada pelo derramamento de óleo no mar, a queima do petróleo provoca a poluição atmosférica formando uma nuvem negra denominada fuligem, que é proveniente da combustão