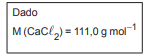O esgoto doméstico é uma das principais fontes de poluentes orgânicos despejados nos corpos d'água.
Se a quantidade de matéria orgânica e de microrganismos aeróbios no esgoto for alta, a diminuição da concentração de oxigênio dissolvido no meio provocará alterações no ambiente aquático.
A quantidade de oxigênio necessária para o consumo da matéria orgânica pode ser avaliada em laboratório, utilizando o excesso do reagente
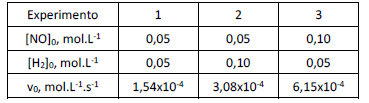
As velocidades iniciais (v0) da reação
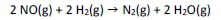
foram determinadas em diferentes experimentos, nos quais as concentrações iniciais dos reagentes ([NO] 0 e [H2]0) eram variadas.
Os resultados estão resumidos na tabela a seguir.
Nas condições deste experimento, a lei de velocidade da reação é
Fluidos não newtonianos são aqueles em que a relação entre tensão de cisalhamento e taxa de deformação é não linear.
Um exemplo de fluido não newtoniano é a tinta, que é muito viscosa ao ser retirada da lata, porém, ao ser aplicada na parede, a camada de tinta formada é submetida a uma grande tensão de cisalhamento, diminuindo sua viscosidade aparente.
Este comportamento é característico dos fluidos
A figura mostra um Tubo de Pitot que foi colocado em um tubo horizontal por onde escoa um fluido incompressível de densidade 5x102 kg.m -3.
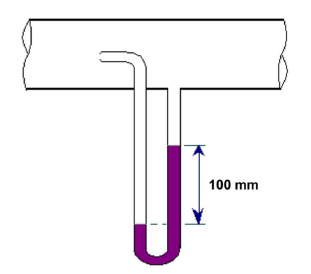
Considerando a densidade relativa do fluido manométrico como 2,75 e desprezando o atrito, a velocidade de escoamento do fluido, em m.s -1, é:
Dados: densidade (H2O) = 1000 kg.m -3; g = 10 m.s-2.
Com relação aos materiais utilizados nos laboratórios de ensino de química e às normas de segurança laboratoriais, julgue o item subsequente.
As pipetas, se comparadas às provetas e aos béqueres, são as vidrarias adequadas para medir volume de líquidos com maior precisão.
Uma bola de massa M é lançada verticalmente para cima, de uma altura de H0 a partir do solo chegando a uma altura máxima H. Devido à ação da gravidade, cuja aceleração é g, depois de algum tempo após o lançamento, a bola atinge o solo.
Qual foi o trabalho realizado pela força gravitacional sobre a bola entre o lançamento e o instante em que esta atinge o solo?
Um número adimensional muito importante para o estudo de fluidos em movimento é o Número de Reynolds (Re). Ele é construído a partir dos valores da densidade do fluido ρ (em kg/m 3), da velocidade típica do fluido V (em m/s), da viscosidade do fluido μ (em Pa.s) e de um comprimento típico do problema L (em m).
A forma correta do número de Reynolds será dada por
Na seção transversal retangular de uma viga sob flexão, atuam um momento fletor M e uma força cisalhante V, conforme mostrado na Figura abaixo.
Em decorrência desses esforços internos, a tensão normal máxima de tração e a tensão cisalhante máxima atuam, respectivamente, nos pontos da seção sobre a
Um motor, quando não está devidamente lubrificado, possui um rendimento η =1/3, liberando uma certa quantidade de calor Q0 quando em funcionamento. Quando corretamente lubrificado, seu rendimento aumenta em 30%.
Nessas condições, a nova quantidade de calor liberada pelo motor será
Durante um processo termodinâmico de expansão em um gás, observa-se que TV2 = constante, onde T é a temperatura, e V é o volume do gás. O trabalho realizado na expansão entre V0 e 2V0 é W1 , e o trabalho realizado na expansão entre 2V0 e 3V0 é W2.
Se é válida a relação dos gases ideais, pV = nRT, qual a razão W2/W1?
Uma massa igual a 5,5 g de cloreto de cálcio (CaC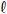
O valor mais aproximado da concentração de cloreto, em quantidade de matéria (mol L-1), na solução de trabalho é
A seguir são apresentadas informações referentes à reação de decomposição do H 2O2.
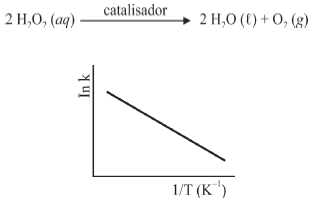
A figura precedente mostra o gráfico do logaritmo neperiano da constante de velocidade k da reação em função do recíproco da temperatura, sendo que a equação que descreve a reta obtida é y = 30 - 3,0 × 10 4 x.
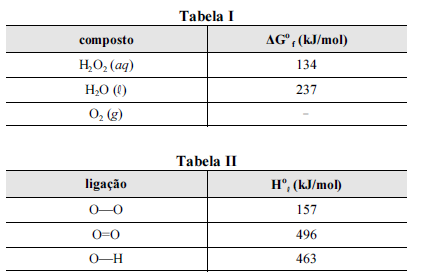
Nas tabelas I e II são apresentadas, para uma temperatura de 25 ºC, as energias livres de Gibbs padrão de formação (ΔGº f) para as espécies envolvidas na reação e algumas entalpias padrão de ligação (Hº l), respectivamente.
Considerando que a reação de decomposição do H 2O2 seja exotérmica e se processe de acordo com uma cinética de primeira ordem, e que a constante universal dos gases seja igual a 8,3 J × mol-1 × K-1, julgue os itens subsequentes, acerca da reação em questão.
As entalpias padrão de ligação fornecidas permitem determinar que a decomposição de 1,00 mol de H2O2, quando realizada à pressão constante de 1 bar e a 25 ºC, libera quantidade de calor superior a 100 kJ.
O O 2 (g) produzido na decomposição de 4,00 mol de H2O2 foi coletado a uma pressão de 1,00 atm e uma temperatura de 300 K. Posteriormente, o gás foi comprimido adiabaticamente pelo deslocamento de um pistão móvel até que a pressão interna atingisse 300 atm. Imediatamente após a compressão, a temperatura verificada foi T2.
A figura precedente mostra o gráfico do coeficiente de compressibilidade (Z) dos gases O
2 e CO2 em função da pressão para a temperatura T2. Considerando a situação hipotética apresentada e as informações fornecidas, que a constante universal dos gases seja igual a 0,082 atm × L × mol-1 × K-1, que a 300 K e 1,00 atm o O2 (g) e o CO2 (g) apresentem comportamento de gás ideal, e que a 300 atm e a uma temperatura T2 o O2 (g) e o CO2 (g) obedeçam a equação de estado de van der Waals expressa como: 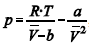
A partir do gráfico apresentado, conclui-se que o CO2 (g) apresenta a constante b na equação de van der Waals inferior à do O2 (g).
Considerando que a análise de uma amostra de minério de chumbo tenha apresentado os seguintes resultados percentuais (%): 8,10; 8,32; 8,12; 8,22; 7,99; 8,31, julgue o item a seguir, relativo a esses dados.
O desvio padrão da análise em apreço é dado pela raiz quadrada do valor médio dividido pelo número de amostras, no caso, 6.
Tendo em vista que, do ponto de vista prático, a quimiometria permite planejar ou selecionar condições ótimas de medidas e experimentos e, com isso, extrair o máximo de informação de dados químicos, julgue o item seguinte, relativo a esse assunto e a aspectos a ele correlacionados.
Para se fazer uma avaliação sistemática dos efeitos de duas temperaturas, duas pressões e duas concentrações de reagentes sobre o rendimento de uma reação química genérica devem ser realizados, pelo menos, oito experimentos.