Em uma pilha combustível ocorre as seguintes semi - reações representadas abaixo, responda à questão
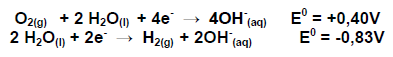
A ordem de grandeza da constante de equilíbrio K da pilha é
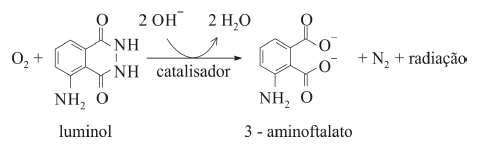
O composto conhecido como luminol é empregado para a detecção de sangue em perícias criminais. Em meio básico, em presença de peróxido de hidrogênio (H 2O2) e de um catalisador adequado, o luminol é oxidado ao ânion 3-aminoftalato, o qual é obtido inicialmente em um estado excitado, mas que rapidamente libera o excesso de energia emitindo radiação na faixa do azul.
A oxidação do luminol é realizada pelo O 2 (g) formado a partir da decomposição do peróxido de hidrogênio (H2O2), de acordo com a equação:
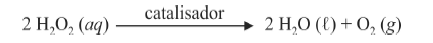
Sem a presença de um catalisador, a decomposição em questão é bastante lenta. Entretanto, o ferro presente na hemoglobina do sangue catalisa a decomposição e o O 2 (g) formado rapidamente oxida o luminol, ocasionando a característica luminescência azul.
Com relação à reação apresentada e às espécies nela envolvidas, e considerando a primeira constante de ionização ácida do H 2O2 igual a 2,4 × 10-12, julgue o item a seguir.
Em solução aquosa com pH igual a 10,0, o grau de ionização ácida do H2O2 é superior a 2,0%.
Um dispositivo analítico, conforme ilustrado na figura precedente, baseado em papel microfluídico (μPAD), foi desenvolvido para a determinação in loco da presença de chumbo, bário, antimônio, ferro, alumínio, zinco e magnésio, em resíduos de explosivos pirotécnicos. Cada canal contém um conjunto específico de reagentes que produz uma mudança de cor após a interação com um sal de metal específico, conforme esquematizado na tabela anterior. Esse novo dispositivo deve ser útil na detecção in loco de resíduos pós-explosão de pirotecnia no campo, devido à sua portabilidade e facilidade de uso.
Tendo como referência a figura e os dados da tabela precedentes, julgue o item a seguir
Considere que a reação entre antimônio e sulfeto produza o sal Sb
2S3, pouco solúvel e de cor ocre que, em meio aquoso, dissocia-se parcialmente, de acordo com o equilíbrio Sb2S3(s) X 2Sb3+(aq) + 3S2-(aq). Nesse caso, a concentração de sulfeto necessária para iniciar a formação do sólido Sb2S3 em uma solução aquosa de Sb3+ de concentração x mol/L deverá ser maior que 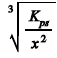
A precipitação de cátions metálicos pela adição de um ânion com o qual eles formem composto insolúvel é uma ferramenta bastante utilizada para a remoção, identificação e(ou) quantificação de um metal em solução. Por exemplo, a adição de uma solução de H 2S é empregada para promover a precipitação de sulfetos metálicos pouco solúveis.
Considerando que as constantes de ionização ácida do H
2S (Ka1 e Ka2) sejam iguais a 1,0 × 10-7 e 1,0 × 10-13, que o produto de solubilidade (Kps) do CdS seja igual a 1,0 × 10-27 e que todas as soluções envolvidas apresentem comportamento ideal, julgue o item a seguir.
Em uma solução aquosa de H 2S, a ordem decrescente de concentração das espécies presentes é [H2O] > [H3O+] > [H2S] > [S2-] > [HS-].
Em um recipiente fechado, mantido a uma temperatura de 40°C, são inseridos os gases monóxido de carbono e gás oxigênio, cujas pressões parciais foram determinadas respectivamente em 2,1 e 1,6 atm. Observando a reação química do processo e sabendo-se que no momento que o equilíbrio químico foi atingido a pressão parcial do gás oxigênio era de 0,6 atm, podemos informar que a constante de equilíbrio Kp vale, aproximadamente:
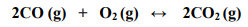
Para garantir a segurança do paciente que fizer uso do contraste, deve-se preparar essa suspensão em
Com relação à velocidade de reação química, a fatores que a influenciam e a assuntos correlatos, julgue o item a seguir.
As expressões da constante de equilíbrio são muito importantes porque permitem que os químicos possam prever a direção e a extensão de uma reação química. Contudo, uma expressão da constante de equilíbrio não fornece informações relacionadas à velocidade na qual o equilíbrio é alcançado.
Essa remediação promove no solo o(a)
A precipitação de cátions metálicos pela adição de um ânion com o qual eles formem composto insolúvel é uma ferramenta bastante utilizada para a remoção, identificação e(ou) quantificação de um metal em solução. Por exemplo, a adição de uma solução de H 2S é empregada para promover a precipitação de sulfetos metálicos pouco solúveis.
Considerando que as constantes de ionização ácida do H
2S (Ka1 e Ka2) sejam iguais a 1,0 × 10-7 e 1,0 × 10-13, que o produto de solubilidade (Kps) do CdS seja igual a 1,0 × 10-27 e que todas as soluções envolvidas apresentem comportamento ideal, julgue o item a seguir.
A concentração de íons S2- em uma solução aquosa de H2S 0,100 mol/L é inferior a 1,0 × 10-10.
A hidroxiapatita [Ca 5(PO4)3(OH)] é um mineral natural que correspondente a 96% da composição do esmalte dentário, e, na cavidade oral, está susceptível às seguintes reações:

ons fluoreto [F -] (assim como outros elementos) podem ser incorporados durante a formação do esmalte substituindo a hidroxila [OH-], conforme demonstrado a seguir:

Assim, a proteção contra a cárie foi atribuída à substituição da hidroxiapatita pela fluorapatita [Ca5(PO4)3(F)] durante a remineralização do esmalte, uma vez que o derivado com flúor apresenta menor solubilidade que hidroxiapatita. Diante do exposto, assinale a alternativa correta.
A seguir são apresentadas informações referentes à reação de decomposição do H 2O2.
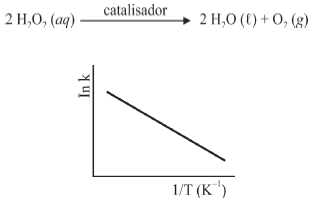
A figura precedente mostra o gráfico do logaritmo neperiano da constante de velocidade k da reação em função do recíproco da temperatura, sendo que a equação que descreve a reta obtida é y = 30 - 3,0 × 10 4 x.
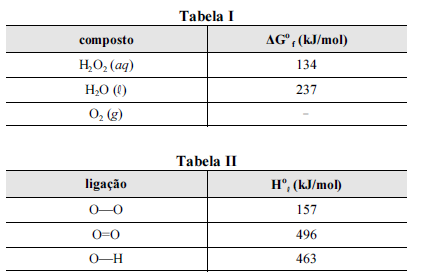
Nas tabelas I e II são apresentadas, para uma temperatura de 25 ºC, as energias livres de Gibbs padrão de formação (ΔGº f) para as espécies envolvidas na reação e algumas entalpias padrão de ligação (Hº l), respectivamente.
Considerando que a reação de decomposição do H 2O2 seja exotérmica e se processe de acordo com uma cinética de primeira ordem, e que a constante universal dos gases seja igual a 8,3 J × mol-1 × K-1, julgue os itens subsequentes, acerca da reação em questão.
Em temperaturas mais elevadas, o valor da constante de equilíbrio da reação de decomposição do H2O2 é superior ao verificado em temperaturas mais baixas.
Com relação à velocidade de reação química, a fatores que a influenciam e a assuntos correlatos, julgue o item a seguir.
Pelo princípio de Le Chatelier, quando se exerce uma ação sobre um sistema em equilíbrio dinâmico, ele se desloca no sentido que produz uma minimização da ação exercida. Em outras palavras, sempre que se aplicar um esforço sobre um sistema em equilíbrio, a posição de equilíbrio será alterada na direção que tende a minimizar ou anular o efeito do esforço aplicado.
Atenção: Para responder à questão, considere a curva de titulação abaixo.
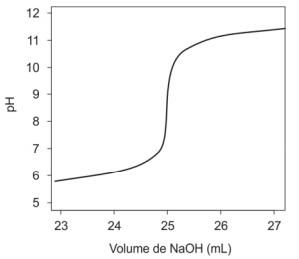
O valor de pH obtido no ponto estequiométrico deve-se a
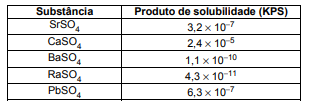
Considere uma solução aquosa 0,1 mol L−1 contendo os cátions Sr2+, Ca2+, Ba2+, Ra2+ e Pb2+.
Dadas as constantes do produto de solubilidade (KPS):
Se íons sulfato 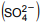 forem gradualmente adicionados à solução acima,
forem gradualmente adicionados à solução acima,
De acordo com a equação a seguir e as informações hipotéticas da tabela apresentada, a respeito da produção de gás metano (CH4) partindo de CS2 (g) e 4H2(g) à 500ºC, assinale a alternativa que apresenta o correto comportamento das mudanças qualitativas nas concentrações dos reagentes e produtos à medida que o sistema se aproxima do equilíbrio, se a temperatura foi mantida a 500ºC.
Considere Kc a constante de equilíbrio de concentração.