A qualidade de um corpo d'água foi monitorada, durante
quatro meses, pelo parâmetro concentração de fosfato.
As concentrações deste ânion, em mg.L–1, foram determinadas
utilizando a mesma metodologia e os valores obtidos estão
apresentados no gráfico a seguir:
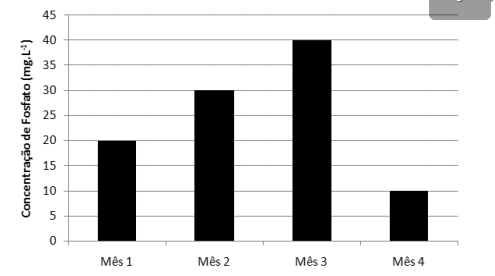
De acordo com o gráfico, a concentração média de fosfato em quantidade de matéria (mol.L–1) no corpo d'água, durante os meses avaliados, é aproximadamente de
Dados: Massas Molares (g.mol–1) O = 16 e P =31
O modelo de repulsão dos pares de elétrons da camada de
valência (modelo VSEPR) baseia–se na ideia de que as regiões
de altas concentrações de elétrons (ligações e pares isolados do
átomo central) se repelem e, para reduzir essa repulsão, elas
tendem a se afastar o máximo possível, mantendo a mesma
distância do átomo central. Aplicando essa teoria, a geometria
prevista para a molécula de pentacloreto de fósforo é
Dados: P (Z=15) e Cl (Z=17)
A vitamina B5, encontrada em diversos alimentos, é importante para a saúde humana, pois ajuda a controlar a capacidade de resposta do corpo ao stress, além de aturar na produção dos hormônios nas glândulas suprarrenais, na formação de anticorpos e no metabolismo das proteínas, gorduras e açucares.
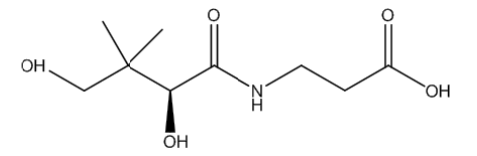
A estrutura química da vitamina B5, representada na figura, apresenta grupos funcionais que identificam as funções.
A ureia, utilizada como fertilizante, pode ser produzida através da reação de amônia líquida com o CO2 gasoso, em um reator de síntese, ocorrendo inicialmente a formação do carbamato de amônio que posteriormente se decompõe parcialmente em ureia e água. O carbamato de amônio não reagido é decomposto em amônia e CO2 num processo endotérmico segundo a equação:
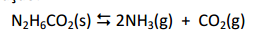
Em relação ao equilíbrio apresentado, a reação de decomposição do carbamato é favorecida pela
A produção de eteno a partir da desidratação de etanol oriundo
de cana de açúcar permitiu a entrada no mercado de um
polietileno com menor impacto ambiental, logo apelidado de
“Polietileno Verde”.
Analise as afirmativas a seguir sobre o Polietileno Verde:
I. Apesar das origens diferentes do eteno, a reação de
polimerização do etileno verde é idêntica à reação de
polimerização do etileno convencional, obtido pelas rotas
petroquímicas conhecidas.
II. Por ser originário do etanol ele possui alguns átomos de
oxigênio na sua estrutura, o que facilita sua degradação no
ambiente
III. O descarte do polietileno verde apresenta o mesmo
impacto ambiental do polietileno convencional
Assinale:
Reações de condensação aldólicas são importantes na síntese
de diversos compostos naturais e biológicos, inclusive na
gliconeogênese. Estas reações acoplam dois compostos
orgânicos formando uma nova ligação química. No século XIX, o
químico russo Borodin realizou a condensação do etanal em
presença de hidróxido de sódio diluído, produzindo em
condições adequadas, um aldeído α, β−insaturado.
Considerando apenas etanal e o aldeído α, β−insaturado.
produto final da reação, foram quebradas e formadas ligações
químicas do tipo:
Uma parte relevante do estudo das ligações químicas é a
relação entre o tipo de ligação interatômica e as propriedades
das substâncias. Isso porque as propriedades químicas e físicas
das substâncias estão diretamente associadas ao tipo de ligação
química existente entre os átomos.
A tabela a seguir apresenta algumas observações experimentais
para uma substância hipotética.

A substância que possui propriedades químicas e físicas semelhantes às da tabela pode ser representado pela seguinte fórmula:
O α−pineno tem sido utilizado, na indústria química, para
sintetizar compostos que são matérias primas para a fabricação
de perfumes e polímeros.
Um desses compostos pode ser obtido com cerca de
90% por meio da reação representada a seguir.
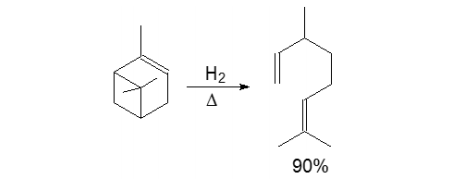
O hidrocarboneto produzido na reação é denominado
A vida das diferentes espécies de peixes é diretamente
influenciada pela acidez do corpo d’água, mas sabe–se que em
concentrações de íons H+ superiores a 10–5 mol.L–1 a maioria
dos peixes não sobrevive. Em um aquário, a 25qC, foram
determinadas as concentrações de alguns íons, entre eles o íon
OH– que apresentou concentração 10–11mol.L–1.
Para essas condições, assinale a alternativa que indica a acidez da
água e a previsão sobre a sobrevivência dos peixes nesse aquário.
O ácido tereftálico é um monômero muito utilizado para a produção de diversos poliésteres importantes. Este ácido é obtido pela oxidação catalítica do p–xileno, utilizando ar como oxidante, de acordo com a reação a seguir.
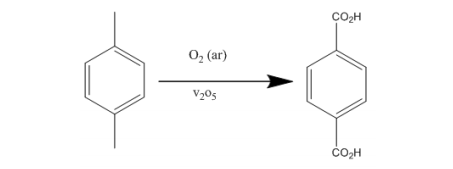
Esta reação deve ser conduzida com um rigoroso controle de temperatura, pois há o risco de ocorrer a combustão de parte do reagente.
Numa fábrica de ácido tereftálico houve falha no sistema de refrigeração do reator principal, levando ao descontrole da reação e causando uma queda de 50 % no rendimento teórico da reação em relação ao ácido tereftálico. Uma análise dos produtos revelou que foram formados apenas ácido tereftálico, água e CO2.
Nessas condições, para uma carga inicial de 530 quilos de p–xileno no reator, e considerando que este foi totalmente consumido, é correto calcular que, nestas condições, foram produzidos
Dados: massa molar p–xileno= 106 g.mol–1; ácido tereftálico = 166 g.mol–1; CO2= 44 g.mol–1
Organismos vivos devem ser capazes de regular a atividade de
suas enzimas de modo a coordenar os seus inúmeros processos
metabólicos.
Entre os componentes fundamentais dos ácidos nucleicos estão
moléculas denominadas pirimidinas. Na síntese dessas
moléculas, a primeira etapa do processo consiste na reação
entre aspartato e carbamoil–fosfato, catalisada pela enzima
aspartato transcarbamoilase (ATCase).
A figura a seguir retrata o comportamento da ATCase de E.Coli,
na ausência e na presença das substâncias trifosfato de citidina
(CTP) e trifosfato de adenosina (ATP), em diferentes
concentrações do substrato aspartato.
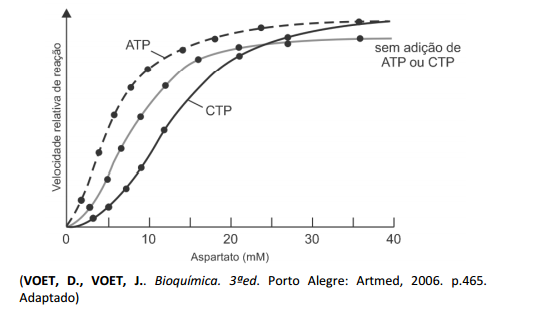
Sobre a atividade da enzima ATCase, é correto concluir que
O crômio é um metal lustroso, brilhante e resistente à corrosão. O nome, que vem da palavra grega para “cor”, lhe foi atribuído pelo colorido de seus compostos. O metal é obtido a partir do mineral cromita (FeCr20d), por redução com carbono em um formo de arco elétrico:
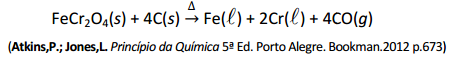
Assinale a alternativa que indica a massa máxima de crômio (em quilograma) que pode ser produzida pelo processo descrito a partir de 100 mol de cromita.
Dados> Massas molares O=16g.mol−1 Cr=52g.mol−1 Fe=56 g.mol−1
Alguns organismos são bioluminescentes e a luz emitida desempenha a função de comunicação e até mesmo de defesa. Nos vagalumes a emissão de luz é consequência da ação de enzimas que promovem a reação de descarboxilação que pode ser representada como:

A tabela a seguir apresenta valores das energias das ligações (em kJ.mol–1).

A variação da entalpia envolvida na reação, calculada a partir dos valores das energias das ligações, é de
A figura a seguir representa o diagrama de energia de uma reação, realizada em diferentes condições.
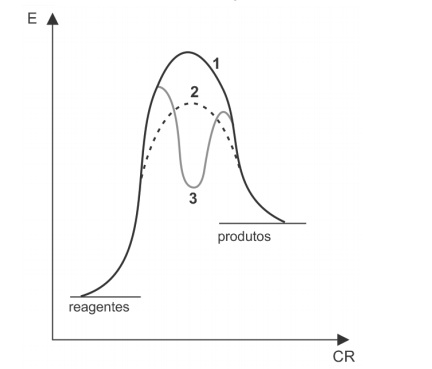
A partir do diagrama, assinale a afirmativa correta.
O carbonato de sódio é largamente utilizado na confecção de vidros, sabões, papel e outros produtos. O processo Solvay, atualmente, é o responsável por 3/4 da produção mundial de carbonato de sódio e se baseia em uma série de reações que envolvem, como insumos principais, o carbonato de cálcio e o cloreto de sódio em solução aquosa (salmoura). O diagrama geral do processo pode ser visto a seguir.
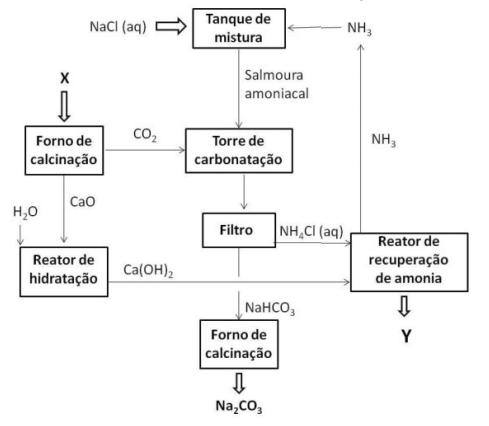
Para que o processo industrial seja conduzido de forma econômica, entretanto, são necessários outros processos complementares para a geração ou para a reciclagem de insumos. Com base nas informações disponíveis, é correto afirmar que a matéria–prima X e o co–produto Y são, respectivamente:

