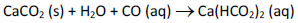O nitrogênio (Z = 7) tem a configuração [He]2s22p1 x2p1 y2p1 z e o oxigênio (Z = 8), que aparece um orbital 2p duplamente ocupado, resulta [He]2s22p2 x2p1 y2p1 z. O conceito que explica quando os elétrons ocupam isoladamente um orbital é chamado de
Sobre a classificação periódica dos elementos é correto afirmar que
A tabela periódica organiza metodicamente os elementos químicos em ordem
O elemento com número atômico 53 está classificado na tabela periódica como
O alumínio e o índio estão ambos no grupo 13 da tabela periódica. O alumínio forma cátions com três cargas positivas enquanto o índio forma cátions com três cargas positivas e cátions com apenas uma carga positiva. A tendência manifestada pelo índio para formar cátions com duas unidades mais baixas se deve ao efeito
A tabela periódica e o modelo atômico evoluíram gradualmente ao longo do tempo, até as versões atuais. A figura precedente mostra uma ilustração bastante utilizada na representação de um átomo e que se baseia no modelo atômico de Bohr. Com relação à tabela periódica, aos modelos atômicos e aspectos a eles relacionados, julgue o próximo item.
Os elementos metálicos caracterizam-se por apresentarem elevadas afinidade eletrônica e energia de ionização.
A tabela periódica é uma das realizações mais notáveis da Química porque ajuda a organizar a extensa quantidade de propriedades dos elementos, que, de outra forma, seria um arranjo confuso. A tabela periódica pode ser usada na previsão de um grande número de propriedades, muitas das quais são cruciais para a compreensão das características químicas e físicas dos compostos.
Sobre as propriedades periódicas dos átomos, pode-se afirmar que
Sobre as ligações iônicas, assinale a alternativa que completa correta e respectivamente as lacunas do texto.
Os compostos iônicos são resultados da reação entre um metal e um ametal. Os elétrons são transferidos do ______________ para o _______________ formando os______________e os________________ respectivamente. Um exemplo de reação desse tipo ocorre quando colocamos gás cloro em contato com sódio metálico, formando assim o cloreto de sódio.
Considere as afirmativas dadas abaixo.
I. A primeira energia de ionização, I1, é a quantidade de energia necessária para remover o elétron mais fracamente ligado de um átomo gasoso.
II. A afinidade eletrônica é a alteração de energia quando um átomo gasoso ganha um elétron para formar um íon gasoso.
III. É modo geral, ao longo de um período, a carga nuclear efetiva Zef aumenta e, consequentemente, fica mais difícil remover um elétron.
Está(Estão) correta(s) a(s) afirmativa(s)
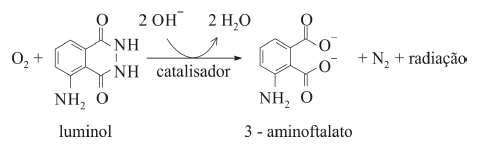
O composto conhecido como luminol é empregado para a detecção de sangue em perícias criminais. Em meio básico, em presença de peróxido de hidrogênio (H 2O2) e de um catalisador adequado, o luminol é oxidado ao ânion 3-aminoftalato, o qual é obtido inicialmente em um estado excitado, mas que rapidamente libera o excesso de energia emitindo radiação na faixa do azul.
A oxidação do luminol é realizada pelo O 2 (g) formado a partir da decomposição do peróxido de hidrogênio (H2O2), de acordo com a equação:
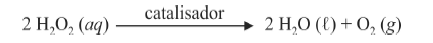
Sem a presença de um catalisador, a decomposição em questão é bastante lenta. Entretanto, o ferro presente na hemoglobina do sangue catalisa a decomposição e o O 2 (g) formado rapidamente oxida o luminol, ocasionando a característica luminescência azul.
Com relação à reação apresentada e às espécies nela envolvidas, e considerando a primeira constante de ionização ácida do H 2O2 igual a 2,4 × 10-12, julgue o item a seguir.
A partir das posições relativas dos elementos na tabela periódica, é possível inferir que um átomo neutro de ferro apresenta maior raio atômico do que um átomo neutro de manganês.
Os elementos que possuem propriedades semelhantes são:
Julgue o item a seguir quanto às reações e aos usos que envolvem o carbonato de cálcio e seus derivados.
Cavernas de calcário são formadas pela ação de dissolução das rochas calcárias pela água subterrânea, que contém dióxido de carbono, conforme a equação química a seguir.

Considere as reações I, II e III a seguir.
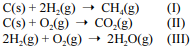
Com relação a essas informações, julgue o item que se segue.
A substituição de 1, 2 ou 3 átomos de hidrogênio por átomos de cloro na molécula de metano tornaria polares todos os compostos formados, contudo, caso os 4 átomos de hidrogênio na molécula de metano fossem substituídos por átomos de cloro, a molécula formada seria mantida apolar, como o próprio metano.
Todas as propriedades macroscópicas das substâncias, ou seja, que a gente pode observar a olho nu, são definidas pelo tipo de ligação que ocorre microscopicamente entre os átomos. A natureza destas ligações depende da estrutura eletrônica dos átomos. Mas você deve estar se perguntando, por que os átomos se ligam?
Assim como os seres humanos, os átomos também procuram estabelecer ligações com outros átomos para adquirir mais segurança ou estabilidade, formando por meio dessas ligações as moléculas ou os cristais.
A molécula nada mais é do que um grupo de átomos unidos por ligações químicas. Sabemos, por exemplo, que o gás hidrogênio é formado por dois átomos do elemento hidrogênio (H2) e que a água é formada por dois átomos de hidrogênio mais um átomo de oxigênio (H2O).Com base neste contexto considere o elemento X do terceiro período da tabela periódica forma com o magnésio o composto MgX e, com o hidrogênio, H2X. O número de elétrons da última camada de X é:
Identifique a família e o período da Tabela Periódica nos quais está localizado um elemento cujos números quânticos para o elétron mais energético do cátion bivalente são: n = 5, l = 2, m = +2, s = + ½. Considere s = s = - ½ para o primeiro elétron no orbital.