Até quando essa juventude será alvo de preconceito, criminalização e repressão
- por parte de agentes do Estado? (linhas 9 e 10)
O trecho acima sugere que:
Considere as afirmativas a respeito dos trechos a seguir e marque (V ) caso sejam
verdadeiras e (F ) caso sejam falsas.
( ) “Toda geração tem marcas próprias na juventude. " (linha 1). Constitui-se como uma
declaração inicial com vistas a assinalar as mudanças a serem efetivadas ao longo
do tempo.
( ) O questionamento feito ao final do 3º parágrafo reforça a posição defendida pelo
autor, motivando o envolvimento do leitor.
( ) “Uma marca negativa do mundo atual está diretamente relacionada com os valores
da ideologia neoliberal impregnada na juventude, como demonstra uma pesquisa
em que 40,3% dos jovens entrevistados [...]." (linhas 15-17). Exemplifica argumento
de autoridade.
( ) “É preciso conhecê-los ? se quisermos construir um futuro melhor." (linha 27).
Sintetiza o problema, por meio de uma prescrição.
Assinale a alternativa que apresenta a sequência correta.
Sobre o Internet Explorer, Mozilla Firefox, Google Chrome e conceitos relacionados tais como URL, apontadores, “sites” Web e de Pesquisa é INCORRETO afirmar que:
Pode-se afirmar que os laboratórios são as partes mais importantes dos estabelecimentos de ensino, institutos de pesquisa e indústrias. Pelos tipos de trabalho que neles são desenvolvidos são incontáveis os riscos de acidentes causados por exposição a agentes tóxicos e/ou corrosivos, queimaduras, lesões, incêndios e explosões, radiações ionizantes e agentes biológicos patogênicos. Manual de segurança para proteção Química, Microbiológica e Radiológica. Disponível em http://www2.iq.usp.br/cipa/manual/manualinteiro.pdf>. Acesso em: 1º out. 2016. Para minimizar riscos e acidentes em laboratórios de ensino, os técnicos devem considerar que
Os incêndios em laboratórios químicos são muito comuns e devem ser combatidos com o uso de extintores adequados. Desse modo, considera-se que os extintores de
O ácido acético é muito utilizado nas aulas experimentais de química e pode ser encontrado no vinagre. Ao estudante de química de uma universidade, foi solicitado preparar uma solução contendo 0,760 mmol de ácido acético a partir de uma solução estoque 0,0380 mol.L-1 do mesmo ácido. Para tanto, é necessário ao estudante
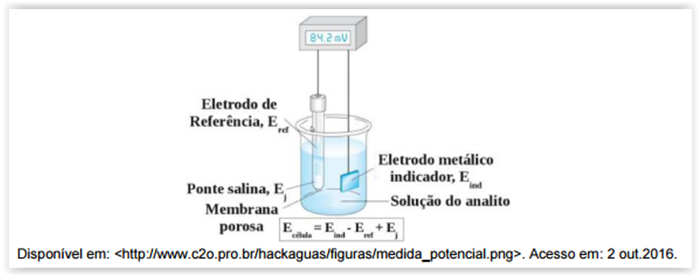
Considere a figura a seguir.
Dos componentes potenciométricos do sistema representado pela figura, o potencial
Sólidos iônicos são muito manipulados em laboratórios químicos e possuem como modelo explicativo a regularidade das estruturas cristalinas. São exemplos desses sólidos:
A determinação de ânions cloreto na urina de um paciente do Hospital de Clínicas da UFU ocorreu por análise química de precipitação desse cloreto com solução aquosa de nitrato de prata. Para tanto, após coleta adequada, evaporou-se a urina e, no resíduo, adicionou-se água até o volume final de 1L. Uma alíquota de 25 mL foi transferida para um erlenmeyer, em que foram adicionados 50,0 mL de solução aquosa de nitrato de prata 0,120 mol/L. A partir dos procedimentos descritos, e com a finalidade de determinar a quantidade de cloreto na urina, o analista químico recomendou
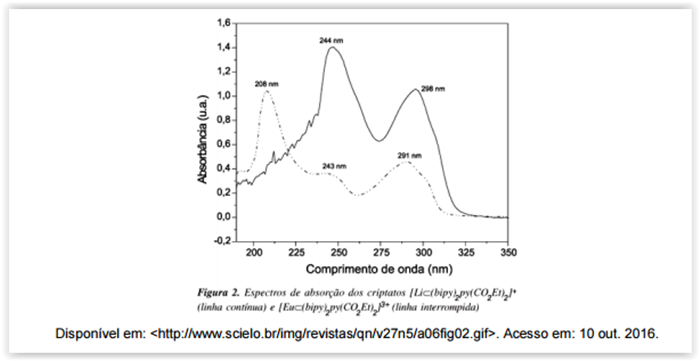
Considere o espectro a seguir.
Os máximos de absorção, representados no espectro, estão relacionados
A segurança nos laboratórios químicos é de fundamental importância e deve ser conhecida por todos os seus usuários. A alternativa que melhor expressa cinco recomendações de segurança em laboratórios químicos é:
Embora o conceito de juventude seja bem recente, inclusive com definição de faixa etária pela ONU, de 15 a 24 anos de idade, todos convivem e enfrentam dilemas nessa fase de transição para a vida adulta. (linhas 1-3)
No excerto, o termo em negrito expressa
O Decreto nº. 1.171, de 22 de junho de 1994, aprova o Código de Ética Profissional do Servidor Público Civil do Poder Executivo Federal. Sobre as vedações, assinale a alternativa que NÃO caracteriza uma vedação ao servidor público.
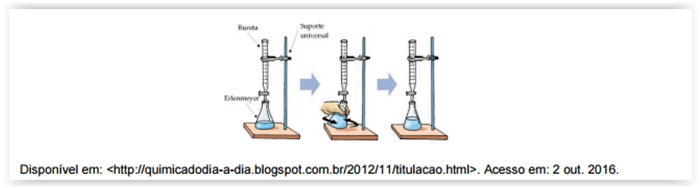
A figura ilustra o processo de análise volumétrica que consiste na determinação da
concentração ou da quantidade de substância pela medida de volume, podendo ser
interpretada como uma
Um técnico em análises químicas recebeu uma amostra de 0,101g de minério de
ferro e supôs que a porcentagem de massa de ferro na amostra era superior a 20%. Para
comprovar sua suposição, ele optou por dissolver a amostra em meio ácido e realizar uma
titulação com solução aquosa 0,005 mol/L de permanganato de potássio. Foram consumidos
10,5 mL do titulante. A equação não balanceada que representa a reação é dada abaixo.
O ponto estequiométrico pôde ser percebido pela cor persistente do íon permanganato,
indicando a transformação total do Fe (II) em Fe (III). A partir desses dados, é possível
concluir que o técnico em química estava