Considere que um químico encontrou no almoxarifado algumas garrafas antigas de
reagentes. Um dos reagentes estava rotulado como óxido cobáltico mono–hidratado.
Assinale a alternativa que apresenta respectivamente a nomenclatura atual e a fórmula
química CORRETA.
Ao longo da história da ciência, as pessoas que fazem descobertas importantes são
frequentemente homenageadas, tendo os seus nomes ligados às descobertas. Embora
essa prática não seja muito comum atualmente, os métodos mais antigos tais como os
métodos argentimétricos, recebem o nome dos químicos responsáveis pelo seu
desenvolvimento.
Numere a COLUNA II de acordo com a COLUNA I, fazendo a relação entre o método
argentimétrico e o químico relacionado ao método.

Assinale a alternativa que apresenta a sequência CORRETA.
Considere que uma solução de um ácido fraco (Ka=10–10) com pH igual a 5 foi diluído 10
vezes.
Nessas condições, é CORRETO afirmar que a concentração da solução do ácido fraco
após sua diluição será igual a
Considere que num experimento de difração foram utilizados raios X de comprimento de
onda de 0,154 nm sobre um cristal de NaCl. Uma difração de primeira ordem teve lugar
no ângulo θ de 22,77º.
Nessas condições experimentais, é CORRETO afirmar que a distância entre as camadas
de átomos responsáveis por esse raio é
Considere sen θ=0,4
A teoria do orbital molecular descreve os elétrons na molécula, usando funções de onda
específicas, chamadas orbitais moleculares.
São regras que descrevem a formação dos Orbitais Moleculares (OM) e como eles são
ocupados pelos elétrons, EXCETO:
Uma solução contendo KMnO4 e H2SO4 é despejada em uma proveta; e uma solução de
FeSO4 é despejada em outra. Uma ponte salina é usada para unir as provetas. Uma
lâmina de platina é colocada em cada solução e as duas soluções são conectadas por um
fio que passa por um voltímetro.
Analise as afirmações que foram feitas a partir da pilha obtida.
I. A soma dos menores números inteiros dos coeficientes estequiométricos da equação
balanceada da reação global é 24.
II. A semireação do anodo ocorre no ferro e do catodo no manganês.
III. A representação da célula voltaica da reação de oxirredução é
Fe2+(aq)/Fe3+(aq) ?? Mn7+(aq) / Mn2+(aq).
A partir dessa análise, conclui–se que estão CORRETAS as afirmativas
O cloreto de alumínio anidro é obtido a partir da seguinte reação:
2Al(s) + 3Cl2(g) → 2AlCl3M(s)
Observe as seguintes equações.
2Al(s) + 6HCl(aq) → 2AlCl3(aq) + 3H2(g) ΔH0= –1.049 kJ
HCl(g) → HCl(aq) ΔH0= –74,8 kJ
H2(g) + Cl2(g) → 2HCl(g) ΔH0= –185 kJ
AlCl3(s) → AlCl3(aq) ΔH0= –323 kJ
Considerando–se as equações acima, é CORRETO afirmar que a entalpia de reação da
formação do cloreto de alumínio anidro é igual a
A síntese do amoníaco, também designada por síntese de Haber, refere–se a um
processo hoje largamente empregado em escala industrial em que os parâmetros que
interferem na reação química entre nitrogênio e hidrogênio são idealmente ajustados, a
fim de maximizar a síntese do amoníaco.
Sobre a produção de amônia pelo processo Haber, assinale com V as afirmativas
verdadeiras e com F as falsas.
( ) A velocidade de desaparecimento do gás nitrogênio é um terço vezes a velocidade
de desaparecimento do gás hidrogênio.
( ) A velocidade de formação da amônia é duas vezes a velocidade de
desaparecimento de gás hidrogênio.
( ) A velocidade de formação da amônia é dois terços vezes a velocidade de
decomposição do gás nitrogênio.
( ) O processo de formação da amônia a partir de gás nitrogênio e gás hidrogênio é
exotérmico.
Assinale a alternativa que apresenta a sequência CORRETA.
Um dos princípios ativos dos medicamentos indicados para o tratamento da dor, da tosse
e no combate à diarreia é a codeína, um derivado da morfina, princípio ativo extraído da
papoula, sendo o ópio conhecido desde a época dos sumérios há 4.000 anos a.C.
A figura abaixo mostra a estrutura da codeína.
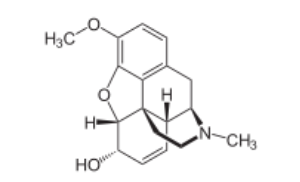
Sobre a estrutura da codeína, assinale a alternativa INCORRETA.
Um químico precisou preparar uma solução de HCl em um balão volumétrico de 100 mL.
Ele utilizou uma solução estoque com as seguintes especificações no rótulo:
Porcentagem em massa por volume do HCl = 38% m/v
Densidade da solução = 1,2 g/mL
Massa molar do HCl = 36,5 g/mol
Considerando–se as informações citadas, é CORRETO afirmar que o volume aproximado
extraído da solução estoque utilizado para preparar a solução de 0,5 mol/L de HCl é
Para remover as impurezas grossas na produção do álcool, o caldo é inicialmente
peneirado e, em seguida, tratado com agentes químicos, para coagular parte da matéria
coloidal, precipitar certas impurezas e modificar o pH.
Com relação aos métodos utilizados no processo de clarificação do caldo da cana–deaçúcar
é INCORRETO afirmar que
Um modo de aumentar a velocidade de uma reação é usar um catalisador, uma
substância que aumenta a velocidade da reação química.
Sobre os catalisadores, é INCORRETO afirmar que
Durante os processos de produção do álcool, são gerados resíduos que, quando não
reutilizados, podem causar impactos ambientais. Entre esses resíduos, estão: bagaço,
torta de filtro, vinhaça, levedura seca e óleo fusel.
Sobre os resíduos resultantes dos sistemas de produção do álcool, avalie as afirmações
que se seguem.
I. O bagaço é um resíduo fibroso que pode ser utilizado como combustível nas caldeiras
para geração de energia elétrica e calor, mas também pode ser utilizado na
fabricação de papeis e como ração animal, se for hidrolisado.
II. A vinhaça é um resíduo resultante de destilação do álcool que é utilizado,
principalmente, na lavoura para irrigação da cana, na chamada fertirrigação.
III. O óleo fusel é resultante da destilação do álcool que é utilizado nas indústrias
químicas e indústrias de cosméticos.
Assinale a alternativa que apresenta a sequência CORRETA.
Considere uma titulação de 25,0 mL de uma solução 0,100 mol/L de FeSO4 com uma
solução de 0,100 mol/L de Ce4+ em meio ácido, feita na temperatura de 25 ºC. As semireações
abaixo mostram os potenciais padrões de redução do cério e ferro,
respectivamente.
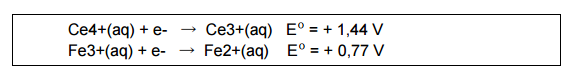
Nessas condições, é CORRETO afirmar que o potencial da reação global, quando se
atinge o ponto de equivalência, é
A reatividade química dos metais está relacionada às propriedades periódicas e à configuração eletrônica dos elementos. Com relação à reatividade dos metais, é INCORRETO afirmar que

