O número de Nusselt representa, para a camada limite térmica, o que o coeficiente de atrito representa para a camada limite fluidodinâmica. Esse parâmetro de similaridade sugere:
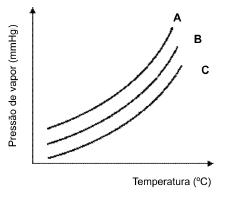
A variação da pressão de vapor, em mmHg, de três
amostras líquidas A, B e C com a temperatura, em ºC,
é mostrada no gráfico que segue.
Analise as afirmativas feitas sobre as amostras.
I. Colocando−se uma gota de cada amostra em
diferentes pontos de um tecido, a amostra A
vaporizará mais rápido.
II. A temperatura de ebulição da amostra B é maior
que da amostra C.
III. As forças intermoleculares na amostra C são,
provavelmente, mais intensas que na amostra A.
IV. Se as amostras forem de água, acetona e álcool,
então pode−se fazer a seguinte associação:
A= água, B= álcool eC= acetona.
V. Se as interações intermoleculares nas amostras
são do mesmo tipo, a molécula da substância da
amostra A é, provavelmente, mais pesada que a
de C.
A alternativa que só contém afirmações verdadeiras
é:
Considerando a lei dos gases ideais, a temperatura máxima que a massa de 19,9 kg de argônio (massa molar = 39,8 kg / kmol) contida em um recipiente de 1 m pode ser aquecida sem que a pressão manométrica exceda 15 kgf/cm2 será: Dado: Cons tante uni ver sal dos gases , R= 8,3 kJ/(kmol*K)
Sobre o segundo princípio da termodinâmica é correto afirmar que:
Considerando um corpo maciço de 1 kg abandonado em queda de uma altura de 100 metros. Admitindo que não há troca de energia entre este corpo e as suas vizinhanças e considerando a gravidade como 9,81 m/s2 , a energia potencial deste corpo, no exato momento do abandono em relação à base da queda, será:
Areação de reforma a vapor do metano é utilizada em diversos processos químicos na indústria e consiste na reação de vapor d'água com metano em fase gasosa produzindo os gases monóxido de carbono e hidrogênio. Considerando que esta reação encontrase em equilíbrio, para 5 mols de vapor d'água consumidos durante a reunião será(ão) produzido(s):
Água (1000 kg/m3) é bombeada de um tanque para outro a uma distância de 300 metros. O nível de água no segundo tanque está a 40 metros acima do nível do primeiro. Considerando a força gravitacional local de 9,8 m/s2, o aumento da energia potencial específica da água, expresso em J/kg, será:
Uma mistura ideal de hidrocarbonetos na temperatura de 20 ºC apresenta composição volumétrica de 40% em n–octano e 60% em i–octano. As massas específicas dos hidrocarbonetos são 703 e 692 kg/m , respectivamente. A densidade da mistura nesta temperatura, considerando a massa específica da água a 4 C igual a 1000 kg/m , será:
Da análise dos gases de combustão de um forno, verificou–se que sua composição apresentava 8,4% de gás oxigênio (O2 ), 83,7% de gás nitrogênio (N2 ) e 7,9% de gás carbônico (CO2 ). Considerando que na corrente de ar antes de ser misturada com a corrente de combustível apresentava 20% de O e 80% deN , o percentual de excesso de ar será:
Para uma transformação ideal de um sistema isolado, a equação da variação infinitesimal da entropia pode ser escrita como:
As equações da primeira lei da termodinâmica podem ser escritas para sistemas de quaisquer tamanhos e complexidades. Neste contexto é relevante citar o conceito de propriedades intensivas e extensivas. Assinale a opção que indica uma grandeza extensiva.
O desempenho de uma máquina de refrigeração é usualmente caracterizado pelo coeficiente de eficiência (COE). Considerando o refrigerador, inicialmente a 480 R, com uma máquina a ciclo de ar, e com sua temperatura final de 600 R, oCOEserá:
A efetividade de uma aleta pode ser definida como:
O poder emissivo total de um corpo negro está
relacionado diretamente com a temperatura e a
constante de Stefan−Boltzmann. Esta relação
conhecida como lei de Stefan−Boltzmann permite
calcular a quantidade de radiação emitida em todas
as direções e ao longo de todos os comprimentos de
onda. Considerando um grande recipiente isotérmico
como um corpo negro mantido a uma temperatura
uniforme de 2000 K, a intensidade total associada à
emissão de um corpo negro, expressa em W/m2,
será:
Dados: constante de Stefan−Boltzmann igual
5,67 x 10 W/(m2 .K4 )
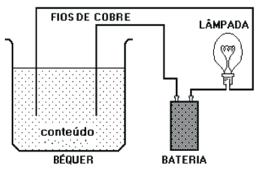
O desenho que segue representa um circuito elétrico
que pode servir de teste para verificar se um meio é
ou não um bom condutor de corrente elétrica,
observando o efeito sobre a lâmpada.
Considere os seguintes conteúdos no béquer
testados isoladamente: Hg(l), KOH(s), NaCl(aq),
HCl(l) e CH3COOH(aq). O número de testes em que
a lâmpada acendeu é: