Os exemplos de substâncias incompatíveis com a água são:
Analise as seguintes reações orgânicas e indique a alternativa que apresenta uma reação cujo produto apresentado é o esperado para a reação.
Considerando os conceitos de átomo, estados da matéria e reações químicas, julgue os itens seguintes.
As reações químicas podem ser reversíveis ou irreversíveis; como exemplo de uma transformação reversível, tem-se a solubilização de comprimidos efervescentes em água com formação de bolhas.
Existem vários tipos de extintores para uso em diferentes classes de incêndio. Os principais deles são: o extintor de pó químico (NaHCO3), que age por abafamento, interrompendo a combustão; o extintor de gás carbônico (CO2), que age por abafamento e resfriamento; o extintor de água (H2O), que age por resfriamento e, em parte, por abafamento; e o extintor de espuma mecânica, que age por abafamento e por resfriamento.
Com relação ao funcionamento desses tipos de extintores e aos seus componentes químicos, julgue os itens a seguir.
Quando em funcionamento, o extintor de espuma facilita o contato do comburente com o combustível.
Considerando os conceitos de átomo, estados da matéria e reações químicas, julgue os itens seguintes.
Uma reação química é o processo de mudança química da matéria, isto é, a conversão de uma ou mais substâncias em outras substâncias.
Assinale a alternativa que contenha somente a reação química correta para a afirmação I:
Existem vários tipos de extintores para uso em diferentes classes de incêndio. Os principais deles são: o extintor de pó químico (NaHCO 3), que age por abafamento, interrompendo a combustão; o extintor de gás carbônico (CO2), que age por abafamento e resfriamento; o extintor de água (H2O), que age por resfriamento e, em parte, por abafamento; e o extintor de espuma mecânica, que age por abafamento e por resfriamento.
Com relação ao funcionamento desses tipos de extintores e aos seus componentes químicos, julgue os itens a seguir.
A primeira substância citada no texto — NaHCO3 — pode ser formada pela adição de CO2 a uma solução de hidróxido de sódio.
A química ambiental trata das reações, dos destinos,
dos movimentos e das fontes das substâncias no ar, na água
e no solo. Na ausência do ser humano, a discussão seria
limitada às substâncias de ocorrência natural. Hoje, com o
borbulhar da população na Terra, junto com o contínuo
avanço da tecnologia, as atividades humanas têm uma
influência sempre crescente na química do meio ambiente.
C. Baird e M. Cann. Química ambiental.
4ª ed. Porto Alegre: Bookman, 2011
Julgue os itens subsecutivos com relação à química e ao meio
ambiente.
A camada de ozônio é a região da atmosfera que filtra os raios infravermelhos (IV) nocivos provenientes da luz solar. Assim, esses raios, que poderiam causar danos aos seres humanos e a outras formas de vida, são eliminados antes de atingir a superfície do planeta.
Uma reação de simples troca é apresentada na alternativa:
Reações químicas são processos importantes que podem acontecer no dia a dia, na indústria, nos organismos dos seres vivos etc., havendo vários indícios de sua ocorrência. Sobre essa temática, considere as situações apresentadas a seguir:

São exemplos de reações químicas as que estão presentes nos itens
Os clorofluorcarbonos são um conjunto de moléculas orgânicas muito estáveis na atmosfera, compostas por 1 ou 2 carbonos e átomos de flúor e cloro ligados a essa cadeia carbônica. Foram muito utilizados nas indústrias de refrigeração e ar condicionado, espumas, aerossóis e extintores de incêndio. Foi banido em Protocolo de Montreal, que entrou em vigor dia 01 de janeiro de 1989.
Sobre os problemas ambientais relacionados aos CFCs, analise as afirmações abaixo.
I. Por serem moléculas estáveis na atmosfera, possuem tempos de meia vida longos.
II. A radiação solar retira um átomo (radicalar) de flúor da molécula de CFC, este ao entrar em contato com o ozônio (O3), promove a quebra deste e forma o buraco na camada de ozônio.
III. Os maiores buracos na camada de ozônio estão sobre o Ártico, que está derretendo em uma taxa maior do que a esperada pelos climatologistas.
IV. O buraco na camada de O3 atinge seu maior tamanho em outubro, por uma combinação de fatores climáticos e insolação solar.
V. Os CFCs são um dos gases mais eficientes no processo de aquecimento da atmosfera e consequentemente, nas mudanças climáticas globais.
Assinale a alternativa que contém somente as afirmações verdadeiras:
Leia o fragmento a seguir.
“O objetivo da atividade é evidenciar que esse tipo de
transformação envolve a formação de novas substâncias e que
podem ser acompanhadas de aspectos facilmente perceptíveis ou
evidências.”
(MACHADO, A.H. Aula de Química: discurso e conhecimento. Ed. UNIJUÍ, Ijuí, 3ª ed., 2014)
Em uma das práticas apresentadas pela autora, os alunos
deveriam misturar em um tubo de ensaio três gotas de solução
de nitrato de chumbo II e três gotas de bicromato de potássio.
Ao realizar esse experimento, os alunos deveriam observar
Leia o fragmento a seguir.
“A análise refere-se a um trecho da transcrição de uma aula na
qual um grupo de alunos vai discutir (...) sobre o fenômeno da
queima de uma fita de magnésio. A atividade proposta (...) inclui
a realização de cinco testes que correspondem a transformações
químicas que são acompanhadas por diferentes evidências.”
(MACHADO, A. H. Aula de Química: discurso e conhecimento. Ed. UNIJUÍ, Ijuí, 3ª ed., 2014)
Na prática citada com uma fita de magnésio, os alunos
observariam as seguintes evidências de transformações químicas:
I. a liberação de energia luminosa.
II. a formação de um sólido branco.
III. a necessidade de aquecimento.
Está correto o que se afirma em
A glicose, na presença de enzimas, passa por um processo de fermentação, no qual açúcares são quimicamente convertidos em
Duas garrafas pet de 500 mL tiveram o fundo retirado e foram
encaixadas, formando um tubo, como mostrado na figura.
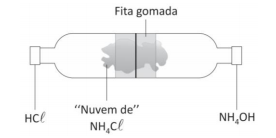
Em uma das tampas foi colocado um algodão embebido em ácido
clorídrico (HCL) e, na outra, um algodão embebido em hidróxido
de amônio (NH4OH). As tampas foram atarraxadas e, em alguns
segundos, os alunos foram surpreendidos com a formação de
uma “nuvem" esbranquiçada, próximo ao centro da montagem.
O professor explicou que a nuvem correspondia a uma espécie de
poeira de cloreto de amônio (NH4CL).
O experimento pode ser utilizado para demonstrar uma reação
de


