Na escala de temperatura Fahrenheit, o ponto de fusão da água corresponde a 32 °F, enquanto o ponto de ebulição da água corresponde a 212 °F. Na escala de temperatura Celsius, esses pontos correspondem, respectivamente, a 0 °C e 100 °C.
A tabela a seguir apresenta os estados do corpo humano correspondentes a diferentes temperaturas.
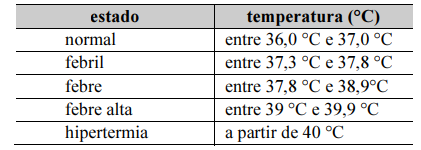
Com base no texto e na tabela precedentes, assinale a opção correta.
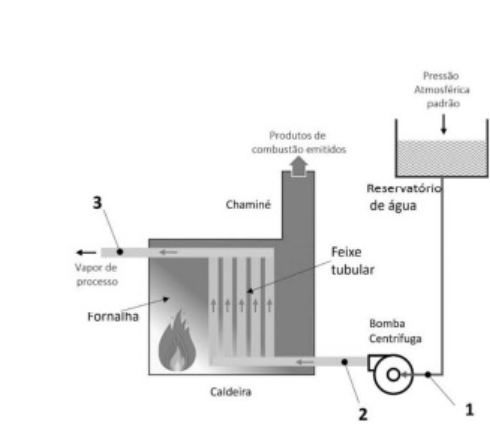
O diagrama precedente representa uma unidade geradora de vapor instalada ao nível do mar. Nos pontos 1 e 2, a temperatura da água, cuja densidade é igual a 1.000 kg/cm3, é igual a 25 °C, a elevação de pressão causada pela bomba é de 74 kPa, a temperatura no ponto 3 é igual a 133 °C, e o reservatório de água é mantido aberto e cheio, tendo sido instalado a 5 m de altura do ponto de sucção da bomba centrífuga.
A tabela seguinte apresenta as propriedades de saturação da água.
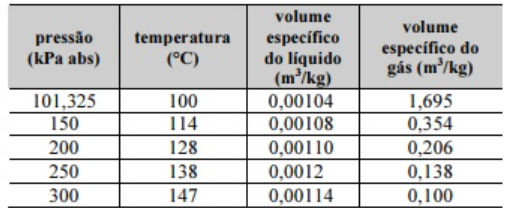
Com base nas informações apresentadas e considerando que a aceleração gravitacional local é igual a 10 m/s2, que a pressão atmosférica é igual a 101,325 kPa abs e que a perda de água é desprezível, julgue os itens que se seguem.
A aplicação de um revestimento com baixa emissividade sobre a superfície externa da fornalha possibilita a redução da perda de calor para o ambiente.
O calor de fusão de um sólido, Csólido, é a energia por unidade de massa necessária para fusão. Os materiais A, B e C são sólidos que estão em seus pontos de fusão. São necessários 300 J para fundir 4 kg do material A, 200 J para fundir 5 kg do material B e 240 J para fundir 6 kg do material C.
Assinale a alternativa em que o calor de fusão dos três sólidos se encontra em ordem decrescente.
A madeira é uma fonte de energia de baixo custo e fácil obtenção usada como combustível para alimentar caldeiras na geração de energia elétrica em termelétricas no Brasil. A queima da madeira aquece a água que, ao atingir o estado gasoso, passa por uma turbina convertendo parte da energia cinética em energia elétrica. Sabendo-se que o poder calorífico de uma remessa de madeira é de 3.000 kcal/kg, qual deve ser a quantidade de madeira necessária para transformar em vapor uma massa de 30 kg de água a uma pressão de 1 atm, inicialmente a 30 °C?
Ao tocarmos um piso de madeira, temos a sensação de que este é mais quente que o piso de ladrilho. É correto afirmar que isso ocorre porque
Em um calorímetro de capacidade térmica 30 cal/ºC, que contém 1,0 kg de água, ambos a 30 °C, coloca-se 600 g de gelo, inicialmente a –20 °C.
Dados:
Calor especifico da água 1,0 cal/g .°C
Calor especifico do gelo 0,5 cal/g .°C
Calor latente de fusão do gelo 80 cal/g
Desprezando as perdas de calor, após o equilíbrio térmico tem-se que
O corpo humano perde para o ambiente uma potência média de 100,0W na forma de calor. Esse valor fica 30 vezes maior quando o corpo está submerso em água, podendo causar hipotermia. Os sintomas da hipotermia vão desde tremores leves, mãos e pés dormentes, cansaço excessivo e lentidão nos movimentos. Esses sintomas se iniciam quando a temperatura corporal fica inferior a 35°C e pode ser fatal a partir de 21°C. Determine o intervalo de tempo em que uma pessoa de 75kg, inicialmente com temperatura de 37°C, passa a ter os primeiros sintomas de hipotermia quando estiver submersa em água.
(Considere o calor específico do corpo humano 1,1cal/g°C e 1,0cal = 4,0J.)
Com relação aos processos de propagação do calor, é correto afirmar que
Considere-se uma barra de aço com 10 cm de comprimento, 6 cm2 de área de seção transversal retangular e cujas extremidades sejam submetidas a temperaturas constantes e
diferentes, 20 ℃ em uma extremidade e 130 ℃ em outra. Nessa hipótese, sabendo-se que a condutividade térmica do aço vale 1,1 × 10−2 kcal ∙ m ∙ ℃ ∙ s−1, após alcançado o estado estacionário, o valor do fluxo de calor na barra, devido ao processo de transmissão de calor por condução, é
A tabela a seguir informa o calor específico de algumas substâncias.

I. A água, por ter um calor específico muito alto, é um excelente elemento termorregulador. A ausência de água faz com que, nos desertos, ocorram enormes diferenças entre a temperatura máxima e a mínima em um mesmo dia.
II. Para refrigerar uma peça aquecida, é comum mergulhá-la em água. Será mais eficiente, para resfriá-la, mergulhá-la em mercúrio. Só não se faz isso porque, além de muito caro, seus vapores são extremamente tóxicos.
III. Se cedermos a mesma quantidade de calor a amostras de massas iguais de alumínio e ferro, a temperatura da amostra de ferro aumentará o dobro do que aumenta a amostra de alumínio.
Está correto o que se afirma em
Duas amostras “A” e “B” de água no estado líquido de mesma massa (m) e mesmo calor específico (c) possuem temperatura iniciais diferentes TIA e TIB, sendo TIA maior que TIB. A mistura obtida com as duas amostras, após algum tempo, atinge a temperatura final TF. A quantidade de calor que a amostra “A” cedeu é igual a ____.
A taxa metabólica basal de um adulto é, em média, de 120 W. Ou seja, essa é a taxa com que esse adulto, quando em repouso, converte a energia química contida nos alimentos em energia térmica. Por serem animais homeotérmicos, os seres humanos apresentam a capacidade de controlar sua temperatura corpórea, mantendo-a aproximadamente constante. Assim, quando em repouso, devem transferir energia para o ambiente a uma taxa igual à taxa metabólica basal. Considere que uma pessoa de 80 kg esteja dormindo em um local, onde, em 2 h, a temperatura ambiente se eleva de 20 ºC para 23 ºC. Considerando a taxa metabólica basal citada anteriormente, o calor específico médio do corpo dessa pessoa é de
Na maioria das vezes, a água pode ser utilizada para evitar incêndios. Entretanto, nem todos os tipos de incêndio podem ser apagados com água.
Uma propriedade física importante da água e que contribui para a utilização dela como meio para se evitar incêndios é a(o)
Um ebulidor é um aparelho que funciona por efeito joule. Quando ligado em 110V e colocado dentro de um béquer contendo 0,5 kg de água a uma temperatura de 20°C, consegue elevar a temperatura dessa amostra para 80°C em 4,0 minutos.

Dados:
• calor específico da água c = 4,0J/g°C
• 1 cal = 4,0 J
Considerando que toda a energia liberada pelo ebulidor seja utilizada para aquecer apenas a água, podemos afirmar que a potência dele vale
Uma quantidade de gelo é aquecida do ponto de fusão (TF) até uma temperatura acima do ponto de ebulição da água (TE). O gráfico que melhor expressa a entropia S em função da temperatura T nesse processo é


